Izokorični postopek
- 3340
- 339
- Don Nitzsche
Kaj je izokorični postopek?
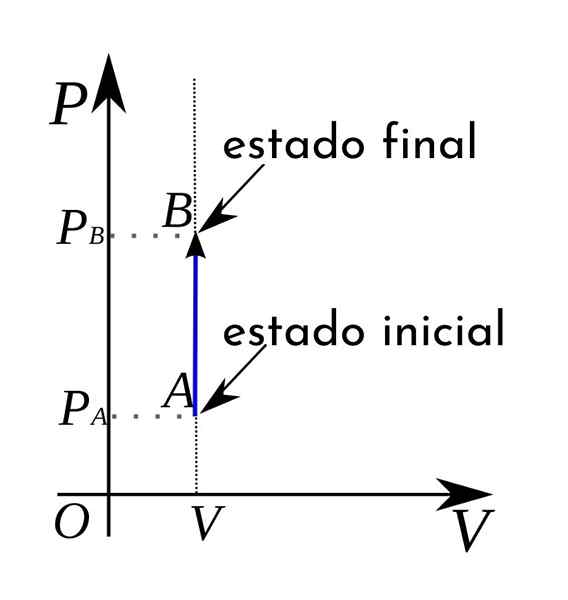
A Izokorični postopek To je vsak termodinamični postopek, v katerem glasnost ostane konstanten. Ti procesi pogosto dobijo tudi ime izometričnega ali izovolumetričnega. Na splošno se lahko pri konstantnem tlaku pojavi termodinamični postopek in se nato imenuje izobarično.
Ko se pojavi pri konstantni temperaturi, se v tem primeru reče, da gre za izotermalni postopek. Če med sistemom in okoljem ni izmenjave toplote, potem se govori o adiabatic. Po drugi strani se, ko je konstantna prostornina, ustvarjen postopek imenuje izokoričen.

V primeru izokoričnega procesa je mogoče potrditi, da je v teh procesih delo tlak-količina nična, saj to izhaja iz množenja tlaka s povečanjem volumna.
Poleg tega so v termodinamičnem diagramu tlačnega volumna izokorični procesi predstavljeni v obliki navpične ravne črte.
Formule in izračun
Prvo načelo termodinamike
V termodinamiki se delo izračuna iz naslednjega izraza:
W = p ∙ ∆ v
V tem izrazu W je delo, merjeno v joulesu, p tlak, izmerjen v Newtonu na kvadratni meter, in ∆ V je variacija ali povečanje volumna, izmerjeno v kubičnih merilih.
Prav tako znano kot prvo načelo termodinamike ugotovi, da:
∆ U = Q - W
V tej formuli je to delo, ki ga opravlja sistem ali v sistemu, ki jo sistem prejme ali izda, in ∆ u To je notranja sprememba energije sistema. Ob tej priložnosti se trije veličini merijo v joulesu.
Ker je v izokorskem procesu delo nič, se izkaže, da je izpolnjeno:
Vam lahko služi: Neptun (planet)∆ U = QV (Od, ∆ v = 0, in zato w = 0)
To pomeni, da je notranja sprememba energije sistema posledica samo izmenjave toplote med sistemom in okoljem. V tem primeru se prenesena toplota imenuje toplota v konstantno prostornino.
 Toplotna zmogljivost pri konstantni prostornini
Toplotna zmogljivost pri konstantni prostornini
Toplotna zmogljivost telesa ali sistema je posledica delitve količine energije v obliki toplote, prenašane na telo ali sistem v določenem postopku in spremembo temperature, ki jo doživlja isto.
Ko se postopek izvede s konstantno prostornino, se izgovori o toplotni zmogljivosti do konstantne prostornine in ga označuje Cv (Molarna toplotna zmogljivost).
V tem primeru bo izpolnjeno:
Qv = N ∙ cv ∙ ∆t
V tej situaciji je n število molov, cv Je zgoraj omenjena toplotna zmogljivost mola do konstantne prostornine in ∆t je zvišanje temperature, ki ga doživlja telo ali sistem.
Dnevni primeri izokoričnih procesov
Lahka si je predstavljati izokorični proces, treba je razmišljati le o postopku, ki se pojavi ob konstantni glasnosti; to je, v katerem posoda, ki vsebuje material ali materialni sistem, ne spreminja glasnosti.
Primer bi lahko bil primer (idealen), zaklenjen v zaprti posodi, katere prostornine ni mogoče spremeniti na kakršen koli način, ki je na voljo toplota. Recimo, da je primer plina zaklenjen v steklenico.
S prenosom toplote na plin, kot je že pojasnjeno, bo na koncu povzročil povečanje ali povečanje njegove notranje energije.
Vzvratni postopek bi bil plin, zaprt v posodi, katerega prostornine ni mogoče spremeniti. Če se plin ohladi in daje toploto okolju, bi se tlak plina in vrednost notranje energije plina zmanjšala.
Lahko vam služi: diskretna spremenljivka: značilnosti in primeriIdealen cikel Otto
Cikel OTTO je idealen primer cikla, ki ga uporabljajo bencinski stroji. Vendar je bila njegova prvotna uporaba v strojih, ki so v plinastim stanju uporabljali zemeljski plin ali druga goriva.
Vsekakor je Ottov idealni cikel zanimiv primer izokoričnega procesa. Pojavi se, ko v avtomobilu z notranjim zgorevanjem zgorevanje bencina in zraka pride takoj.
V tem primeru pride do povečanja temperature in tlaka plina znotraj jeklenke, ki ostane konstantna prostornina.
Praktični primeri
Prvi primer
Glede na plin (idealno), zaklenjen v valj, ki je opremljen z batom, navedite, ali so naslednji primeri primeri izokoričnih procesov.
- 500 j dela na plin je končano.
V tem primeru to ne bi bil izokorični postopek, ker je za opravljanje dela na plinu potrebno, da ga stisnete, zato spremenijo njegovo količino.
- Plin se vodoravno razširi bat.
Spet to ne bi bil izokorični postopek, saj širitev plina pomeni različico njegove prostornine.
- Bat jeklenke je pritrjen, tako da plina ni mogoče premakniti in plin ohladiti.
Ob tej priložnosti bi bil to izokorični proces, saj ne bi bilo nobenih sprememb glasnosti.
Drugi primer
Določite variacijo notranje energije, ki bo doživela plin v posodi z prostornino 10 L, predloženega na 1 atm tlaka, če se njegova temperatura v izokorskem procesu dvigne s 34 ° C do 60 ° C Cv = 2.5 ·R (biti R = 8.31 j/mol · k).
Lahko vam služi: Graff Van Generator: zabave, kako deluje, aplikacijeKer gre za konstanten volumen postopek, se bo notranja sprememba energije pojavila le kot posledica toplote, dobavljene v plinu. To je določeno z naslednjo formulo:
Qv = N ∙ cv ∙ ∆t
Za izračun dobavljene toplote je najprej treba izračunati mole plina v posodi. Za to se je treba zateči k enačbi idealnih plinov:
P ∙ v = n ∙ r ∙ t
V tej enačbi je n število molov, r je konstanta, katere vrednost je 8,31 j/mol · k, t je temperatura, p je tlak, na katerega je plin, izmerjen v atmosferi, podvržen in t je t, t je izmerjena temperatura v Kelvinu.
Očiščena je in pridobljena:
n = r ∙ t/ (p ∙ v) = 0, 39 molov
Tako da:
∆ U = QV = N ∙ cv ∙ ∆t = 0,39 ∙ 2,5 ∙ 8,31 ∙ 26 = 210,65 J

