Atomski modeli
- 4534
- 1426
- Raymond Moen
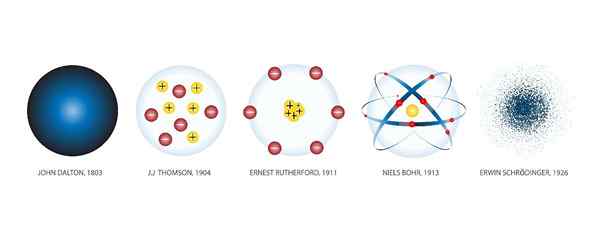
 Atomski modeli so različne grafične predstavitve, ki so jih v zgodovini dajali atomom. Shuttersock
Atomski modeli so različne grafične predstavitve, ki so jih v zgodovini dajali atomom. Shuttersock Kaj so atomski modeli?
The Atomski modeli So grafične predstavitve strukture in delovanja atoma. Skozi zgodovino je bilo veliko modelov.
To je zato, ker se je ideja o atomu kot temeljnem bloku, ki je narejena, rojena pred tisoč leti, v starodavni Grčiji. Takrat je bil atom le produkt filozofskih špekulacij.
Ko so bila narejena nova znanstvena odkritja, so bili ustvarjeni novi modeli za vključitev pridobljenega znanja. In tako se je zgodilo že stoletje po stoletju do danes, ko nam je tehnologija omogočila opazovanje atomov z mikroskopi in določitev pravilnega modela.
Kaj so atomi?
Atomi so submikroskopske strukture, od katerih se tvori vse predmet, ki ga zaznamo, in s katerimi vsak dan komuniciramo, od lastnega telesa, hrane, oblačil, ki jih nosimo.
Tudi sonce, luna, planeti, zvezde in galaksije tvorijo z atomi.
Te so tako majhne, da jih ni mogoče videti s skupnimi mikroskopi. Drugi so potrebni za večjo moč, imenovani ultraminroskopi. Vendar atomi niso najmanjše enote narave.
Atomi nastajajo še manjši delci: protoni, nevtroni in elektroni.
Protoni imajo pozitiven električni naboj, medtem ko nevtroni nimajo električnega naboja. Ti dve vrsti delcev tvorita jedro atoma.
Vrtenje okoli jedra, kot so planeti okoli sonca, so elektroni, ki imajo negativni električni naboj.
Atomski model Demokrita

Demokrit Abdera je bil grški filozof, ki je živel med 460 in 370 pred sedanjo dobo. Potrdil je, da so vse snovi tvorili drobni delci, ki jih je imenoval atomi, kar v grščini pomeni nedeljivo.
Po demokraciji je atom najmanjši del, v katerem je mogoče zadevo razdeliti. Obstaja neskončno število, ki so neuničljive, neverjetne, večne in popolnoma kompaktne, brez pore. Obstaja več vrst, ki se razlikujejo po obliki, velikosti, položaju in načinu, kako so pripravljeni.
Lahko vam služi: nesreče, ki jih povzroča človek pri uporabi znanosti in tehnologijeAristotel je zavrnil teorijo demokracije in nato popolnoma pozabljeno do pojava sodobne znanosti.
Dalton Atomski model

John Dalton (1766-1844) je bil angleški meteorolog, ki je bil zainteresiran za preiskavo zakonov, ki urejajo vedenje plina. Plod njegovega dela na tem področju je bil prvi atomski model moderne znanosti, ki ga je naredil leta 1803.
Ker obstoj protonov in elektronov še ni bil odkrit, je Dalton dejal, da je atom najmanjši del, v katerem je mogoče snov razdeliti in je zato sam po sebi nedeljivo.
Po Daltonu so atomi trdni in imajo sferično obliko, kot baseball kroglica. Dalton je ilustriral svojo teorijo, ki je izrezal v lesu, skupaj s svojimi pomočniki, na desetine sfer, ki predstavljajo atome različnih kemičnih elementov.
Ta model je veljal do odkritja elektrona.
Thomson Atomski model
Angleški fizik Joseph John Thomson (1865-1940) je moral narediti eno najpomembnejših odkritij moderne znanosti: Electron.
Bilo je leta 1897 v laboratoriju Cavendish University v Cambridgeu v Angliji, kjer plak še vedno spominja na veliko odkritje.
Thompson in njegovi pomočniki projicirajo katodne žarke na električnem polju. Po stiku s poljem so žarki odklonili široke kote. To je potrdilo, da imajo katodni žarki negativni električni naboj. Ti negativno nabiti delci so jih imenovali elektroni.
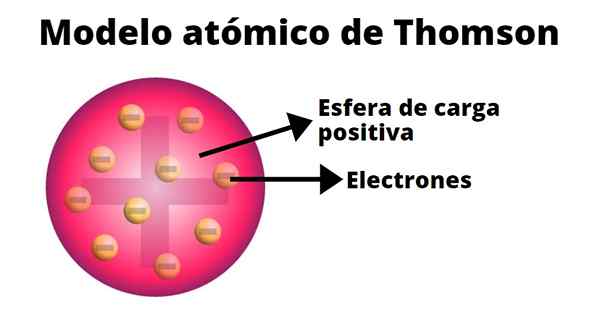
Thomson je domneval, da so elektroni vdelani v atome. Njegov atomski model izvira iz leta 1904.
Puding rozin
V Thompsonovem atomskem modelu je atom trdna krogla s pozitivno obremenitvijo (protoni), na kateri se nevtroni (negativna obremenitev) naključno porazdelijo, kot rozine, vržene na pudin. Zato je bil ta model znan kot "Pudin de Pasas".
Po Thompsonu ima atom polmer 0,00000001 centimetrov, njegova obremenitev pa je nevtralna, saj imajo protoni in elektroni enako obremenitev, vendar nasprotnega znaka.
Thompsonov model ne predstavlja nevtronov.
Atomski model Rutherford
Ernest Rutherford (1871-1937), neozilski fizik, je bil eden najvidnejših Thomsonovih študentov.
Vam lahko služi: korelacijske raziskaveLeta 1911 in na podlagi nedavnega odkritja radioaktivnosti je Rutherford izvedel naslednji eksperiment: izstrelili so alfa radioaktivne delce visoke hitrosti in energije proti listu zlata.
Če bi bil Thompsonov atomski model pravilen, bi alfa delci prešli skozi list, ne da bi odstopali ali z nepomembnim odstopanjem. Ko pa so izračunali kot odstopanja od delcev, so ugotovili, da je širok, in da nekateri celo odskočijo proti zlati listi.
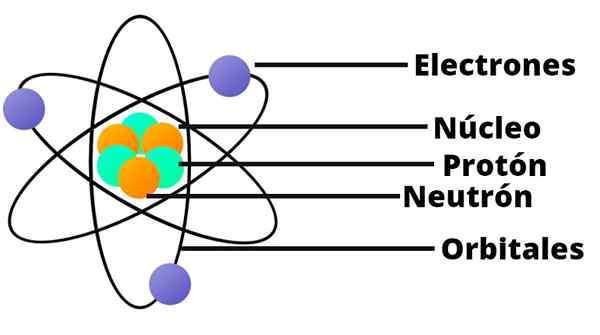
S tem rezultatom je Rutherford razumel, da bi moral atom imeti zelo majhno in zelo zgoščeno jedro. To jedro je bilo pozitivno nabito.
Majhen sončni sistem
Atomski model Rutherforda je kot miniaturni sončni sistem. V središču, na mestu, ki bi ustrezalo soncu, je jedro s svojimi pozitivno obremenjenimi protoni. Okoli tega, kot planeti, so naključno razporejeni elektroni.
Rutherford je tudi ugotovil, da je masa atoma enakovredna vsoti mase elektronov in protonov.
Atomski model Bohr
Čeprav je bil model Rutherforda v primerjavi s prejšnjimi modeli nesporno napredovanje, je imel pomembne pomanjkljivosti. Na primer, če bi elektroni učinkovito orbitalirali okoli jedra, bi na koncu izgubili energijo in zrušili jedro. Toda to se očitno ni zgodilo.
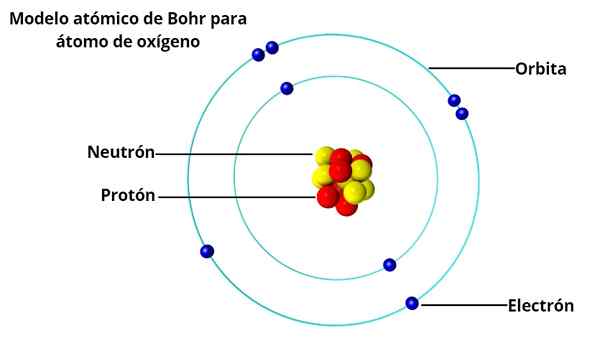
Danski fizik Niels Bohr (1885-1962), študent Rutherforda z univerze v Manchestru (Anglija), ki bi leta 1913 predlagal atomski model.
Krožne orbite
V atomskem modelu Bohr elektroni ne krožijo prosto okoli. Vsaka orbita se imenuje energija ali raven energije.
Na podlagi preiskav Maxa Plancka in Alberta Einsteina je ugotovil, da ima vsak elektron v njihovi orbiti določeno količino energije.
Medtem ko orbirate stabilno okoli jedra, naj bi elektroni v nepremični državi. Po drugi strani pa, ko elektron "skoči" na nižjo energijsko orbito, obstaja foton.
Vam lahko služi: metodologijaVendar model BOHR ni bil uspešen, da bi razložil delovanje atomov z več kot enim elektronom.
Sommerfeld Atomski model
Arnold Sommerfeld (1868-1951) je bil nemški fizik, ki je svoje delo posvetil širjenju Bohrovega atomskega modela. Ta razširjeni model je bil predstavljen leta 1916.
Na podlagi Einsteinove teorije relativnosti je Sommerfeld odkril, da nekateri elektroni krožijo okoli jedra pri hitrosti blizu svetlobe (300.000 kilometrov na sekundo).
Naslednje spremembe je naredil tudi za model Bohr:
- Elektroni se gibljejo okoli jedra v krožnih in eliptičnih orbitah. Bohr samo prepoznane krožne orbite.
- Znotraj iste energijske ravni so podvrsti z nekoliko drugačnimi energijami.
Kvantni mehanski model (Broglie, Heisenberg in Schrödinger)
To je najbolj natančen atomski model, ki je znan in je trenutno sprejet, z nekaj nadaljnjimi dodatki. Razvili so ga trije znanstveniki: nemški Werner Heisenberg (1901-1976), avstrijski Erwin Schrödinger (1887-1961) in Francoz Louis de Broglie (1892-1987).
Ta model zavrže idejo o elektronih, ki krožijo jedro. Namesto tega imamo elektronske oblake, ki so prostori okoli jedra, v katerih je mogoče najti elektron. To se obnaša kot nepremičen val.
Verjetnost, da ga najdete, se izračuna z enačbo, ki jo je vzpostavil Schrödinger.
To je kvantni mehanski model atoma, ki se je začel iz Schrödingerjeve enačbe. S to enačbo bi lahko vedeli verjetnost, da boste našli elektron na določeni točki atoma.
V tem modelu se vsak elektron premakne v določeno smer, ki jo določa štiri kvantna številka, ki so: glavno kvantno število, sekundarno kvantno število, magnetno kvantno število in kvantno število Spin.
Ni dveh elektronov, ki imata enake kvantne številke, kot je navedeno z načelom izključevanja, ki ga je odkril fizik Wolfgang Pauli.
Reference
- (2010). Atom. Sodobna enciklopedija Britanska.
- (s. F.). Atomski model demokracije, filozofski atomorizem. Vzeti iz energijsko-jedrskega.mreža.
- (s. F.). Sommerfeld Atomski model, razširitev na model Bohr. Vzeti iz energijsko-jedrskega.mreža.
- Bertsch, g. F.; Trefil, James in McGrayne, Sharon Bertsch (2021). Atom. Enciklopedija Britannica. Vzeti iz Britannice.com.
- Duignan, b. (2021). Demokrit. Enciklopedija Britannica. Vzeti iz Britannice.com.
- Sodelavci New World Encyclopedia. (2021). Atom. Vzeti iz Newworldiklopedije.org.
- Zita, Ana. (s. F.). Atomski modeli. Vzeti iz Todamaterije.com.

