Buteno

- 868
- 191
- Cary Goyette
 Kemična struktura buutena
Kemična struktura buutena Kaj je buteno?
On Buteno To je ime, ki prejme serijo štirih izomerov s kemijsko formulo C4H8. So alkeni ali olefini, to je, da imajo v svoji strukturi dvojno vez c = c. Poleg tega so ogljikovodiki, ki jih najdemo v nahajališčih nafte ali izvirajo s toplotnim razpokom in pridobivanjem produktov nižje molekulske mase.
Štirje izomeri reagirajo s toploto, ki sprošča kisik, in rumenim plamenom. Lahko reagirajo tudi s širokim spektrom majhnih molekul, ki se dodajo njihovi dvojni vezi.
Toda kaj so izomeri butno? Na zgornji sliki je za 1 buten predstavljena struktura z belimi kroglicami (vodiki) in črno (ogljikovod). 1-buten je najpreprostejši izomer ogljikovodika c4H8.
Upoštevajte, da obstaja osem belih sfer in štirih črnih kroglic, kar se strinja s kemijsko formulo.
Ostali trije izomeri so cis in trans 2-butena ter iso-buten. Vsi imajo zelo podobne kemijske lastnosti, čeprav njihove strukture povzročajo razlike v fizikalnih lastnostih (fuzijske in vrelišča, gostote itd.).
Tudi njihovi spektri imajo podobne vzorce absorpcijskih pasov.
Pogovorno je 1-buten imenovan kot buteno, čeprav se 1-buten nanaša samo na en sam izomer in ne na generično ime. Te štiri organske spojine so plini, vendar jih je mogoče utekočiniti do visokih tlakov ali kondenj.
So vir toplote in energije, reagentov za sintezo drugih organskih spojin in predvsem potrebne za izdelavo umetne gume po sintezi butadiena.
Fizikalne in kemijske lastnosti Butana
Molekularna teža
56.106 g/mol. Ta teža je enaka za vse izomere formule C4H8.
Fizični vidiki
Je brezbarven in vnetljiv plin (kot drugi izomeri) in ima relativno aromatičen vonj.
Vrelišče
Vrezne točke za izomere Buta so naslednje:
1 -Buten: -6 ° C
Cis-2-buten: 3.7. c
Trans-2-buten: 0.96 ° C
2 -metilpropene: -6.9 ° C
Tališče
1 -Butene: -185.3. c
Cis-2-buten: -138.9 ° C
Trans-2-buten: -105.5. c
2 -methylpropeno: -140.4. c
Topnost
Butano je zaradi svoje apolarne narave zelo netopen v vodi. Vendar se odlično raztopi v nekaterih alkoholih, kot so benzen, toluen in ethers.
Gostota
0.577 do 25 ° C. Zato je manj gosta kot voda in v posodi bi se nahajala nad isto.
Reaktivnost
Kot vsaka alkena je tudi njegova dvojna vez dovzetna za dodajanje molekul ali oksidacijo. Zaradi tega je butno in njegovi izomeri reaktivni. Po drugi strani so vnetljive snovi, zato pred presežkom temperature reagirajo s kisikom zraka.
Vam lahko služi: butanal: struktura, lastnosti, uporabe in tveganjaKemična struktura buutena
Na zgornji sliki je predstavljena struktura 1-butena. Na levi si lahko ogledate lokacijo dvojne vezi med prvim in drugim ogljikom.
Molekula ima linearno strukturo, čeprav je območje okoli povezave C = C ravno zaradi hibridizacije SP2 teh ogljikov.
Če bi bila 1-butenska molekula obrnjena pod kotom 180 °, ista molekula ne bi imela očitnih sprememb, zato ji primanjkuje optične aktivnosti.
Kako bi medsebojno delovale vaše molekule? Povezave C-H, C in C-C so apolarna narava, zato nobeden od njih ne sodeluje pri oblikovanju dipolnega trenutka.
Posledično molekule CHO2= Chch2Pogl3 Morajo komunicirati prek londonskih disperzijskih sil.
Desni konec butena tvori takojšen dipol, ki na kratki razdalji polarizira sosednje atome sosednje molekule. Po drugi strani pa levi konec povezave C = C deluje na prekrivanju oblakov π na drugem (na primer dve rezini ali listi).
Ker obstajajo štirje ogljikovi atomi, ki sestavljajo molekulsko okostje, njegove interakcije skoraj niso dovolj, da ima tekoča faza vrelišče -6 ° C.
Ustavni in geometrijski izomeri
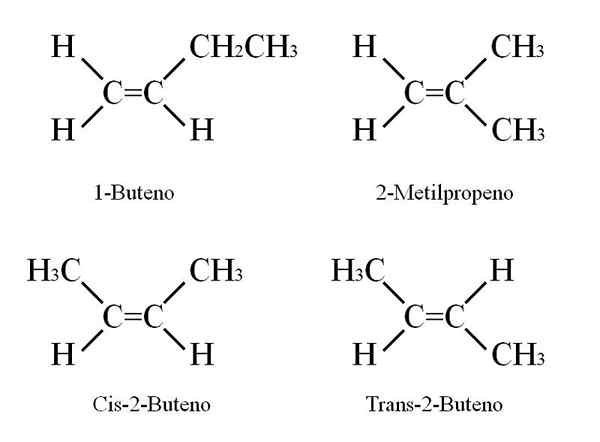 Burene strukture. Vir: Gabriel Bolívar
Burene strukture. Vir: Gabriel Bolívar 1-buten ima molekularno formulo c4H8; Vendar imajo lahko druge spojine v svoji strukturi enak delež atomov C in H.
Kako je mogoče? Če natančno opazimo strukturo 1-butena, lahko zamenjava ogljikove nadomestke c = c. Ta izmenjava proizvaja druge spojine iz istega okostja.
Poleg tega se lahko položaj dvojne vezi med C-1 in C-2 premakne proti C-2 in C-3: CH3Ch = chch3, 2-buten.
V 2-butenu lahko H atomi postavimo na isto stran dvojne vezi, kar ustreza CIS stereoizomeru; ali v nasprotni prostorski orientaciji v trans stereoizomerju. Oba predstavljata tisto, kar je znano tudi kot geometrijski izomeri. Enako velja za skupine -CH3.
Upoštevajte tudi, da če ostane v Chojevi molekuli3Ch = chch3 Atomi H na eni strani in skupine CH3 V drugem bi dobili ustavni izomer: ch2= C (Ch3)2, 2-metilpropen (znan tudi kot ISO-buten).
Vam lahko postreže: kalijev nitrat (KNO3)Te štiri spojine imajo isto formulo c4H8 Vendar različne strukture. 1-buten in 2-metilpropen sta ustavni izomeri; in geometrijske izomere CIS in trans-2 med njima dva (in ustavno glede na ostale).
Stabilnost
Toplota zgorevanja
Iz zgornje slike, kdo od štirih izomerov predstavlja najbolj stabilno strukturo? Odgovor najdete na primer v zgorevalni toploti vsakega od njih.
Ko reagira s kisikom, izomer s formulo C4H8 se spremeni v co2 Sproščanje vode in toplote:
C4H8(g) + 6o2(g) => 4co2(g) + 4h2O (g)
Izgorevanje je eksotermično, tako da se več toplote sprosti, bolj nestabilen je ogljikovodik. Zato bo od štirih izomerov, ki sproščajo manj toplote, da bi goreli v zraku, najbolj stabilna.
Izgorevanje za štiri izomere so:
-1-buten: 2717 kJ/mol
-Cis-2-buten: 2710 kJ/mol
-Trans-2-buten: 2707 kJ/mol
-2-metilpropeno: 2700 kJ/mol
Upoštevajte, da je 2-metilpropen izomer, ki oddaja manj toplote. Medtem ko je 1-buten tisti, ki sprošča največ toplote, kar pomeni večjo nestabilnost.
Stericni in elektronski učinek
To razliko stabilnosti med izomeri lahko odštejemo neposredno iz kemijske strukture.
Po Alkeni po besedah Alkenov tisti, ki ima najbolj substituente R, pridobi večjo stabilizacijo svoje dvojne vezi. Tako je 1-buten najbolj nestabilen, ker ima komaj substituent (-CH2Pogl3); to pomeni, da je monosustuido (rhc = cho2).
CIS in trans izomeri 2-butena se razlikujejo po energiji zaradi napetosti stene van der, ki izvira iz stericnega učinka.
V Isomerju CIS obe skupini Ch3 Na isti strani dvojne vezi se med seboj odbijajo, medtem ko so v trans izomeru dovolj oddaljeni drug od drugega.
Toda zakaj je potem 2-metilpropen najbolj stabilen izomer? Ker elektronski učinek posreduje.
V tem primeru, čeprav gre za raztopljen alken, dve skupini CH3 So v istem ogljiku; v položaju geminala glede drugega.
Te skupine stabilizirajo ogljik z dvojno vezi, ki mu daje del svojega elektronskega oblaka (saj je relativno bolj kisla s hibridizacijo SP2).
Poleg tega imata v 2-buteni le dva izomera samo 2. ogljikove ogljike; Medtem ko 2-metilpropen vsebuje 3. ogljik, večje elektronske stabilnosti.
Vam lahko služi: struktura materialov: koncept in primeriMedmolekularne sile
Stabilnost štirih izomerov sledi logičnemu zaporedju, vendar se ne dogaja z medmolekularnimi silami. Če se primerjajo njihove točke in vrelišča, bodo ugotovili, da ne upoštevajo istega reda.
Pričakovano bi bilo, da bo Trans 2-buten predstavil največje medmolekulske sile za večji površinski stik med dvema molekulama, za razliko od cis-2-butena, katerega okostje črpa A C. Vendar cis-2-buten zavre pri višji temperaturi (3.7. c), da je trans izomer (0.96 ° C).
Podobne vrelišča za 1-buten in 2-metilpropen bi jih pričakovali, ker so strukturno zelo podobni. Vendar se v trdnem stanju razlika korenito spreminja. 1 -Buten se topi na -185.3 ° C, medtem ko 2 -metilpropen pri -140.4. c.
Poleg tega se izomer cis-2-butena topi na -138.9 ° C, pri temperaturi zelo blizu 2-metilpropena, kar lahko pomeni, da imajo v trdni snovi enako stabilno ureditev.
Iz teh podatkov je mogoče sklepati, da kljub temu, da poznajo najbolj stabilne strukture, ne osvetlijo dovolj v vedenju, kako medmolekularne sile delujejo v tekočini; In še več, v trdni fazi teh izomerov.
Butenus uporablja
-Butnine, glede na toploto zgorevanja, se lahko preprosto uporabijo kot vir toplote ali goriva. Tako bi bilo pričakovati, da je plamen 1-butena vroč več kot od ostalih izomerov.
-Uporabljajo jih lahko kot organska topila.
-Služijo kot dodatki za dvig stopnje oktana bencina.
-Znotraj organske sinteze 1-buten sodeluje pri proizvodnji drugih spojin, kot so: butilen oksid, 2-glutanol, Succinimida in Terbutilmecaptano (ki se kuhinjski plin uporablja svoj značilen vonj).
Tudi od izomerov butene lahko pridobite butadieno (cho2= Ch-ch = ch2), od katerih je sintetizirana umetna guma.
Poleg te sinteze bo raznolikost izdelkov odvisna od tega, katere molekule so dodane v dvojno vez.
Na primer, alkil halogenide je mogoče sintetizirati, če reagirajo s halogeni; alkoholi, če dodajo vodo v kislem mediju; in tretji butlere, če dodajo alkohole z nizko molekulsko maso (na primer metanol).
Reference
- Frančišek a. Želva. Organska kemija. Karboksilne kisline (šesta izdaja, stran 863-866). MC Graw Hill.
- Wikipedia (2018). Buteno. Vzet od: je.Wikipedija.org
- YPF (julij). Butnajci. [PDF]. Vzet od: ypf.com
- William Reusch (2013). Dodatne reakcije Alkes. Okrevano od: 2.Kemija.MSU.Edu
- Pubchem (2018). 1-buten. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov

