Svinčeno strukturo jodida, lastnosti, pridobivanje, uporabe

- 3509
- 93
- Percy Feeney
On Svinčeno jodid Gre. Njegova kemična formula je BDP2. To je strupena spojina. Ker je vodilna, je škodljiva za človeka, živali in naravne ekosisteme. Poleg tega lahko jodid povzroči tudi nekaj bolezni.
Spojina BDP4, To je, s svincem v oksidaciji +4 se zdi, da ne obstaja, verjetno zaradi zmanjšanja zmogljivosti jodidnega iona (i-). BDP2 Je trdna rumena barva, ki je topna v vodi.
 Svinčeno jodid (BDP2) trdno. W. Oelen/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons.
Svinčeno jodid (BDP2) trdno. W. Oelen/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons. Dobimo ga lahko z reakcijo ionske izmenjave med jodidno soljo in svincem, ki sta topna v vodi.
Ima polprevodniške lastnosti, zato je večina njegovih trenutnih aplikacij v fotovoltaičnih napravah, detektorjih določenih sevanja in senzorjev.
Ena najbolj preučenih uporabe te spojine je sončna celica Perovskita, ki so se izkazale za zelo učinkovite in nizke stroške.
[TOC]
Struktura
V svincu jodid je zveza med atomi le delno ionska. Atomi tvorijo plasti s šesterokotno strukturo in so med seboj povezane s šibkimi silami van der Waalsa.
Te sile niso niti ionske niti kovalentne, so šibke interakcije med elektronskimi plastmi atomov.
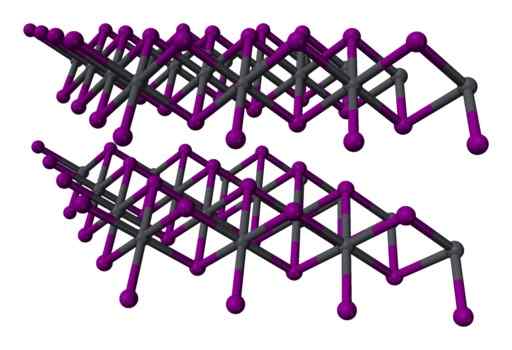 Dve -player Three -player Struktura2 kristalna. Siva = svinec; Vijolična = jod. Benjah-bmm27 / javna domena. Vir: Wikimedia Commons.
Dve -player Three -player Struktura2 kristalna. Siva = svinec; Vijolična = jod. Benjah-bmm27 / javna domena. Vir: Wikimedia Commons. Nomenklatura
- Svinčeno jodid
- Svinčeno jodid (ii)
- Svinčeno diyoduro
- Pluboso jodid
Lastnosti
Fizično stanje
Svetlo rumena kristalna trdna. Šesterokotni kristali.
 Šesterokotni kristali svinčenega jodida. Alessandro e damiano/cc by (https: // creativeCommons.Org/licence/by/4.0. Vir: Wikimedia Commons.
Šesterokotni kristali svinčenega jodida. Alessandro e damiano/cc by (https: // creativeCommons.Org/licence/by/4.0. Vir: Wikimedia Commons. Molekularna teža
461 g/mol
Tališče
410 ° C
Vrelišče
954 ° C, zavremo z razpadom.
Gostota
6,16 g/cm3
Topnost
Rahlo topno v vodi: 0,076 g/100 ml pri 25 ° C. Vroča voda topna. Netopna v alkoholu in hladni klorovodiki (HCl).
Vam lahko služi: natrij: zgodovina, struktura, lastnosti, tveganja in uporabeKemične lastnosti
Njegove oksidacijske in zmanjševanje lastnosti so šibke. Vendar lahko predstavite reakcije oksidenukcije.
Čeprav je v vodi zelo malo topen v koncentriranih raztopinah alkalnih jodidov, kot je kalijev jodid (ki). Topna je v koncentrirani raztopini natrijevega acetata (CH3Žep). Prosto se raztopi v raztopini natrijevega tiosulfata (NA2S2Tudi3).
Nekateri avtorji navajajo, da je v vodi lahko ustvarjen ion PBI+ In če obstaja presežek iona (i-) lahko oblikujejo bolj zapletene vrste, kot je BDP3- in BDP42-, med drugim.
Ni vnetljivo.
Druge fizikalne lastnosti
Obnaša se kot polprevodnik, to je, da lahko ali ne izvaja električne energije, odvisno od pogojev, za katere je podvržen.
To je neposredna vrzel polprevodnik, torej da je eden od njegovih elektronov prešel iz pasu Valencia v vožnjo, mora imeti le količino energije, ki je enaka prepovedani pasovni širini.
Zaradi visokega atomskega števila njegovih elementov (Pb = 82, i = 53) ima visoko fotoelektrično zmogljivost. Njegov 2,5 vrzeli omogočajo fotonapetostne predstave z visoko učinkovitostjo pri temperaturah do 250 ° C.
Pridobivanje
Pripravimo ga lahko tako, da reagirate na vodotopno spojino z iarhidno kislino (HI) ali s topnim kovinskim jodidom. Na primer, vodna raztopina svinčevega acetata s kalijevim jodidom se meša:
PB (pogl3COO)2 + 2 Ki → BDP2↓ + 2 k (izberite3COO)
Ta vrsta reakcije je znana kot "ionska izmenjava", ker se kationi in anioni izmenjujejo med soli.
V omenjenem primeru je kalijev acetat zelo topen v vodi in ostane raztopljen, kalijev jodid. Čiščenje poteka s prekristalizacijo spojine v vodi.
Vam lahko služi: kristalizacijaPadavine PBI2 Na naslednji sliki je razvidno na epruveti, kjer svinčeno nitrat (ii) (PB (št3)2) in kalijev jodid (ki) v vodni raztopini. Ta učinek se imenuje "zlato zlato".
 Dež zlata iz BDP2. Stefano SCT/CC by-S (https: // createCommons.Org/licence/by-sa/4.0. Vir: Wikimedia Commons.
Dež zlata iz BDP2. Stefano SCT/CC by-S (https: // createCommons.Org/licence/by-sa/4.0. Vir: Wikimedia Commons. Prijave
Kot polprevodnik
Uporablja se kot detektor za visokoenergijske fotone, kot so x -roji in gama žarki. Uporablja se lahko v fotovoltaičnih napravah, fotocelicih, LED lučkah, optičnih detektorjih ter v biološki klasifikaciji in senzorjih.
Če se vnese v nanostrukture, ga lahko uporabite v fotokatalizi in sončnih celicah. Poleg tega veliko nanodelcev BDP2 Imajo svetilne lastnosti.
 Svinčevi jodid se uporablja v medicinskih detektorjih X -Ray. Avtor: LKCJJANG40090. Vir: Pixabay.
Svinčevi jodid se uporablja v medicinskih detektorjih X -Ray. Avtor: LKCJJANG40090. Vir: Pixabay. Sončne celice
BDP2 Je posrednik v sintezi Perovskita, namenjenih sončnim celicam. Ta vrsta fotovoltaičnih celic vsebuje metilamonij in svinčeno jodid (izberite3Nh3BDP3) Na podlagi strica2.
Takšne naprave imajo visoko učinkovitost in nizke stroške, zato so bile veliko študij in raziskav.
 Sončne celice na strehi hiše na polju. Sončne celice, v katerih se uporablja PBI2 So zelo učinkoviti in niso zelo dragi, zato jih lahko v prihodnosti uporabljamo v hišah. Avtor: Manfred Antranias Zimmer. Vir: Pixabay.
Sončne celice na strehi hiše na polju. Sončne celice, v katerih se uporablja PBI2 So zelo učinkoviti in niso zelo dragi, zato jih lahko v prihodnosti uporabljamo v hišah. Avtor: Manfred Antranias Zimmer. Vir: Pixabay. Ker pa CHO3Nh3BDP3 Lahko se pokvari z deževnico, proučeno je bilo, kako onesnaževanje teh celic je lahko tako, ko so v uporabi in ko jih zavržejo.
Pogl3Nh3BDP3 Po stiku z vodo se vdre v metilamin (izberite3Nh2), Jodhidrična kislina in BDP2. Slednje, čeprav je v vodi malo topno, lahko sčasoma sprosti količine iz strupenega iona PB2+.
Študije niso prepričljive, ker kraj, kjer se sproščanje svinca pojavi, da ugotovi, ali je znesek lahko kratkoročno škodljiv. Po drugi strani pa lahko nadaljevanje sproščanja bioakumulira in je zelo nevarna.
Vam lahko služi: butanone: struktura, lastnosti in uporabeDruge aplikacije
- Posejano je v obliki razpršila v oblakih, da proizvede dež.
- V filtrih za astronomijo oddaljenega infrardečega.
- V fotografiji, vtisi, filmi za snemanje optičnih slik, fotografske emulzije.
- V zavornem premazu. Pri mazanju maščob.
- Živosrenske parni lok svetilke. Na elektrotičnem papirju.
- Termoelektrični materiali, toplotne baterije z jodom.
Tveganja
Za varnost
Shranjujejo ga daleč od oksidantov, kot so peroksidi, peroksidi, permanganate, klorize in nitrati. Izogibati se je treba tudi stik s kemično aktivnimi kovinami, kot so kalij, natrij, magnezij in cink. V vseh teh primerih se lahko pojavi nasilna reakcija.
Če se ogrejete, se ustvarijo strupeni plini svinca in joda.
Do zdravja
Je zelo škodljiv za človeka. Potrjeno je, da je karcinogen za živali, zato je razumno ugotovljeno, da je tudi za človeka.
Lahko povzroči glavobol, razdražljivost, zmanjša spomin in moti spanje. Svinca, ki jo vsebuje to spojino, lahko povzroči trajne poškodbe ledvic, možganov, živcev, krvnih celic in visokega tlaka.
Ravnati z njim kot teratogen (spojina, ki lahko ustvari prirojeno napako). Lahko ustvari tudi jodam, katere simptomi so zastoji nosnic, glavobola, draženje sluznic in kožni izbruh.
Za naravno okolje
Uvrščena je med strupeno onesnaževanje. Hraniti ga je treba stran od voda in odtok virov. Da se izognete kontaminirajočim nasiljem, je treba zgraditi, kadar koli je potrebno zadržati.
Za vodno življenje je zelo strupeno z učinki, ki trajajo sčasoma, saj je bioakumulabilna.
Reference
- Svinec, d.R. (Urednik) (2003). Priročnik za kemijo in fiziko CRC. 85th CRC Press.
- Ali.S. Nacionalna knjižnica medicine. (2019). Svinčeno jodid. Okrevano od PubChema.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Bombaž, f. Albert in Wilkinson, Geoffrey. (1980). Napredna anorganska kemija. Četrta izdaja. John Wiley & Sons.
- Evstropiev; S.K. et al. (2020). Sinteza in karakterizacija PVP/PBI2. Adv Compos Hybrid Mater 3, 49–57 (2020). Povezava je bila obnovljena.Springer.com.
- Ismail, r.Do. et al. (2016). Sinteza PBI2 Nanodelci z lasersko ablacijo v metanolu. J Mater Sci: Mater Electron 27, 10696-10700 (2016). Povezava je bila obnovljena.Springer.com.
- Materiali. (2013). Svinčeno jodid (BDP2) Polprevodnik. Okreval iz Azoma.com.
- CDH (2008). Svinec (ii) jodid. Gradivo za varnostni podatki. Okrevano od chdfinehemičnega.com.
- Hailegnaw, b. et al. (2015). Dež na metilamonijevi perovskiti na osnovi jodida: Možni okoljski učinki sončnih celic Perovskita. J. Phys. Kem. Lett. 2015, 6, 9, 1543-1547. Okrevani iz lokalov.Acs.org.
- Fundacija Wikimedia (2020). Svinec (ii) jodid. Pridobljeno iz.Wikipedija.org.
- « Svinčeno strukturo acetata, lastnosti, pridobivanje, uporabe
- Organizacija objektivnega podjetja, struktura, primer »

