Arzen trioksid (AS2O3)
- 1489
- 130
- Stuart Armstrong
On Arzen trioksid To je anorganska spojina, katere kemijska formula je tako2Tudi3. Arzen v njegovem kovinskem stanju se hitro spremeni v ta oksid, ki je zelo strupen strup, ki ima lahko akutne in kronične manifestacije.
Ker je arzen in kisikovni elementi bloka P, z relativno nizko razliko v elektronegativnosti, se pričakuje ACE2Tudi3 sestavljen iz kovalentne narave; to pomeni, da vezi AS-O prevladujejo v svoji trdni trdni snovi, na elektrostatičnih interakcijah med asnimi ioni3+ jaz2-.
Akutna zastrupitev z arzenskim trioksidom nastane z vnosom ali vdihavanjem, kar je najpomembnejše manifestacije tega: močne prebavne motnje, krči, krvni propad in pljučni edem.
Kljub svoji strupenosti pa se uporablja industrijsko; Na primer pri ohranjanju lesa, v izdelavi pigmentov, polprevodnikov itd. Prav tako je bil prej uporabljen pri zdravljenju številnih bolezni.
Arzenski trioksid je amfoterična spojina, topna v kislinah in razredčena alkalija, netopna v organskih topilih in sorazmerno topna v vodi. Predstavljen je kot trdna (nadrejena slika), z dvema kristalnima oblikama: kubični in monoklinični.
Arzenska struktura trioksida
Claudeteta
Pri sobni temperaturi as2Tudi3 Kristalizira v dveh monokliničnih polimorfoh, oba najdena v mineralu Claudetita. V njih so trigonalne piramidne enote ASO3, ki se vežejo s svojimi kisikovimi atomi, da kompenzirajo elektronsko pomanjkanje enote.
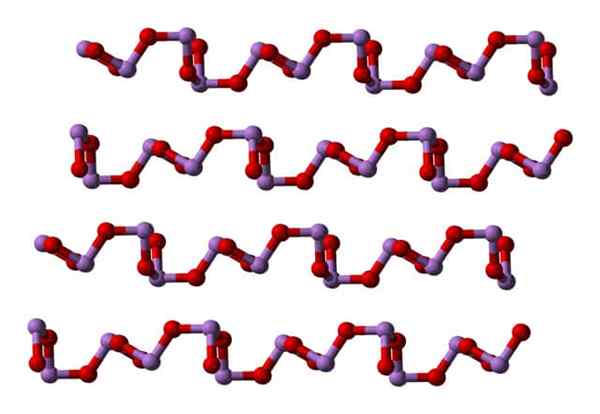
V polimorfu so enote ASO3 Povezane so vrstice (Claudeteta I), v drugem pa so povezane, kot da bi tkali mrežo (Claudeteta II):
Vam lahko služi: aglomerant materiali Claudetita Polymorfo Struktura i. Vir: Ben Mills [javna domena].
Claudetita Polymorfo Struktura i. Vir: Ben Mills [javna domena].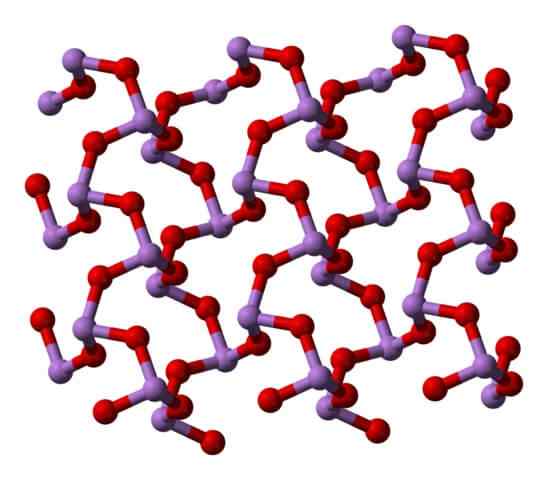 Claudeteta Polymorfo Struktura II. Vir: Ben Mills [javna domena].
Claudeteta Polymorfo Struktura II. Vir: Ben Mills [javna domena].
Tekočina in plinasta
Ko se vse tiste strukture, ki definirajo monoklinične kristale, segrejejo, so vibracije takšne, da je pokvarjeno več povezav AS-O in na koncu prevladuje manjša molekula:4Tudi6. Na spodnji sliki je prikazana njegova struktura.
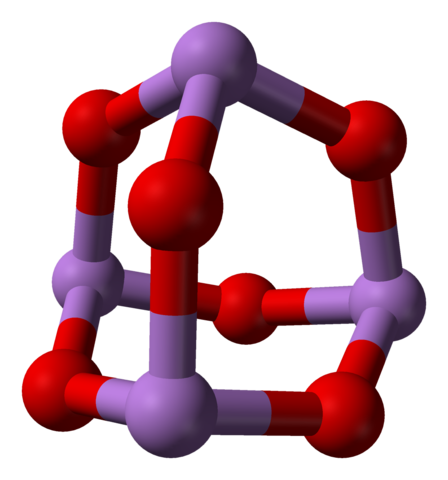 Molekula AS4O6. Vir: Ben Mills [javna domena]
Molekula AS4O6. Vir: Ben Mills [javna domena] Lahko bi rekli, da je sestavljen iz dneva2Tudi3. Njegova stabilnost je taka, da podpira 800 ° C v plinski fazi; Toda nad to temperaturo je razdrobljena kot molekule2Tudi3.
Arsenolit
Enako kot4Tudi6 lahko medsebojno komunicirajo, da se kristalizirajo v kubični trdni snovi, katere strukturo najdemo v mineralu arsenolita.
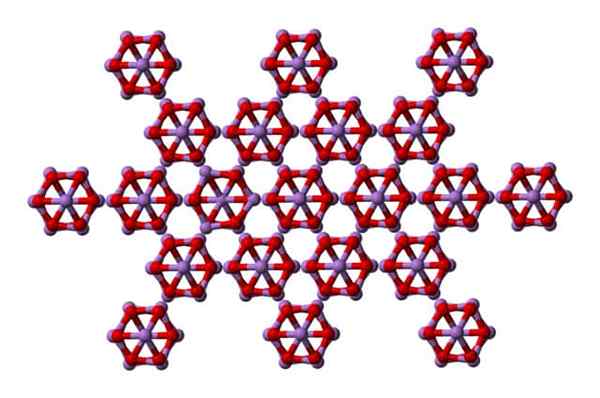 Molekule AS4O6 v arzenolitu. Vir: Ben Mills [javna domena]
Molekule AS4O6 v arzenolitu. Vir: Ben Mills [javna domena] Upoštevajte, da je na sliki struktura prikazana iz višje ravnine. V primerjavi s Claudetito je očitna njegova strukturna razlika z arsenolitom. Tu so diskretne molekule4Tudi6 da enote vzdržujejo sile Van der Waals.
Lastnosti
TradeNames
-Arsenolit
-Arsodent
-Trisenox
-Claudeteta
Molekularna teža
197,84 g/mol.
Fizični videz
-Beli kubični kristali (arsenolit).
-Monoklinski brezbarvni kristali (Claudeteta).
-Beli ali prozoren trdni, steklovi, amorfni grudice ali kristalni prah.
Vonj
Stranišče.
Okus
Brez okusa.
Vrelišče
460 ° C.
Tališče
-313 ° C (Claudeteta).
-274 ° C (arsenolit).
točka vžiga
485 ° C (sublima).
Topnost vode
17 G/L A 18 ° C (20 g/L A 25 ° C).
Topnost
Kislinsko topno (zlasti v klorovodiki) in alkaliji. Praktično netopni v kloroformu in etru.
Vam lahko služi: centrifugiranjeGostota
-3,85 g/cm3 (kubični kristali);
-4,15 g/cm3 (Rombični kristali).
Parni tlak
2,47 · 10-4 mmhg pri 25 ° C.
Razgradnja
Ni gorivo, vendar lahko zaradi segrevanja povzroči strupen dim, ki lahko vključuje Arsino.
Jedkost
V prisotnosti vlage je lahko jedko za kovine.
Toplota za uparjanje
77 kJ/mol.
Konstanta disociacije (ka)
1.1 · 10-4 pri 25 ° C.
Lomni količnik
-1.755 (arsenolit)
-1.92-2.01 (Claudeteta).
Reaktivnost
-Arzen trioksid je amfoterična spojina, vendar deluje po možnosti kot kislina.
-Reagira lahko s klorovodikovo kislino ali s fluorhorično kislino, ki tvori arzenski triflourid ali arzenski triflourur.
-Reagira tudi z močnimi oksidanti, kot je dušikova kislina, kar povzroča arzenovo kislino in dušikovo oksid.
-Arzenski trioksid lahko reagira z dušikovo kislino in proizvaja arzin ali arzen element, odvisno od reakcijskih pogojev.
As2Tudi3 + 6 Zn +12 hno3 => 2 ASH3 + 6 Zn (št3)2 + 3 h2Tudi.
Ta reakcija je služila kot osnova za ustvarjanje telesnega testa, ki se uporablja za odkrivanje zastrupitve z arzenom.
Nomenklatura
Ob2Tudi3 Lahko se imenuje v skladu z naslednjimi nomenklaturami, saj ve, da Arsen deluje z Valencijo +3:
-Arsenioso oksid (tradicionalna nomenklatura).
-Arzenski oksid (III) (nomenklatura zalog).
-Dirsenski trioksid (sistematična nomenklatura).
Prijave
Industrijalisti
-Uporablja se pri izdelavi stekla, zlasti kot bledi sredstvo. Uporablja se tudi pri izdelavi keramike, elektronskih izdelkov in ognjemetov.
-Dodamo ga kot manjša komponenta zlitin na osnovi bakra, da se poveča korozijska odpornost kovin zlitin.
-As2Tudi3 To je začetno gradivo za pripravo osnovnega arzena, za izboljšanje električnih sklepov in za izdelavo polprevodnikov Arsenuros
Lahko vam služi: jedrska kemija: zgodovina, področje študija, območja, aplikacije-As2Tudi3, Kot tudi bakreni arseniato se uporabljajo kot leseni konzervansi. Uporabljali so ga v kombinaciji z bakrenim acetatom za izdelavo zelenega pigmenta Pariza, ki se uporablja pri izdelavi slik in raticidov.
Zdravniki
-Arzenski trioksid je spojina, ki se že stoletja uporablja pri zdravljenju številnih bolezni. Uporabljali so ga kot tonik pri zdravljenju prehranskih motenj, nevralgije, revmatizma, artritisa, astme, Koreje, malarije, sifilisa in tuberkuloze.
-Prav tako se uporablja pri lokalnem zdravljenju kožnih bolezni, ki se uporablja za uničenje nekaterih površinskih epiteliomov.
-Fowlerjeva rešitev je bila uporabljena pri zdravljenju kožnih bolezni in levkemije. Uporaba tega zdravila je ukinjena.
-V 70. letih prejšnjega stoletja je kitajski raziskovalec Zhang Tingdong razvil preiskavo o uporabi arzenskega trioksida pri zdravljenju akutne promielocitne levkemije (APL). Kar je privedlo do proizvodnje zdravila Trisenox, ki ga je odobrila ameriška FDA.
-Trisenox je bil uporabljen pri bolnikih s PLA, ki se ne odzivajo na zdravljenje "prve vrstice", ki je sestavljena iz vse trans kisle kisline (Attric). Dokazano je, da arzenski trioksid povzroči rakave celice, da trpijo apoptozo.
-Trisenox se uporablja kot citostatična pri zdravljenju ognjevzdržne promiselocitne podtipe (m3) aplikacije.
Reference
- Arzen trioksid. Sevier. Pridobljeno iz: SCINCEDIRECT.com
- Arzen (iii) oksid. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov

