Značilnosti, funkcije, presnove, hrana
- 895
- 198
- Ms. Pablo Lebsack
The Serin Je ena od 22 osnovnih aminokislin, čeprav to ni razvrščeno kot bistvena aminokislina za človeka in druge živali, saj ga sintetizira človeško telo.
Glede na treh nomenklaturo je serin v literaturi opisan kot (S v kodi z eno črko). Ta aminokislina sodeluje v velikem številu presnovnih poti in ima polarne značilnosti, vendar nima obremenitve na nevtralni pH.
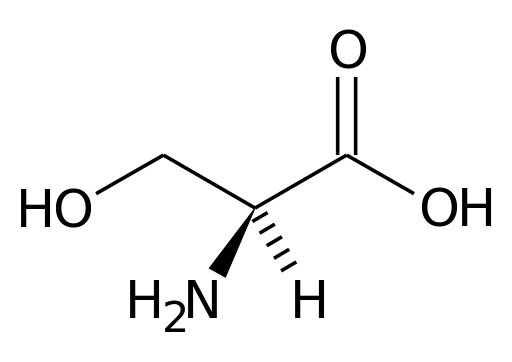
 Predstavitev serije serinske aminokisline (vir: Pagezero na njej.Wikipedia [javna domena] prek Wikimedia Commons)
Predstavitev serije serinske aminokisline (vir: Pagezero na njej.Wikipedia [javna domena] prek Wikimedia Commons) Številni pomembni encimi za celice imajo veliko.
Serin med številnimi njegovimi funkcijami sodeluje kot predhodnika in odrov v biosintezi drugih aminokislin, kot sta glicin in cistein, in je del strukture sfingolipidov, prisotnih v celičnih membranah v celičnih membranah.
Hitrost sinteze serina se razlikuje v vsakem organu, poleg tega pa se spreminja glede na stopnjo razvoja, v kateri je posameznik.
Znanstveniki so predlagali, da se koncentracije L-serina v možganskem tkivu s starostjo povečujejo, saj se prepustnost krvne celične pregrade zmanjšuje v možganih odraslih, saj lahko povzroči hude možganske motnje.
Znano je, da je L-serin ključnega pomena za biosintezo nevrotransmiterjev, fosfolipidov in drugih zapletenih makromolekul.
Različne študije so pokazale, da dobava dodatkov ali koncentratov L-serina za nekatere vrste bolnikov izboljšuje homeostazo glukoze, mitohondrijsko delovanje in zmanjšuje smrt nevronov.
[TOC]
Značilnosti in struktura
Vse aminokisline imajo kot osnovno strukturo karboksilno skupino in amino skupino, pritrjeno na isti ogljikov atom; Vendar se med seboj razlikujejo po svojih stranskih verigah, znane kot R skupine, ki se lahko razlikujejo po njihovi velikosti, strukturi in celo v električnem naboju
Serin vsebuje tri atome ogljika: Združeni centralni ogljik, na eni strani, v karboksilno skupino (COOH) in na drugi, amino skupino (NH3+). Drugi dve centralni ogljikovi vezi zasedata vodikov atom in skupina CH2OH (skupina R), značilna za serin.
Osrednji ogljik, na katerega so amino in karboksilne skupine aminokislin znani kot α ogljik. Drugi ogljikovi atomi R skupinah so označeni s črkami grške abecede.
V primeru serina je na primer edini atom ogljika v svoji skupini R, ki je povezan s skupino OH, znan kot ogljik γ.
Vam lahko služi: fosfatidilserin: struktura, sinteza, funkcije, lokacijaKlasifikacija
Serin je razvrščen v skupino polarnih aminokislin brez obremenitve. Člani te skupine so zelo topne aminokisline v vodi, torej so hidrofilne spojine. V serinu in treoninu je hidrofilnost posledica njegove sposobnosti oblikovanja vodikovih mostov z vodo prek hidroksilnih skupin (OH).
Znotraj skupine polarnih aminokislin brez obremenitve so cistein, asparagin in glutamin združeni tudi skupaj. Vsi ti imajo polarno skupino v svoji R verigi, vendar ta skupina ni ionizabilna in pH blizu nevtralnosti prekličejo svoje stroške, ki povzročajo spojino v obliki "Zwitterion".
Stereokemija
Splošna asimetrija aminokislin naredi stereokemijo teh spojin bistvenega pomena na presnovnih poteh, v katerih sodelujejo. V primeru serina lahko to najdemo kot d-o l-serin, slednji pa so sintetizirane izključno celice živčnega sistema, znane kot astrociti.
Α ogljikovi aminokislini so kiralni ogljiki, saj imajo štiri različne združene substituente, kar ustvarja, da obstajata vsaj dva različna stereoizomera za vsako aminokislino.
Stereoizomer je zrcalna podoba molekule, to pomeni, da se na drugi ne morete prekrivati. Raztopine teh aminokislin vrtijo polarizirano svetlobno ravnino v nasprotnih smereh v nasprotnih smereh, ki so označene s črko d o, ki eksperimentalno.
L-serin, ki se sintetizira v živčnih celicah, služi kot substrat za sintetizacijo glicina ali D-serina. D-serin je eden najpomembnejših elementov za izmenjavo veziklov med nevroni, zato nekateri avtorji predlagajo, da sta obe serinski izoformi v resnici bistvene aminokisline za nevrone za nevrone.
Funkcije
OH skupina serina v svoji R verigi R je dober nukleofil, zato je ključna za aktivnost številnih encimov s serinom na svojih aktivnih mestih. Serin je eden od potrebnih substratov za sintezo NADPH in glutationske nukleotide.
L-serija je nepogrešljiva za razvoj in pravilno delovanje centralnega živčnega sistema. Študije so pokazale, da eksogena oskrba L-serina v nizkih odmerkih nevronom hipokampusa in celic Purkinje In vitro, Izboljša vaše preživetje.
Več raziskav rakavih celic in limfocitov je ugotovilo, da so ogljikove enote, odvisne od serina.
Vam lahko služi: mikrobiota: sestava, funkcije in kje jeSelenocistein je del 22 osnovnih aminokislin in ga dobimo le kot derivat serina. To aminokislino smo opazili le pri nekaterih beljakovinah, vsebuje selen namesto žvepla, pritrjenega na cistein in je sintetiziran na podlagi sterificiranega serina.
Biosinteza
Serin je neobčutljiva aminokislina, saj ga sintetizira človeško telo. Vendar je to mogoče asimilirati iz prehrane različnih virov, kot so beljakovine in fosfolipidi, predvsem.
Serin se sintetizira v njegovi obliki s pretvorbo glicinske molekule, reakcije, ki jo posreduje encim hidroksimetil-transferaze.
Znano je, da je glavno mesto sinteze L-serina v astrocitih in ne v nevronih. Prav te celice se sinteza pojavlja s fosforilacijo, v kateri sodeluje 3-fosfoglicerat, glikolitični posrednik.
Na tej poti delujejo trije encimi: 3-fosfoglicerat dehidrogenaza, fosfoserin-transferaza in fosfoserina-fosfataza.
Drugi pomembni organi glede sinteze serin so jetra, ledvice, testisi in vranica. Encimi, ki sintetizirajo serin.
Ena prvih sinteznih poti serina, ki je bila znana, je bila katabolična pot, ki je vključena v glukoneogenezo, kjer se L-serin dobiva kot sekundarni presnovek. Vendar je prispevek te poti k proizvodnji telesa serin.
Metabolizem
Trenutno je znano, da lahko serin pridobimo iz presnove ogljikovih hidratov v jetrih, kjer se proizvaja D-glicerična kislina, 3-fosfoglijeva kislina in 3-fosfohidroksipirúvična kislina. Zahvaljujoč postopku transaminacije med 3-hidroksi piruvično kislino in alanin nastane serin.
Poskusi s podganami, ki radioaktivno označujejo ogljik 4 glukoze, so ugotovili, da je ta ogljik učinkovito vgrajen v ogljikove okostja serina, kar kaže na to, da ima omenjena aminokislina predhodnik treh ogljikov, verjetno iz piruvata.
V bakterijah je encim L-serin-dezaminaze glavni encim, ki je zadolžen za presnovo serina: L-serin pretvori v piruvat. Znano je, da je ta encim prisoten in aktiven v pridelkih In. coli Dodelitev v minimalnih medijih z glukozo.
Zagotovo ni znano, kakšna je resnična funkcija L-serin-dezaminaze v teh mikroorganizmi drugi, zato sledi, da mora imeti pomembne fiziološke posledice.
Vam lahko postreže: Dryopithecus: odkritje, značilnosti, lobanja, hranaSerinsko bogato hrano
Vsa živila z visoko koncentracijo beljakovin je bogata z serinom, predvsem jajci, mesom in ribami. Vendar je to nepomembna aminokislina, zato ga ni treba zaužiti glede na dejstvo, da ga telo lahko sintetizira samo po sebi.
Nekateri ljudje trpijo zaradi nenavadne motnje, saj imajo fenotip pomanjkanja glede na mehanizme sinteze serina in glicina, zato morajo zaužiti koncentrirane prehrambene dodatke za obe aminokislini.
Poleg tega komercialne blagovne znamke, specializirane za prodajo vitaminskih dodatkov (Lamberts, zdaj Sport in Holomega), ponujajo fosfatidilserina in koncentrate L-serin, da povečajo proizvodnjo mišične mase pri visokih konkurenčnih športnikih in dvigovanju uteži.
Sorodne bolezni
Napaka encimov, vključenih v biosintezo serina, lahko povzroči resne patologije. Z zmanjšanjem koncentracije serina v krvni plazmi in cerebrospinalni tekočini lahko povzroči hipertonijo, psihomotorno zamudo, mikrocefalijo, epilepsijo in zapletene motnje centralnega živčnega sistema.
Trenutno je bilo ugotovljeno, da je pomanjkanje serina vključeno v razvoj diabetesa mellitusa, saj je L-serin potreben za sintezo insulina in njene receptorje.
Dojenčki, ki predstavljajo okvare v biosintezi serine, so ob rojstvu nevrološko nenormalne, zamude pri rasti intrauterine, prirojene mikrocefalije, katarakte, napadov in hude zamude pri nevrološkem razvoju.
Reference
- Elsila, J. In., Dworkin, J. Str., Bernstein, m. Str., Martin, m. Str., & Sandford, s. Do. (2007). Mehanizmi tvorbe aminokislin v medzvezdnih analogih ledu. Astrophysical Journal, 660 (1), 911.
- Ichord, r. N., & Bearden, D. R. (2017). Perinatalne presnovne encefalopatije. V Swaimanovi pediatrični nevrologiji (pp. 171-177). Elsevier.
- Mothet, J. Str., Starš, a. T., Wolosker, h., Brady, r. Tudi., Linden, d. J., Ferris, c. D.,… & Snyder, s. H. (2000). D-serin je endogeni ligand za glicin mesto N-metil-D-apartatnega sprejemnika. Zbornik Nacionalne akademije znanosti, 97 (9), 4926-4931
- Nelson, d. L., Lehninger, a. L., & Cox, m. M. (2008). Lehningerjeva načela biokemije. Macmillan.
- Rodríguez, a. In., Ducker, g. S., Billingham, l. K., Martinez, c. Do., Mainolfi, n., Suri, v.,… & Chandel, n. S. (2019). Serinski presnova podpira proizvodnjo makrofaga IL-1β. Metabolizem celic, 29 (4), 1003-1011.
- Tabatabaie, l., Klomp, l. W., Berger, r., & Koning, t. J. (2010). Sinteza L-serina v centralnem živčnem sistemu: pregled motenj pomanjkanja serina. Molekularna genetika in presnova, 99 (3), 256-262.
- « Struktura gliceraldehida, značilnosti, funkcije
- Zgodovina cinka, lastnosti, struktura, tveganja, uporabe »

