Struktura magnezijevega nitrata (mg (NO3) 2), lastnosti, uporabe

- 3420
- 788
- Ms. Pablo Lebsack
On Magnezijev nitrat Je anorganska trdna snov, katere kemična formula je Mg (ne3)2. Gre za ionsko spojino, ki jo tvori zveza mag magnezijevega2+ in dva nitratna aniona št3-.
MG (št3)2 Je kristalno bela trdna snov. Je zelo higroskopsko, to je, da zlahka absorbira vodo iz okolja. S tem, ko ostane v stiku z zrakom okolja, ponavadi tvori svoj mg heksahidrat (ne3)2 •6H2Tudi.
 Mg magnezijev nitrat (št3)2 v prahu. Ondřej mangl [javna domena]. Vir: Wikimedia Commons.
Mg magnezijev nitrat (št3)2 v prahu. Ondřej mangl [javna domena]. Vir: Wikimedia Commons. Mag nitrate heksahidrat (ne3)2 •6H2O ima v svoji kristalni strukturi 6 molekul vode h2Ali za vsako mg molekulo (ne3)2. Magnezijev nitrat najdemo v kavernah in minah v obliki nitromagnezita minerala.
MG (št3)2 Dobimo ga komercialno z reakcijo kovinske kovine mg z dušikovo kislino hno3.
Ima zelo raznolike namene, kot je kmetijstvo kot gnojilo, ker zagotavlja hranljive elemente za rastline, kot sta dušik (N) in magnezij (MG).
Uporablja se v ognjemetni industriji ali pirotehniki in tudi pri pridobivanju koncentrirane dušikove kisline. Uporablja se v kemijski analizi, v fizikalnih poskusih ter medicinskih in znanstvenih študijah.
[TOC]
Struktura
Anhidro magnezijev nitrat tvori magnezio mg kation2+ in dva nitratna aniona št3-.
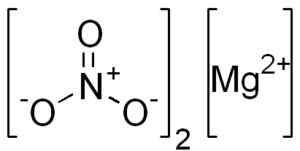 Mg struktura (št3)2. Edgar181 [javna domena]. Vir: Wikimedia Commons.
Mg struktura (št3)2. Edgar181 [javna domena]. Vir: Wikimedia Commons. Magnesio mg ion2+ Ima elektronsko konfiguracijo: 1s2, 2s2 2 p6, 3s0, No, dva elektrona najbolj oddaljene plasti (3s) sta. Ta konformacija je zelo stabilna.
Ion št3- Ima ravno in simetrično strukturo.
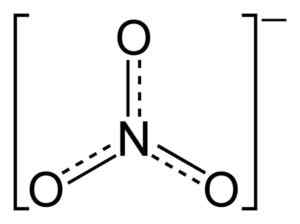 Ravna nitratna ionska struktura št3-. Pikčaste črte označujejo pravično porazdelitev elektronov med tremi N-O vezi. Benjah-BMM27 [javna domena]. Vir: Wikimedia Commons.
Ravna nitratna ionska struktura št3-. Pikčaste črte označujejo pravično porazdelitev elektronov med tremi N-O vezi. Benjah-BMM27 [javna domena]. Vir: Wikimedia Commons. V strukturi št3- Negativna obremenitev se neprestano porazdeli med tremi atomi kisika.
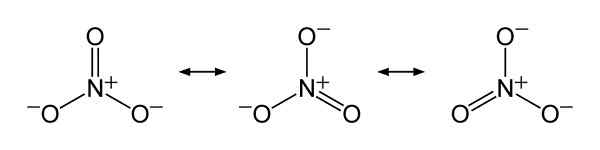 Nitratne ionske resonančne strukture št3-, Razložiti pravično porazdelitev negativne obremenitve med tremi atomi kisika. Benjah-BMM27 [javna domena]. Vir: Wikimedia Commons.
Nitratne ionske resonančne strukture št3-, Razložiti pravično porazdelitev negativne obremenitve med tremi atomi kisika. Benjah-BMM27 [javna domena]. Vir: Wikimedia Commons. Nomenklatura
-Anhidro magnezijev nitrat: mg (ne3)2
Vam lahko služi: destilirana voda-Dihidrirani magnezijev nitrat: Mg (št3)2 •2H2Tudi
-Heksahidratni magnezijev nitrat: mg (ne3)2 •6H2Tudi
-Magnezijev dinitrat
Lastnosti
Fizično stanje
-Mg (št3)2 Brezvodni: beli trdni, kubični kristali.
-Mg (št3)2 Dihidrado: kristalno bela trdna snov.
-Mg (št3)2 Šesterokotni: brezbarvni trdni, monoklinski kristali
Molekularna teža
-Mg (št3)2 Brezvodna: 148,31 g/mol
-Mg (št3)2 Heksahidrat: 256,41 g/mol
Tališče
-Mg (št3)2 Heksahidrat: 88,9 ° C
Vrelišče
-Mg (št3)2 Heksahidrat: Ne vrejte, razgradite pri 330 ° C
Gostota
-Mg (št3)2 Brezvodna: 2,32 g/cm3
-Mg (št3)2 Dihidrardeni: 1.456 g/cm3
-Mg (št3)2 Heksahidrat: 1.464 g/cm3
Topnost
Anhidro magnezijev nitrat je zelo topen v vodi: 62,1 g/100 ml pri 0 ° C; 69,5 g/100 ml pri 20 ° C. Prav tako je zelo higroskopsko, v stiku z zrakom hitro tvori heksahidrat.
MG (št3)2 Dihydrado je tudi zelo topen v vodi in etanolu. Je higroskopska.
MG (št3)2 Heksahidrat je tudi zelo topen v vodi. V etanolu je zmerno topen. Je najbolj stabilna od treh v stiku z zrakom, torej od treh je tisti, ki najmanj absorbira vodo iz okolja.
Učinek grelnega ogrevanja
S predložitvijo vodne raztopine mg (št3)2 Za izhlapevanje vode je sol, ki kristalizira, heksahidrat: mg (ne3)2 •6H2Tudi. Heksahidrat pomeni, da v trdni snovi vsaka molekula Mg (ne3)2 Povezana je s 6 molekulami vode.
Obstaja tudi mg dihidrat (ne3)2 •2H2Ali, v katerem je mg (ne3)2 trdna snov je pritrjena na 2 molekuli vode.
Ogrevanje mg heksahidrata (ne3)2 •6H2Ali pa anhidra soli ne dobimo, ker ima magnezijev nitrat visoko afiniteto do vode.
Zaradi tega je s segrevanjem nad njeno tališče mešano nitratno sol in magnezijev hidroksid MG (ne3)2 •4mg (OH)2.
Ta mešana sol, ko doseže 400 ° C, se razgradi na magnezijev oksid in odstrani pline dušikove okside.
Lahko vam služi: kalcijev hipoklorit (CA (CLO) 2)Pridobivanje
Pripravimo ga z reakcijo mgco magnezijev karbonat3 Z dušikovo kislino hno3, odpoved ogljikovem dioksidu Co2:
MGCO3 + 2 hno3 → mg (št3)2 + Co2↑ + h2Tudi
Dobimo ga lahko tudi z Mg (OH) magnezijevim hidroksidom2 in dušikova kislina:
MG (OH)2 + 2 hno3 → mg (št3)2 + 2 h2Tudi
Komercialno pridobljeno na več načinov:
1- reagiranje magnesio mg z dušikovo kislino hno3.
2- Z reakcijo MgO magnezijevega oksida z dušikovo kislino HNO3.
3- Pridružitev MG (OH) magnezijev hidroksid2 in NH amonijev nitrat4Ne3, Oblikovanje magnezijevega nitrata z odvajanjem NH amoniaka3.
Lokacija v naravi
MG (št3)2 Heksahidrat seveda najdemo v rudnikih in jamah ali kavernah v obliki minerala nitromagnezita.
Ta mineral je prisoten, ko Guano pride v stik z bogatimi skalami v magneziju. Guano je material, ki je posledica iztrebkov morskih ptic in tjulnjev v zelo suhih okoljih.
Prijave
MG (št3)2 Heksahidrat se uporablja v industriji keramike, kemije in kmetijstva.
Ta spojina je gnojilo, ker zagotavlja dušik (n), ki je eden od treh osnovnih elementov, ki jih potrebujejo rastline, in magnezij (MG), ki je tudi sekundarna komponenta, pomembna tudi za to.
Na ta način se uporablja z drugimi sestavinami v rastlinjakih in v hidroponski kulturi. Slednje je, da rastline gojijo v vodni raztopini s soli z gnojili namesto v zemljo.
 Hidroponska kultura. Ogledate si lahko kanale, skozi katere vodna raztopina s soli gnojil, kot je mg magnezijev nitratni kroženje (ne3)2. Avtor: Marsraw. Vir: Pixabay.
Hidroponska kultura. Ogledate si lahko kanale, skozi katere vodna raztopina s soli gnojil, kot je mg magnezijev nitratni kroženje (ne3)2. Avtor: Marsraw. Vir: Pixabay. Uporablja se tudi kot katalizator pri pridobivanju petrokemičnih spojin. Omogoča prilagajanje viskoznosti v določenih procesih. Anhidro magnezijev nitrat se uporablja v pirotehniki, torej za proizvodnjo ognjemetov.
 Ognjemet vsebuje mg magnezijev nitrat (ne3)2. Avtor: brezplačni goos. Vir: Pixabay.
Ognjemet vsebuje mg magnezijev nitrat (ne3)2. Avtor: brezplačni goos. Vir: Pixabay. Anhidro magnezijev nitrat je dehidrirajoč. Uporablja se na primer za pridobivanje koncentrirane dušikove kisline, saj odpravlja vodo in koncentrira kisline do 90-95% HNOS3.
Vam lahko služi: diagonalno pravilo Koncentrirana dušikova kislina. Originalni nalagalec je bil Fabexposive na italijanski Wikipediji. [GFDL (http: // www.GNU.Org/copyleft/fdl.html)]. Vir: Wikimedia Commons.
Koncentrirana dušikova kislina. Originalni nalagalec je bil Fabexposive na italijanski Wikipediji. [GFDL (http: // www.GNU.Org/copyleft/fdl.html)]. Vir: Wikimedia Commons. Uporablja se tudi za pokrivanje amonijevega nitrata in omogoča nastanek biserov omenjenega stisnjenega materiala.
Ima uporabnost v formulaciji črnila, tonerju (črni prah, ki se uporablja v fotokopiranih sistemih) in izdelkih za barvanje. Služi kot magnezijev standard v analitični kemiji.
Magnezij in cerio mg nitratna sol (ne3)2 •Mrzlo3)3 Zanimiv je za fizične poskuse pri nizkih temperaturah, saj se uporablja kot hladilno sredstvo v adiabatskih poskusih sumagnetizacije (brez prenosa toplote).
Ta magnezij in cerio sol sta bila uporabljena za vzpostavitev izjemno nizkih temperatur ravni Kelvinove lestvice (blizu absolutne ničle).
V zadnjih študijah
Več raziskovalcev je uporabilo MG (št3)2 V sestavah s sintetičnimi in naravnimi polimeri za povečanje prevodnosti v magnezijskih baterijah.
Raziskali so ga tudi pri gradnji supercaugade za shranjevanje energije z visoko močjo.
V študijah bolezni
Magnezijevi nitrat se daje laboratorijskim podganam z arterijsko hipertenzijo (visok tlak) in ugotovljeno je bilo, da krvni tlak učinkovito zniža in zmanjša ali ublaži učinke zapletov te bolezni.
Prav tako je pokazal zaščitne učinke proti nevrološkim motnjam (motnje pri nevronih) in proti smrti pri podganah med procesi kaktonidov karotidne arterije.
Reference
- Qian, m. et al. (2018). Izvlečni porozni nekaj plastnih ogljikih z visoko kapacitivnostjo iz pehinija zgorevanja magnezijevega nitratnega gela. ACS Appl Mater Interfaces 2018, 10 (1): 381-388. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Manjuladevi, r. et al. (2018). Študija o mešanem polimernem elektrolitu, ki temelji na Poly. Ionics (2018) 24: 3493. Povezava je bila obnovljena.Springer.com.
- Kiruthika, s. et al. (2019). Okolju prijazen biopolimerni elektrolit, pektin z magnezijevo nitratno soljo, za uporabo v elektrokemičnih napravah. J Solid State Elcochem (2019) 23: 2181. Povezava je bila obnovljena.Springer.com.
- Vilskerts r. et al. (2014). Magnezijev nitrat zmanjšuje zvišanje krvnega tlaka pri podganah SHR. Magnes Res 2014, 27 (1): 16-24. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Kuzenkov v.S. in Krushinskii a.L. (2014). Zaščitni učinek magnezijevega nitrata proti nevrološkim motnjam, ki jih izzove cerebralna ishemija pri podganah. Bull Exp Biol Med 2014, 157 (6): 721-3. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Ropp, r.C. (2013). Skupina 15 (n, p, as, sb in bi) alkalne zemeljske spojine. Magnezijev nitrat. V enciklopediji alkalnih zemeljskih spojin. Okrevano od Scientirect.com.
- Kirk-Othmer (1994). Enciklopedija kemijske tehnologije. Zvezek 1. Četrta izdaja. John Wiley & Sons.
- Ali.S. Nacionalna knjižnica medicine. (2019). Magnezijev nitrat. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- « Koncept in značilnosti tehničnega sistema, elementi, primeri
- Masovna številka, iz česa je sestavljena in kako ga dobiti (s primeri) »

