Hidroksidi
- 3849
- 423
- Barry Ernser
Kaj so hidroksidi?
The Hidroksidi So anorganske in trinalne spojine, ki so sestavljene iz interakcije med kovinskim kationom in funkcionalno skupino OH (hidroksid Anion, OH-). Večina jih je ionske narave, čeprav imajo lahko tudi kovalentne vezi.
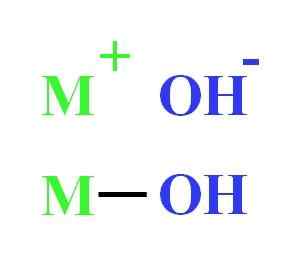
Na primer, hidroksid je lahko predstavljen kot elektrostatična interakcija med kationom M+ in anion oh-, ali kot kovalentna zveza prek povezave M-OH (spodnja slika). V prvem je dana jonska vez, v drugem. To dejstvo je v bistvu odvisno od kovine ali citacije+, kot tudi njegov radio obremenitev in ionski radio.
 Predstavitev hidroksida. Vir: Gabriel Bolívar
Predstavitev hidroksida. Vir: Gabriel Bolívar Ker jih večina prihaja iz kovin, jih je enakovredno omeniti kot kovinski hidroksidi.
Kako nastanejo hidroksidi?
Obstajata dve glavni sintetični poti: z reakcijo ustreznega oksida z vodo ali z močno podlago v kislem mediju:
Mo + h2O => m (oh)2
Mo + h+ + Oh- => M (OH)2
Samo tisti vodni topni kovinski oksidi reagirajo neposredno, da tvorijo hidroksid (prva kemična enačba). Drugi so netopni in potrebujejo kislinske vrste, ki sproščajo m+, ki nato komunicira z OH- iz močnih baz (druga kemijska enačba).
Vendar so te močne podlage NaOH, KOH in drugi iz kovinskih hidroksidov (CSOH) iz kovinskih hidroksidov (CSOH). To so zelo topne ionske spojine v vodi, torej njihov OH- Lahko sodelujejo v kemičnih reakcijah.
Po drugi strani so netopni kovinski hidroksidi in posledično so zelo šibke podlage. Tudi nekateri so kisli, kot je to pri Tellurski kislini, TE (OH)6.
Hidroksid vzpostavlja ravnovesje topnosti s topilom okoli njega. Če je na primer voda, se ravnotežje izraža na naslednji način:
M (OH)2 M2+(AC) + OH-(AC)
Kjer (ac) označuje, da je medij vodni. Ko je trdna snov netopna, je koncentracija raztopljene OH majhna ali zaničljiva. Zaradi tega netopni kovinski hidroksidi ne morejo ustvariti rešitev tako osnovne kot NaOH.
Iz zgoraj navedenega je mogoče razbrati, da hidroksidi kažejo zelo različne lastnosti, povezane s kemijsko strukturo in interakcijami med kovino in OH. Čeprav so mnogi ionski, z raznolikimi kristalnimi strukturami, imajo tudi druge zapletene in zmedene polimerne strukture.
Lastnosti hidroksida
Oh anion-
Hidroksilni ion je atom kisika, povezan z vodikom. Tako je to zlahka predstavljeno kot OH-. Negativna obremenitev je nameščena na kisiku, zaradi česar je ta anion darovalec elektronov: baza.
Če oh- Izdelala svoje elektrone v vodik, tvori se molekula H2Tudi. Svoje elektrone lahko podarite tudi za pozitivne vrste: kot kovinska središča m+. Tako se koordinacijski kompleks oblikuje s pomočjo M-OH Dative (kisik zagotavlja par elektronov).
Vendar pa se mora to kisik učinkovito uskladiti s kovino, sicer pa bodo interakcije med M in OH imeli označen ionski značaj (m+ Oh-).
Vam lahko služi: volumetrična pipeta: značilnosti, uporabe, umerjanje in napakeKer je hidroksilni ion v vseh hidroksidih enak, je razlika med vsemi v kationu, ki ga spremlja.
Prav tako, ker lahko ta kation izhaja iz katere koli kovine iz periodične tabele (skupine 1, 2, 14, 15, 16 ali prehodnih kovin), se lastnosti takšnih hidroksidov močno razlikujejo, čeprav vsi skupaj razmišljajo o nekaterih vidikih.
Ionski in osnovni značaj
Hidroksidi, čeprav imajo koordinacijske povezave, imajo latentni ionski značaj. V nekaterih, kot je NaOH, so njegovi ioni del kristalne mreže, ki jo sestavljajo NA Kationi+ in oh anioni- v razmerjih 1: 1; to je za vsak na ion+ Obstaja oh ion- kolega.
Odvisno od kovinske obremenitve bo več ali manj OH Anions- okoli tega. Na primer za kovinski kation m2+ Bosta dva OH iona- interakcija z njim: M (OH)2, Kaj je skice, kot je HO- M2+ Oh-.
Na enak način se zgodi s kovinami m3+ in z drugimi bolj pozitivnimi stroški (čeprav redko presegajo 3+).
Ta ionski značaj je odgovoren za številne fizikalne lastnosti, kot so fuzija in vrelišča. Ti so visoki, kar odraža elektrostatične sile, ki delujejo v kristalni mreži. Tudi ko se hidroksidi raztopijo ali stopijo, lahko zaradi mobilnosti ionov izvedejo električni tok.
Vendar pa vsi hidroksidi nimajo enakih kristalnih omrežij. Tisti z najbolj stabilnimi bodo manj nagnjeni k raztopini v polarnih topilih, kot je voda. Na splošno so bolj različni ionski radijski sprejemniki M+ in oh-, Bolj topno bo enako.
Periodični trend
Zgornje pojasnjuje, zakaj se topnost alkalnih kovinskih hidroksidov povečuje, ko se skupina spušča. Tako je vse večji red topnosti v vodi za to: lioh Oh- To je majhen anion, in ko kation postane bolj zajeten, kristalna mreža oslabi energijo. Po drugi strani alkalinoterne kovine tvorijo manj topne hidrokside zaradi največjih pozitivnih obremenitev. To je zato, ker m2+ Privabi več sile v OH- v primerjavi z m+. Prav tako so njeni kationi manjši in zato manj neenakosti v primerjavi z OH-. Rezultat tega je eksperimentalni dokaz, da je NaOH veliko bolj osnoven kot CA (OH)2. Enako sklepanje je mogoče uporabiti za druge hidrokside, bodisi za tiste iz prehodnih kovin bodisi za tiste iz bloka P (Al, PB, TE itd.). Tudi manjši in velik ionski polmer in pozitivna obremenitev m+, Minor bo ionski značaj hidroksida, z drugimi besedami, tisti z zelo veliko gostoto obremenitve. Primer tega se zgodi z berilskim hidroksidom, BE (OH)2. On bo2+ Gre za zelo majhen kation in njegova dvovalentna obremenitev je električno zelo gosta. M hidroksidi (OH)2 reagirati s kislinami, da tvorijo akkokompleks, torej m+ konci, obkroženi z molekulami vode. Vendar pa obstaja omejeno število hidroksidov, ki lahko tudi reagirajo z bazami. To so tisti, ki so znani kot amfoteros hidroksidi. Anfoterski hidroksidi reagirajo tako s kislinami kot bazami. Druga situacija je lahko predstavljena z naslednjo kemijsko enačbo: M (OH)2 + Oh- => M (OH)3- Kako pa ugotoviti, ali je hidroksid amfoter? S preprostim laboratorijskim poskusom. Ker je veliko kovinskih hidroksidov netopnih v vodi in dodamo močno podlago z raztopino z M ioni+ raztopljeno, na primer3+, Bo oboril ustrezen hidroksid: Do3+(Ac) + 3oh-(AC) => AH (OH)3(S) Ampak imeti presežek OH- Hidroksid še naprej reagira: Al (OH)3(s) + oh- => Al (oh)4-(AC) Kot rezultat, nov negativni kompleks tovora teli z okoliškimi molekulami vode, ki raztaplja beli aluminijev hidroksid. Tisti hidroksidi, ki ostanejo nespremenjeni z dodatkom dodatnega baz, se ne obnašajo kot kisline in zato niso amfotični. Hidroksidi imajo lahko kristalne strukture, podobne tistim iz številnih soli ali oksidov; Nekateri preprosti, drugi pa zelo zapleteni. Poleg tega lahko tisti, kjer pride do zmanjšanja ionskega značaja, predstavljajo kovinske centre, ki jih združujejo kisiški mostovi. V raztopini so strukture različne. Čeprav je za zelo topne hidrokside dovolj, da jih obravnavamo kot ione, raztopljene v vodi, za druge je treba upoštevati kemijo usklajevanja. Tako vsak kation m+ Lahko uskladimo na omejeno število vrst. Bolj zajetno, večje je število molekul vode ali OH- povezan z njim. Od tod nastane znamenit koordinacijski oktaeder številnih kovin, raztopljenih v vodi (ali v katerem koli drugem topilu): M (OH2)6+n, biti enak pozitivni kovinski obremenitvi. Cr (OH)3, Na primer, res oktaedron. Kot? Glede na spojino kot [CR (OH2)3(OH)3], od tega tri molekule vode nadomeščajo OH anioni-. Če bi vse molekule zamenjali z OH-, Potem bi dobili negativno obremenitev in oktaedrsko strukturo [CR (OH)6]3-. Obremenitev -3 je rezultat šestih negativnih nabojev OH-. Hidroksidi lahko štejemo za "hidrirane okside". Vendar je v njih "voda" v neposrednem stiku z M+; medtem ko je v navlaženih oksidih mo · nh2Ali pa so molekule vode del zunanje koordinacijske sfere (niso blizu kovine). Te molekule vode lahko ekstrahiramo s segrevanjem vzorca hidroksida: M (OH)2 + Q (toplota) => mo + h2Tudi MO je kovinski oksid, ki je nastal kot posledica dehidracije hidroksida. Primer te reakcije je tisto, kar opazimo pri cupric hidroksidu, Cu (OH) je dehidriran2: Cu (OH)2 (modra) + q => cuo (črna) + h2Tudi Kakšen je pravi način, da omenjam hidrokside? IUPAC je v ta namen dvignil tri nomenklature: tradicionalno, zalogo in sistematično. Pravilno je uporabiti katero koli od treh, vendar je za nekatere hidrokside morda bolj udobno ali praktično omeniti tako ali drugače. Tradicionalna nomenklatura je preprosto sestavljena iz dodajanja najvišje valence, ki jo predstavlja kovina; in pripona -le najnižja. Tako na primer, če ima kovina M valence +3 in +1, hidroksid M (OH)3 Imenuje se hidroksid (kovinsko ime)ICO, medtem ko MOH hidroksid (kovinsko ime)medved. Za določitev, kakšna je kovinska valencia v hidroksidu, je dovolj za opazovanje številke po OH, zaprtem v oklepajih. Tako, m (OH)5 To pomeni, da ima kovina obremenitev ali valenco +5. Glavna neprijetnost te nomenklature pa je, da je lahko zapletena za kovine z več kot dvema stanjem oksidacije (kot pri Chromu in manganu). V takih primerih se za označevanje najvišjih in najnižjih valenc uporabljajo hiper-in hiper predpone. Če ima M namesto samo valence +3 in +1, ima tudi +4 in +2, potem so imena njegovih največjih hidroksidov in manjših valenc: hidroksid hiper(Kovinsko ime)ICO, in hidroksid kolcanje(Kovinsko ime)medved. Od vseh nomenklatura je to najpreprostejše. Tu imenu hidroksida preprosto sledi valencia kovine, zaklenjene v oklepajih in zapisano v rimskih številkah. Spet za M (OH)5, Na primer, njegova nomenklatura zalog bi bila: hidroksid (kovinsko ime) (v). (V) denota potem (+5). Nazadnje je za sistematično nomenklaturo značilno, da se zateče k množilnim predponam (di-, tri-, tetra-, penta-, hexa- itd.). Te predpone se uporabljajo za določitev števila kovinskih atomov in OH ionov-. Na ta način M (OH)5 Poimenovan je: pentahidroksid (kovinsko ime). V primeru HG2(OH)2, Na primer, to bi bil dihidroksid Dimercury; Eden od hidroksidov, katerega kemična struktura je na prvi pogled zapletena. Nekaj primerov hidroksidov in ustreznih nomenklatur je tisti, ki sledijo: -NaOH (natrijev hidroksid) -CA (OH) 2 (kalcijev hidroksid) -Vera (OH)3 (Železov hidroksid; železni hidroksid (III); ali železni trihidroksid). -V (OH)5 (Pervanat hidroksid; vanadijev hidroksid (V); ali vanadijev pentahidroksid). -Sn (oh)4 (Hidroksid Isñico; kositer hidroksid (IV); ali kositer tetrahidroksid). -Ba (oh)2 (Barijev hidroksid ali barijev dihidroksid). -Mn (OH)6 (Manganiski hidroksid, manganski hidroksid (VI) ali manganski heksahidroksid). -Augah (argikalni hidroksid, srebrni hidroksid ali srebrni hidroksid). Upoštevajte, da za to spojino ni razlikovanja med zalogami in sistematičnimi nomenklaturami. -PB (OH)4 (Plúmbic hidroksid, svinčev hidroksid (IV) ali svinčev tetrahidroksid). -Liop (litijev hidroksid). -CD (OH) 2 (kadmijev hidroksid). -Ba (oh)2 (Barijev hidroksid). -Kromijev hidroksid.Anfoterizem
Strukture
Reakcija dehidracije
Nomenklatura hidroksida
Tradicionalno
Zaloga
Sistematično
Primeri hidroksidov
 Videz natrijevega hidroksida
Videz natrijevega hidroksida  Videz trdnega stanja kalcijevega hidroksida
Videz trdnega stanja kalcijevega hidroksida Reference

