Hidroksilna skupina

- 3646
- 84
- Mr. Shane Larkin
Pojasnjujemo, kaj so hidroksilna skupina, njene značilnosti, struktura in več primerov
 Kemična struktura hidroksilne skupine
Kemična struktura hidroksilne skupine Kaj je hidroksilna skupina?
A Hidroksilna skupina Je funkcionalna skupina ali del drugih funkcionalnih skupin, ki so prisotni v številnih organskih in anorganskih spojinah. Nastane ga vodikov atom in eden od kisika (od tod tudi ime).
Hidroksilne skupine so običajno povezane z ogljikovim atomom ali drugim nemetalnim elementom, kot sta žveplo ali fosfor, med drugim in so ena najpomembnejših funkcionalnih skupin v organski kemiji.
Ta skupina atomov je prisotna v organskih funkcionalnih skupinah, kot so alkoholi, fenoli in karboksilne kisline, in je tista, ki vsakemu od teh funkcionalnih skupin daje značilnosti značilnosti kemijskih lastnosti. V različnih strukturah ga je mogoče predstaviti kot -oh ali ho-
Značilnosti hidroksilnih skupin
- Sestavljen je iz atoma kisika in enega od vodika, povezanih med seboj in je povezan z drugim atomom v molekuli skozi kovalentne vezi.
- Povezava med atomom vodika in kisika je polarna vez, pri kateri ima kisik negativno delno obremenitev in pozitivno delno obremenitev, zaradi česar je hidroksilna skupina polarna funkcionalna skupina A.
- Ima strukturo, podobno strukturi vode. Zaradi tega so številne spojine, ki ga vsebujejo, običajno topne v omenjenem topilu.
- Ima vodik, ki je neposredno povezan z atomom kisika, tako da lahko hidroksilna skupina tvori vodikovo vez, v kateri sodeluje kot darovna vodikova skupina.
- Če ima dva prosta elektrona na atomu kisika, lahko hidroksilna skupina tvori dve dodatni vodikovi vezi, ki delujeta kot sprejemnik vodikovih atomov.
- Lahko delujete kot kislina tako, da daste protonu bazi. Hidroksilna skupina lahko odvisno od funkcionalne skupine, katere del je del, in atoma, na katero je neposredno povezan. Na primer, v alkoholih ima PKA 15 ali več (ostro kislino kot voda), v fenolih se giblje med 7 in 10, medtem ko je v karboksilnih kislinah običajno med 4 in 5.
- Delujete lahko tudi kot baza Lewis, ki podarite enega od svojih elektronskih parov, da se povežejo z drugim protonom ali kakšno drugo Lewisovo kislino.
Struktura hidroksilne skupine
Kot je omenjeno med značilnostmi, atomi kisika in vodika v hidroksilni skupini tvorijo polarno kovalentno vez.
Poleg tega atom kisika tvori drugo kovalentno vez z drugim atomom, ki je del molekule kot alkohol, fenol v kakšno drugo spojino. Spodaj je predstavljena struktura Lewis te skupine:
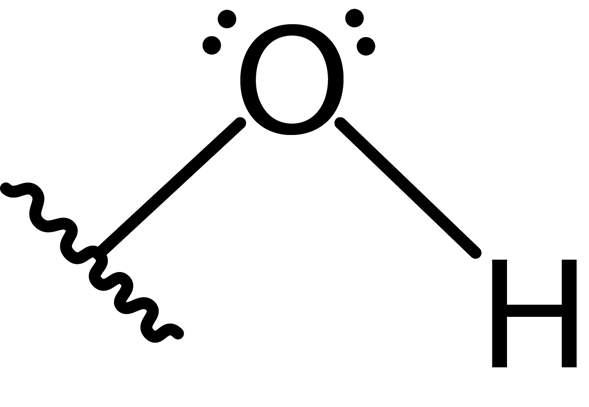
Zaradi prisotnosti dveh parov prostih elektronov na atomu kisika in obeh kovalentnih vezi ima hidroksilna skupina kotno geometrijo s kotom približno 104 °, nekoliko nižji od tetraedrskega kota. Dolžina vezi kisika-vodikove vezi je približno 0.97 angstromi.
Hidroksilna skupina, hidroksilni radikal in hidroksidni anion
Zelo pogosto je zmešati hidroksilno skupino s hidroksilnim radikalom in hidroksidnim anionom, saj vsi tvorita ista dva atoma, vendar se ti izrazi ne nanašajo na isto.
Po eni strani se hidroksilni radikal razlikuje od hidroksilne skupine, v kateri je prosti radikal z neparnim številom valenčnih elektronov, prav tako pa ni povezan z nobenim drugim atomom ali skupino atomov (zato mu rečejo brezplačno).
Kljub tem razlikam mnogi napačno uporabljajo izraz hidroksilnega radikala, da se nanašajo na hidroksilno skupino, kadar je prisotna v molekuli.
Hidroksidni anion je na drugi strani ion z negativno obremenitvijo, ki ga tvorita vodik in kisik, medtem ko je hidroksilna skupina nevtralna skupina.
Poleg tega, medtem ko je hidroksilna skupina vedno povezana z molekulo s kovalentno vezjo, spojine, ki vsebujejo hidroksidne ione, imajo ionsko vez med to in nekaj kovine, kot so natrij, litij ali kalij.
Vam lahko služi: kakšna sta anoda in katoda?Primeri hidroksilne skupine
Alkoholi
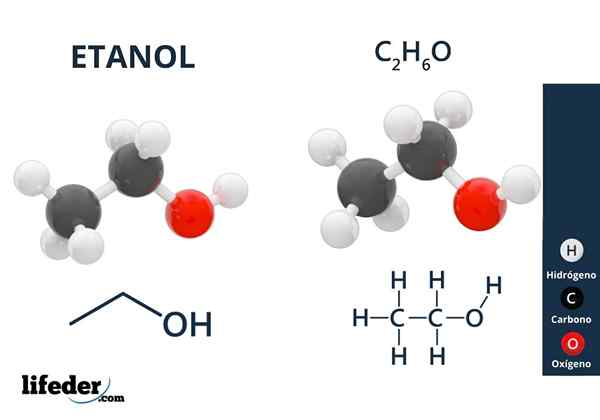 Etanol
Etanol Alkoholi imajo hidroksilne skupine, povezane z alifatskim ogljikom. Primeri alkoholov so:
- Metilni alkohol.
- Etanol.
- Izopropilni alkohol.
Fenoli
Za fenole je značilno, da ima hidroksilna skupina, ki je neposredno povezana z aromatičnim obročem. Nekaj primerov skupnih fenolov je:
- Fenol.
- Alfa in beta-naftol.
- Ortho, cilj in za Cresol.
Ogljikovi hidrati
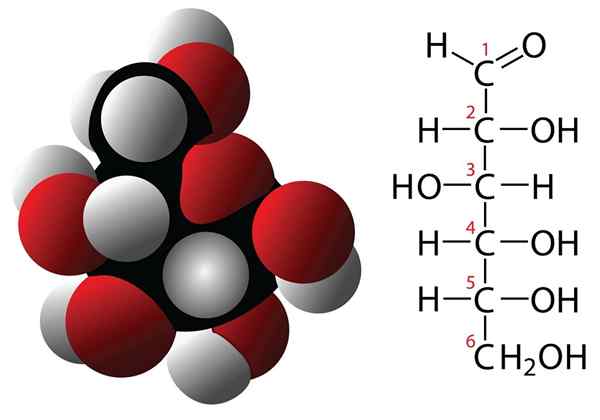 Molekula glukoze in molekularne formule
Molekula glukoze in molekularne formule Ogljikovi hidrati so spojine s 3 ali več ogljikovih atomov, za katere je značilna empirična formula, ki jo tvorijo ogljikovi in vodne molekule. Te spojine imajo pogosto več hidroksilskih skupin, zaradi česar so zelo topne v vodi. Nekaj primerov ogljikovih hidratov je:
- Glukoza.
- Fruktoza.
- Saharoza.
Karboksilne kisline
Karboksilna funkcionalna skupina, ki je prisotna v karboksilnih kislinah, ustreza eni najbolj kisle funkcionalne skupine, ki jo ima lahko organska molekula. Te spojine so običajno šibke kisline, če jih primerjamo z nekaterimi mineralnimi kislinami, vendar lahko postanejo precej kisle, odvisno od njihove strukture.
Kislost karboksilne skupine je posledica prisotnosti hidroksilne skupine, povezane s karbonilno skupino, ki stabilizira negativno obremenitev aniona, ki nastane, ko hidroksil daje svoj proton. Nekaj primerov karboksilnih kislin je:
- Ocetna kislina.
- Benzojska kislina.
- Trifluoroocetna kislina.
Sulfonske kisline
Sulfonske kisline so organske spojine, ki tvorijo reakcijo med nekaterimi organskimi spojinami in žveplovo kislino ali žveplovim dioksidom. Te vrste spojin imajo hidroksilno skupino in so na splošno precej močne kisline, primerljive z žveplovo kislino.
Nekaj primerov sulfonskih kislin je:
- Pentosulfonska kislina.
- Ortho, cilj in toluensulfonske kisline.
- Benzeulfonska kislina.
Anorganske kisline
Hidroksilne skupine se ne pojavljajo samo v organskih spojinah. Številne anorganske spojine jih imajo tudi, zlasti oksicidne kisline. V teh primerih je hidroksilna skupina neposredno povezana z ne -metalom, ki se običajno razlikuje od ogljika.
Nekaj primerov anorganskih kislin, ki imajo hidroksilne skupine, skupaj z ne -kometalom, na katere je povezano, je:
- Hipoklorozna kislina, v kateri je hidroksilna skupina povezana z atomom klora.
- Žveplova kislina, ki ima dve hidroksilni skupini, povezani z atomom žvepla.
- Fosforna kislina, v kateri so tri hidroksilne skupine povezane z atomom fosforja.

