Struktura kalijevega fosfata (K3PO4), lastnosti, uporablja

- 3993
- 207
- Lee Farrell
On Kalijev fosfat Gre+ in fosfatni ion po43-. Njegova kemična formula je k3Po4. Je brezbarvna trdna ali kristalna bela. V vodi je zelo topen, ki tvori alkalne raztopine, torej z mnogimi OH ioni-, Zato osnovni pH.
Fosfatni ion ima pomembno funkcijo v celicah, ki so povezane s shranjevanjem energije. Kalijev fosfat se pogosto uporablja v reakcijah organske kemije, v katerih lahko deluje kot osnova, torej jemanje protonov H+. Lahko deluje tudi kot katalizator ali pospeševalnik nekaterih reakcij.
 Kalijev fosfat k3Po4 trden. Xavier13540 na kitajski Wikipediji [javna domena]. Vir: Wikimedia Commons.
Kalijev fosfat k3Po4 trden. Xavier13540 na kitajski Wikipediji [javna domena]. Vir: Wikimedia Commons. Uporablja se za zmanjšanje napada nekaterih žuželk v pšeničnih rastlinah, ker jih naredi bolj odporni. Vendar je bilo opaziti, da je naklonjen odvajanju metana (ch4), Toplogredni plin, mikrokulture riža.
Uporablja se kot odvajalo, za povečanje trajanja lokalne anestezije, zaustavitev kariesa in za pomoč pri pokrivanju površin, med drugimi aplikacijami.
[TOC]
Struktura
Kalijev fosfat sestavljajo tri katione kalij K+ in fosfatni anion po43-.
Fosfatni ion po43- Nastane ga s fosforjevim (P) atomom in štirimi atomi kisika (O).
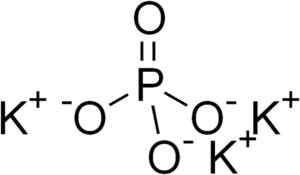 Struktura kalijevega fosfata k3Po4. Edgar181 [javna domena]. Vir: Wikimedia Commons.
Struktura kalijevega fosfata k3Po4. Edgar181 [javna domena]. Vir: Wikimedia Commons. Nomenklatura
- Kalijev fosfat
- Tripotasijev fosfat
- Kalijev tribazični fosfat
- Tripotasijev ortofosfat
Lastnosti
Fizično stanje
Brezbarvna trdna ali kristalno bela.
Molekularna teža
212,27 g/mol
Tališče
1340 ° C
Gostota
2.564 g/cm3
Topnost
Zelo topno v vodi: 106 g/100 g vode pri 25 ° C. Netopna v etanolu.
ph
Rešitev z 1% K3Po4 Ima pH 11,5-12,3.
Kemične lastnosti
Z raztapljanjem v vodi se kalijev fosfat loči na tri katione kalij K+ in fosfatni anion po43-. Fosfatni anion ima proton vode in tvori HPO hidrogenofosfatni anion42-. Slednji vzame še en proton vode in postane dihidrogenofosfat h anion2Po4-.
Vam lahko služi: kako je sintetiziran elastični material?Po43- + H2Ali ⇔ HPO42- + Oh-
HPO42- + H2Ali ⇔ h2Po4- + Oh-
Ko oblikujejo ione oh- Vodna raztopina postane alkalna.
Druge lastnosti
Poleg brezvodne oblike (brez vode) ima več hidriranih oblik; To pomeni, da je K molekula K3Po4 Spremlja ga lahko ena ali več molekul vode znotraj kristalne strukture.
Zaradi tega lahko oblikujete na primer k monohidrat3Po4.H2Ali3Po4.3H2Ali, heptidrat in ne -dehidrat.
Funkcija fosfata v človeškem organizmu
Fosfatni ion po43- Je najpogostejši anion znotraj celic in izvaja pomembno funkcijo pri shranjevanju energije.
Fosfatni ion sodeluje tudi pri tvorbi in prehranskih aktivnostih kosti in zob, saj uravnava koncentracijo kalcija na krvnem serumu in v številnih reakcijah prenosa energije v celici.
Pridobivanje
Kalijev fosfat lahko dobimo iz reakcije med KCl kalijevim kloridom in amonijevim fosfatom (NH4)3Po4.
Kalijev klorid + amonijev fosfat → kalijev fosfat + amonijev klorid
3 kCl + (NH4)3Po4 → k3Po4 + 3 nh4Cl
Prijave
Kot osnova v reakcijah organske kemije
Kalijev fosfat k3Po4 Uporablja se v več reakcijah organske kemije. Na primer, služi v sintezi acetilenov, ki temeljijo na dibromiranih spojinah.
V tej sintezi se pojavi dehidrobromatizacija (izločanje vodika in bromoja), kjer je K3Po4 Ashidro trdna (brez vode) deluje kot mehka podlaga in odvzema dva protona iz molekule, dva atoma broma se izločita in dobimo ustrezen acetilen.
C6H5-Chbr-ch2Br + 2 k3Po4 → c6H5-C≡CH + 2 KBR + 2 K2HPO4
 Avtor: Clker-brez vektorjev. Vir: Pixabay.
Avtor: Clker-brez vektorjev. Vir: Pixabay. Kot katalizator
K3Po4 Služi kot katalizator v različnih reakcijah organske kemije. Na primer, uporablja se kot trdna snov za pridobivanje biodizla iz uporabljenega olja.
Biodizel je gorivo, podobno dizelskemu.
Vam lahko služi: coulombimetrija: osnove, vrste, aplikacijeKalijev fosfat je bil učinkovitejši kot katalizator ali pospeševalnik omenjene reakcije kot natrijev fosfat3Po4 in cao kalcijev oksid.
V kmetijstvu
K3Po4 Uporablja se za zdravljenje pšeničnih rastlin in jih naredi odporne na določene škodljivce.
 Pšenične rastline lahko zdravimo s k3Po4 biti odporen na nekatere vrste žuželk. Avtor: Hans Braxmeier. Vir: Pixabay.
Pšenične rastline lahko zdravimo s k3Po4 biti odporen na nekatere vrste žuželk. Avtor: Hans Braxmeier. Vir: Pixabay. Nekateri raziskovalci so preizkusili sadike pšenice s kalijevim fosfatom in izkazali, da je ta odpor proti listni uši Duraphis Noxia, Žuželka, ki napade te rastline.
Po uporabi razredčene raztopine K3Po4 Na sadikah je bilo manj resnosti simptomov, ki so jih povzročile te žuželke, in zmanjšano število listnih uši, ki se hranijo s temi.
 Avtor: Hans Braxmeier. Vir: Pixabay.
Avtor: Hans Braxmeier. Vir: Pixabay. V medicinskih aplikacijah
Za spreminjanje anestetičnega učinka lidokaina, lokalnega anestetika, je bil uporabljen kalijev fosfat. Lokalni anestetik je zdravilo, ki pri uporabi na območju telesa povzroči izgubo občutljivosti na bolečino na tem območju.
Ugotovljeno je bilo, da K3Po4 Omogoča podaljšanje lokalne anestezije lidokaina.
Kot odvajalo
Kalijev fosfat poveča fluidnost črevesne vsebnosti, ker pomaga ohraniti vodo v črevesju, kar posredno povzroči krčenje črevesja.
V veterinarski medicini
K3Po4 Uporablja se pri živalih z diabetično ketoacidozo (zaplet sladkorne bolezni) za zdravljenje hipofospatije (majhna količina fosfata v krvi).
Vendar, ko ga dovajamo v presežku, lahko povzroči hipokalcemijo (malo kalcija v krvi), hiperfostatijo (presežek fosfata v krvi), neprostovoljno krčenje mišic, mineralizacija mehkih tkiv in odpovedi ledvic.
 Pse s diabetično acidozo lahko zdravimo s kalijevim fosfatom. Avtor: David Mark. Vir: Pixabay.
Pse s diabetično acidozo lahko zdravimo s kalijevim fosfatom. Avtor: David Mark. Vir: Pixabay. Pri pridobivanju DNK
Kalijev fosfat je bil uporabljen kot pufer za čiščenje DNK v genetičnih laboratorijih.
DNK je protein, ki ga najdemo v celicah in vsebuje vse genetske informacije, potrebne za razvoj in delovanje živih bitij.
Lahko vam služi: delna destilacija: postopek, oprema, aplikacije, primeriZ izolacijo DNK se znanstveniki poglobijo v preučevanje, kako se prenašajo dedni liki, zato je kalijev fosfat zelo koristen.
 Risanje molekule DNK. Avtor: javne domene. Vir: Pixabay.
Risanje molekule DNK. Avtor: javne domene. Vir: Pixabay. V več aplikacijah
Kalijev fosfat k3Po4 Služi:
- Kot prehransko dopolnilo,
- Za zamenjavo elektrolitov,
- Kot pufer, torej kot kemični sistem, ki omogoča nadzor nad ravnijo OH ionov- ali vodik h+ V vodni raztopini,
- Ustaviti ali zavirati nastanek zobnega kariesa,
- kot zaviralec korozije in anti -Sniff,
- Kot sredstvo za zdravljenje površin in nanosa,
- kot antifriz,
- pri čiščenju izdelkov.
 Korodirane cevi. K3Po4 omogoča, da se izognemo koroziji v cevi nekaterih panog ali procesov. Avtor: Michael Gaida. Vir: Pixabay.
Korodirane cevi. K3Po4 omogoča, da se izognemo koroziji v cevi nekaterih panog ali procesov. Avtor: Michael Gaida. Vir: Pixabay. Negativni vidik za uporabo v kmetijstvu
Nekateri raziskovalci so to ugotovili z dodajanjem k3Po4 Emisija metana se poveča na mikrokulturo riža (izberite4) v ozračje. Metan je plin, ki prispeva k učinku toplogrednih plinov in zvišanju temperature našega planeta.
Reference
- Ali.S. Nacionalna knjižnica medicine. (2019). Kalijev fosfat. Okrevano od PubChema.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Panciera, d.L. (2012). Terapija s tekočino pri endokrinih in presnovnih motnjah. Dodatek fosforja. V tekočini, elektrolitu in kislinskih baznih motnjah v praksi majhnih živali (četrta izdaja). Okrevano od Scientirect.com.
- Shenawi-Khalil, s. et al. (2012). Sinteza acetilenov z dehidrobromacijo z uporabo trdnega brezvodnega kalijevega fosfata kot podstavka v stanju faznega prenosa. Tetrahedronske črke, letnik 53, številka 18, 2012, strani 2295-2297. Okrevano od Scientirect.com.
- Guan, g. et al. (2009). Tri-pasijev fosfat kot trden katalizator za proizvodnjo biodizla iz olja za kuhanje odpadkov. Tehnologija obdelave goriva, letnik 90, številka 4, 2009, strani 520-524. Okrevano od Scientirect.com.
- Kulkami, m.Do. (2012). Mehanski pristop za širjenje in sintezo α-hidroksi fosfonatov z uporabo kalijevega fosfata kot katalizatorja. Comptes Rendus Chimie, vol. 16, številka 2, 2013, strani 148-152. Okrevano od Scientirect.com.
- Venter, e. et al. (2014). Kalijev phhosfat inducira toleranco proti instal ruske pšenične uši (Duraphis Noxia, Homoptera: Aphididae) v pšenici. Zaščita pridelkov Vol 61, julij 2014, strani 43-50. Okrevano od Scientirect.com.
- Bonturi, n. et al. (2013). Natrijev citrat in kalijev fosfat kot alternativni adsorpcijski puferji v hidrofobnem in aromatičnem tiofilnem kromatografskem čiščenju plazmidne DNK iz nevtraliziranega lizata. Časopis za kromatografijo B, zvezki 919-920, 2013, strani 67–74. Okrevano od Scientirect.com.
- Conrad, r. in Klose, m. (2005). Vpliv oploditve kalijevega fosfata na proizvodnjo in emisije metana in njegovega 13C-stabilna sestava izotopov v mikrokozmosu riža. Biologija tal in biokemija, vol. 37, številka 11. 2005, strani 2099-2108. Okrevano od Scientirect.com.
- Svinec, d.R. (Urednik) (2003). Priročnik za kemijo in fiziko CRC. 85th CRC Press.
- Smokefoot. (2019). Tipitassium fosfat. Pridobljeno iz.Wikipedija.org
- « Značilnosti vhodne naprave, kakšne so uporabe, tipi, primeri
- Struktura faktorja nekroze tumorja (TNF), mehanizem delovanja, delovanje »

