Faktor redčenja
- 2639
- 295
- Ms. Pablo Lebsack
 Serijsko redčenje
Serijsko redčenje Kakšen je faktor redčenja?
On Faktor redčenja (FD) je število, ki označuje čase, da je treba raztopino razredčiti, da dobimo nižjo koncentracijo. Raztopina lahko raztopi bodisi trdno, tekoče ali plinasto topilo.
Zato je njegova koncentracija odvisna od števila delcev topljene in celotne prostornine V.
Na področju kemije se uporablja veliko izrazov koncentracije: odstotek, molarni (m), normalno (n), med drugim. Vsak od njih je odvisen od končne količine topljene; Od gramov, kilogramov ali molov do enakovrednih.
Vendar pa pri zmanjševanju takšnih koncentracij FD velja za vse te izraze.
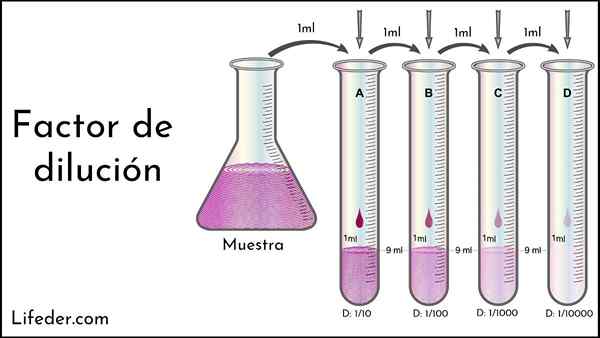
Na vrhunski sliki je primer zaporednega redčenja. Upoštevajte, da od leve proti desni vijolična barva postane jasnejša; ki je enaka nižji koncentraciji vzorca.
Faktor redčenja omogoča določitev, kako razredčeno je zadnje plovilo glede na prvo. Tako lahko namesto preprostih organoleptičnih lastnosti poskus ponovimo iz istega FD iz iste steklenice matične raztopine ali vzorca, tako da je zagotovljeno, da so koncentracije novih žil enake.
Koncentracija se lahko izrazi v kateri koli enoti; Vendar je prostornina žil konstantna in za olajšanje izračunov se preprosto uporablja za količine vzorca, raztopljenega v vodi. Vsota teh bo enaka V: prostornina skupne tekočine v steklu.
Tako kot pri primeru vzorca se tudi v laboratoriju dogaja s katerim koli drugim reagentom. Pripravljene so koncentrirane matere raztopine, od katerih se odvzamejo alikvoti, in razredčeni, da dobijo več razredčenih raztopin. To želi zmanjšati laboratorijska tveganja in izgube reagenta.
Kakšen je faktor redčenja?
Redčenje
Razredčenje je postopek, ki omogoča zmanjšanje koncentracije raztopine ali njegove gostote. Ukrep za zmanjšanje intenzivnosti barve v raztopini barvila je mogoče obravnavati tudi kot redčenje.
Za uspešno razredčenje raztopine do določene koncentracije je treba prvo, kar je treba storiti, vedeti, kolikokrat je koncentracija matične raztopine večja glede na koncentracijo razredčene raztopine.
Lahko vam služi: kalijev dihromro: formula, lastnosti, tveganja in uporabeTako je treba časi začetne raztopine razredčiti, da dobimo raztopino z želeno koncentracijo. Številokrat je znano kot faktor redčenja. In to je v brezdimenzionalni frakciji, kar kaže na redčenje.
Dejavniki
Običajno je, da najdete razredčenje, na primer, na primer: 1/5, 1/10, 1/100 itd. To kaže, da za pridobitev raztopine z želeno koncentracijo, matično raztopino, ki jo poimenovalec frakcije z imenom.
Če na primer uporabimo 1/5 redčenja, je treba začetno raztopino razredčiti, da dobimo raztopino s to koncentracijo 5 -krat. Zato je številka 5 faktor redčenja. To prevaja na naslednji način: Rešitev 1/5 je petkrat bolj razredčena kot mati.
Kako pripraviti to rešitev? Če jemljemo 1 ml matične raztopine, je treba ta volumen, da se koncentracija topljenosti razredči za 1/5 faktorja. Če ga bomo razredčili z vodo (kot v primeru), je treba dodati 1 ml te raztopine 4 ml vode (1+4 = 5 ml končnega volumna VF).
Nato bomo komentirali, kako sklepati in izračunati FD.
Kako dobite faktor redčenja?
Odbitek
Za pripravo redčenja se začetna raztopina ali mati odpelje v oteženo bučko, kjer se doda voda, da se dokonča zmogljivost mere omenjene bučke.
V tem primeru, ko v aggorirano bučko dodamo vodo. Nato masa topljene ali raztopine ostane konstantna:
mYo = mF (1)
mYo = masa začetnega topka (v koncentrirani raztopini).
In mF = masa končnega topka (v razredčeni raztopini).
Ampak, m = v x c. Zamenjava v enačbi (1) imate:
VYo x cYo = VF x cF (2)
VYo = volumen matere ali začetne raztopine, ki je bila odvzeta za redčenje.
CYo = koncentracija matere ali začetne rešitve.
VF = volumen razredčene raztopine, ki je bila pripravljena.
CF = koncentracija razredčene raztopine.
Enačba 2 lahko zapišemo na naslednji način:
CYo / CF = VF / VYo (3)
Dva veljavna izraza za FD
Toda cYo / CF Po definiciji je Faktor redčenja, Ker kaže na čas, da je koncentracija matere ali začetne raztopine večja glede na koncentracijo razredčene raztopine.
Zato označuje redčenje, ki ga je treba izvesti za pripravo raztopine, razredčene iz matične raztopine.
Vam lahko služi: destilirana vodaPrav tako je mogoče iz opazovanja enačbe 3 sklepati, da je razmerje vF / VYo To je še en način za pridobitev Faktor redčenja. To je kateri koli od obeh izrazov (cYo/CF, VF/VYo) veljajo za izračun FD. Uporaba enega ali drugega bo odvisna od razpoložljivih podatkov.
Primeri
Primer 1
Za pripravo 0,015 M razredčene raztopine smo uporabili 0,3 M NaCl raztopino. Izračunajte vrednost faktorja redčenja.
Faktor redčenja je 20. To kaže, da je bilo treba za pripravo razredčene raztopine naCl 0,015 m 0,3 M NaCl raztopino razredčiti 20 -krat:
Fd = cYo / CF
0,3 m / 0,015 m
dvajset
Primer 2
Vedeti, da je faktor redčenja 15: kakšno volumen vode je treba dodati 5 ml koncentrirane raztopine glukoze, da se želeno redčenje naredi?
Kot prvi korak se izračuna prostornina razredčene raztopine (vF). Ko se izračuna, se izračuna dodana volumen vode, da se redčenje.
Fd = VF / VYo.
VF = Fd x vYo
15 x 5 ml
75 ml
Dodana volumen vode = 75 ml - 5 ml
70 ml
Nato smo pripravili razredčeno raztopino s faktorjem redčenja 15, 5 ml iz koncentrirane raztopine 70 ml vode, da smo izpolnili končni volumen 75 ml.
Primer 3
Koncentracija materne raztopine fruktoze je 10 g/l. Iz nje je želeti, da se iz njega pripravite raztopino fruktoze s koncentracijo 0,5 mg/ml. Od 20 ml matične raztopine do redčenja: kakšna naj bo prostornina razredčene raztopine?
Prvi korak za rešitev problema je izračun faktorja redčenja (FD). Ko dobimo, se izračuna prostornina razredčene raztopine (vF).
Toda pred dvigom izračuna je treba naslednje opazovanje: količine koncentracije fruktoze morate postaviti v istih enotah. V tem primeru je 10 g/l enakovredno 10 mg/ml, kar ponazarja to situacijo z naslednjo preobrazbo:
(mg/ml) = (g/l) x (1.000 mg/g) x (l/1.000 ml)
Zato:
10 g/l = 10 mg/ml
Nadaljevanje z izračuni:
Vam lahko služi: amineFd = cYo / CF
Fd = (10 mg/ml)/(0,2 mg/ml)
petdeset
Ampak kot vF = Fd x vYo
VF = 50 x 20 ml
1.000 ml
Torej, 20 ml raztopine 10 g/L fruktoze, 1L 0,2 g/l raztopine.
Primer 4
Ponazorjena bo metoda za serijsko redčenje. Obstaja raztopina glukoze s koncentracijo 32 mg/100 ml, iz nje pa je zaželena/100 ml, 2 mg/100 ml in 1 mg/100 ml.
Postopek
5 epruvetov je označenih za vsako koncentracijo, navedeno v izjavi. V vsakem sta nameščena 2 ml vode, na primer.
Nato do cevi 1 z vodo dodamo 2 ml matične raztopine. Vsebnost cevi 1 je mešana in 2 ml vsebine se prenese v cev 2. Po drugi strani je cev 2 vznemirjena in 2 ml vsebine se prenese v cev 3; nadaljuje na enak način s cevmi 4 in 5.
Pojasnilo
V cev 1 dodamo 2 ml vode in 2 ml matične raztopine s koncentracijo glukoze 32 mg/100 ml. Torej končna koncentracija glukoze v tej cevi je 16 mg/100 ml.
V cev 2 dodamo 2 ml vode in 2 ml vsebnosti cevi 1 s 16 mg/100 ml koncentracije glukoze. Nato v cevi 2 koncentracija cevi 1 razredčimo 2 -krat (FD). Torej končna koncentracija glukoze v tej cevi je 8 mg/100 ml.
Do epruvete 3 2 ml vode in 2 ml vsebnosti cevi 2 se dodajo koncentracija glukoze 8 mg/100 ml. In tako kot drugi dve cevi je koncentracija razdeljena na dva: 4 mg/100 ml glukoze v cevi 3.
Iz zgoraj navedenega razloga je končna koncentracija glukoze v cevi 4 oziroma 5 2 mg/100 ml in 1 mg/100 ml.
FD cevi 1, 2, 3, 4 in 5 glede na matično raztopino so: 2, 4, 8, 16 in 32.
Reference
- Aus in tute. (s.F). Izračuni faktorja redčenja. Vzet od: ausetute.com.Au
- J.T. (s.F.). Faktor redčenja. [PDF]. Vzet iz: CSUS.Edu
- Pomoč za redčenje.F.). Vzeto od: Uregina.AC
- Joshua (2011). Razlika med faktorjem redčenja in redčenja. Razlika med.mreža. Okrevano od: razlika med.mreža
- Whitten, Davis, Peck & Stanley. Kemija (8. izd.). Cengage učenje.
- Innovarte (2014). Serijska redčenja. Pridobljeno iz: 3.Uah.je

