Epoksi nomenklatura, pridobivanje, aplikacije, primeri
- 4646
- 39
- Cary Goyette
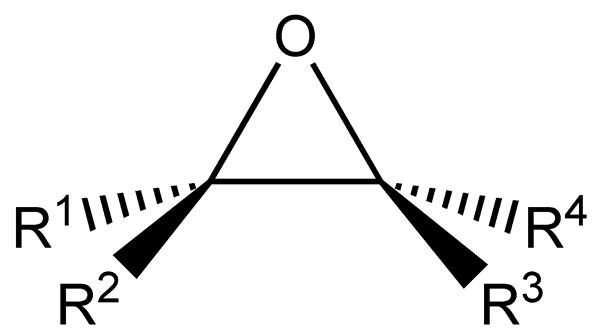
The Epoksidi So alifatski ali ciklični ogljikovodiki, ki imajo atom kisika, ki je hkrati povezan z dvema ogljikovih atomih v svoji strukturi. Ta povezava, kot je razvidno iz spodnje slike, predstavlja trikotno geometrijo, ki je zelo značilna za vse epokside.
Epoksidi izvirajo iz alkenov, ki trpijo rupturo dvojne vezi, da tvorijo funkcionalno skupino epoksida. Vsak od obeh atomov, povezanih s kisikom, je tudi povezan s stranskimi skupinami r1, R2, R3 in r4, Vsi deli iste molekule.
 Strukturna in splošna formula za epokside. Vir: Tomas Kindahl / Public Domain.
Strukturna in splošna formula za epokside. Vir: Tomas Kindahl / Public Domain. Za funkcionalno skupino epoksida je značilno, da ima veliko napetost, kar daje večjo reaktivnost kot pri necikličnem etru. Reakcije epoksida običajno spremlja ruptura njihove funkcionalne skupine.
Najpreprostejši epoksid ustreza etanskemu epoksidu, imenovan tudi etilen oksid, etilen oksid ali oksirano. Od vsega je to epoksid večjega komercialnega pomena.
Največji delež proizvodnje epoksida je namenjen slikanju (površinski premazi). Uporabljajo se tudi pri proizvodnji površinsko aktivnih snovi, lepil, mehčalcev itd.
[TOC]
Nomenklatura
Spojine s funkcionalno skupino epoksida lahko pokličemo na različne načine, kot so: epoksi, epoksidi ali druga imena brez sistematične konotacije, kot je: Oxirano.
Epoksidi s preprostejšimi kemičnimi strukturami so običajno imenovani kot oksidi. Na ta način propeno epoksid (c3H6) Imenuje se propeno oksid (c3H6Da).
Običajno se imenuje epoksid, ki identificira ogljikove ogljike, ki so prisotni v funkcionalni skupini epoksida. Na primer: 2,3-epoksiheksan, 1,2-epoksihikloheksan in 1,2-epoksipropan. Se pravi, "trikotnik" najdemo v ogljikih 2 in 3 heksana in tako naprej s ciklohekanjem in propanom.
Vam lahko služi: entalpijaPridobivanje
Katalitična oksidacija
Etno ali etilen oksid epoksid pripravimo s katalitično oksidacijo etilena v vročem zraku ali kisiku, ki se uporablja kot kovinski srebrni katalizator:
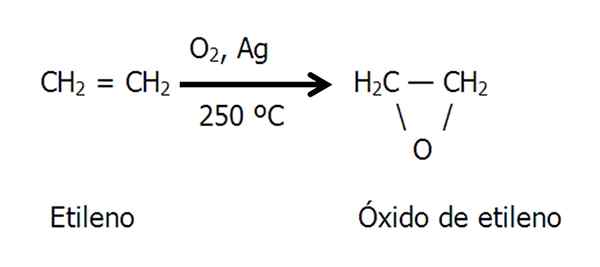 Enačba za sintezo etilen oksida. Vir: Gabriel Bolívar.
Enačba za sintezo etilen oksida. Vir: Gabriel Bolívar. Metoda klorohidrina
Ta metoda se izvaja v dveh stopnjah: a) tvorba klorohidrina in b) obdelava klorohirina z osnovo za izločanje klorovodikove kisline.
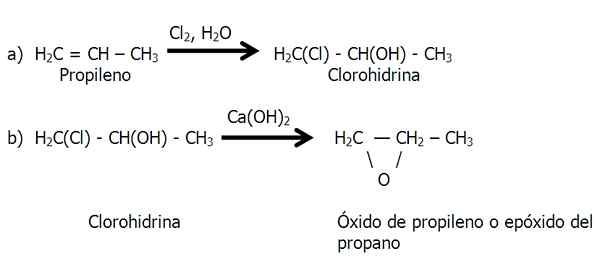 Stopnje metode klorohidrina za sintezo epoksida. Vir: Gabriel Bolívar.
Stopnje metode klorohidrina za sintezo epoksida. Vir: Gabriel Bolívar. V fazi B) izgubljena je molekula HCl, katere vodik prihaja iz skupine OH.
Peroksidacija ogljikovega ogljika z dvojnim vezanjem
Epokside se lahko tvorijo tudi s peroksidacijo alkenov, to je oksidacijo, ki jo povzroča razbojnik, kot je peroksibenzojska kislina:
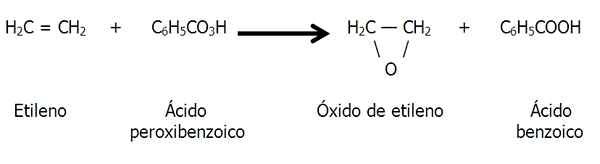 Peroksidacija etilena v tvorbo etilen oksida ali epoksida etana. Vir: Gabriel Bolívar.
Peroksidacija etilena v tvorbo etilen oksida ali epoksida etana. Vir: Gabriel Bolívar. Naravna prisotnost epoksidov
Epoksidi so po naravi nenavadni. Vendar je bila opažena sinteza jeter epoksidov, posredovana s citokromom P450. Celice proizvajajo epokside kot oksidacijske produkte alquenosa in aromatičnih spojin.
V naravi so opazili tudi spojine, kot so epotilonas, ki se proizvajajo kot sekundarni presnovek bakterij Sorangiumov violončele.
Prijave
Priprava površinsko aktivnih snovi
Etilen oksid se pogosto uporablja pri pripravi površinsko aktivnih snovi ali površinsko aktivnih snovi, alkoholnih ali fenolnih reakcijskih produktov z etilen oksidom. Površinsko aktivne snovi izpolnjujejo različne funkcije, vključno z: vlažilnimi sredstvi, detergenti, emulgatorji in solubilizatorji.
Vlažniki povečajo površinsko hidracijo z olajšanjem dostopa do vode do njih. Detergenti odpravijo umazanijo iz oblačil. Emulzije omogočajo in stabilizirajo emulzije. In solubilizatorji omogočajo raztapljanje nekaj mešljivih spojin z vodo.
Vam lahko služi: Fick LawLepila in topila
Reakcija epoksidov, vključno z etilen oksidom, z amini je osnova za pripravo čakalnih vrst ali dlesni paste. Ta lepila se uporabljajo za proizvodnjo zveze površin, pa tudi pri stabilizaciji PVC.
Etilen oksid reagira z natrijevim etoksidom, da nastane 2-toksietanol, znan tudi kot cellosolve. Ta kemična spojina raztopi olja, smole, maščobe, voske, nitrocelulozo in lake.
Epoksi smole
Epoksi ali epoksi smole imajo med svojimi lastnostmi, ko so ojačane, visoka kemična, toplotna in mehanska odpornost. Ti upori omogočajo njihovo uporabo za izdelavo lakas in emajlov, pa tudi za prevleko kovin in laboratorijskih nadstropij ter izdelavo električnih delov.
Nekatera podjetja uporabljajo te smole s polnili kremena, ki nadomeščajo porcelan za izdelavo izolatorjev električnih linij. Epoksidne smole se uporabljajo tudi za izdelavo listov za tiskana vezja in plošče, ojačane s steklenimi vlakni.
Epoksidne smole imajo malo uporabe ločeno, vključno z vinilno stabilnostjo. Da bi povečali svojo uporabnost, so navzkrižno povezani z več spojinami v procesu, znanem kot "ozdravljeni". Med agenti, ki se uporabljajo v ta namen, imamo: primarni, sekundarni, terciarni in poliamidi.
Epoksidi, pridobljeni iz rastlinskih olj, se uporabljajo za sintezo polio, ki se uporabljajo v poliuretanski industriji.
Medicinske uporabe
Epotilonas so presnovni proizvodi bakterij Sorangium celulosum, ki imajo lastnost stabilizacije mikrotubul in tako povzročajo blokiranje celičnega cikla.
Uporaba ixabepilona, epotilonas, je bila odobrena za zdravljenje napredovanja raka dojke. Prav tako smo pri zdravljenju Alzheimerjeve bolezni preučevali uporabo epotilona D.
Vam lahko služi: disulfrinska kislina: kaj je, struktura, lastnosti, uporabeDruge uporabe
Etilen oksid se vmeša v sintezo etilen glikola: spojina, ki se uporablja kot antifriz v hladilnih sistemih avtomobilov. Etilen oksid se uporablja tudi pri sterilizaciji medicinskih materialov in instrumentov.
Strupenost
Absorpcija skozi kožo, vdihavanje ali vnos epoksi je povezana s proizvodnjo strupenih učinkov, tako pri človeku kot pri eksperimentalnih živalih. Sem spadajo: draženje površinskih tkiv in preobčutljivost. Nastajajo tudi spremembe delovanja jeter, krvnih celic in kostnih mozga.
Prav tako so bili epoksidi z rakotvornostjo in mutagenostjo povezani z epoksidi. Eporoksidi so zaradi visoke elektrofilne reaktivnosti in značaja izposojenih spojin veljali za potencialna rakotvorna sredstva.
Primeri epoksije
Končno bodo navedeni še nekateri drugi primeri epoksijev:
-1,2-epoksipropan
-2,3-epoksiheksan
-1,2-epoksikloheksan
-Raztegnjen oksid
-Izobutilenski oksid
-3.4-epoksi-1-butno
Reference
- Graham Solomons t.W., Craig b. Fryhle. (2011). Organska kemija. (10th Izdaja.). Wiley Plus.
- Carey f. (2008). Organska kemija. (Šesta izdaja). MC Graw Hill.
- Morrison in Boyd. (1987). Organska kemija. (Peta izdaja). Addison-Wesley Iberoamericana.
- Wikipedija. (2020). Epoksid. Pridobljeno iz: v.Wikipedija.org
- Leroy g. Wade. (2020). Epoksid. Encyclopædia Britannica. Okrevano od: Britannica.com
- Manson m. M. (1980). Epoksidi: Ali obstaja težava z zdravjem ljudi? British Journal of Industrial Medicine, 37(4), 317–336. doi.org/10.1136/OEM.37.4.317
- Kemikalije. (s.F.). Primeri epoksije. Okrevano od: KEMIKI.mreža
- W.G. Lončar. (1963). Kemija in uporaba epoksidnih smol, pristajalna medicina, letnik 13, številka 1, april 1963, strani 42–47, doi.org/10.1093/OCCMED/13.1.42
- Molinero Muñoz, María in Fernández Arberas, Nerea. (2016). Epotylonas, alternativa na področju protitumorja. Computense Madrid University.
- Alejandro Aguirre f. & Lesly Espinoza B. (2018). Uporaba in uporaba epoksijev in sulfidov. Centralna univerza v Ekvadorju. Okreval od: akademija.Edu
- « Nitrate lastnosti, struktura, nomenklatura, usposabljanje
- Značilnosti reakcije Cannizzaro, mehanizmi, primeri »

