Enantiomeri
- 2465
- 298
- Miguel Gutmann DVM
Pojasnjujemo, kaj so enantiomeri in kiralnost, njihove lastnosti, nomenklatura in več primerov
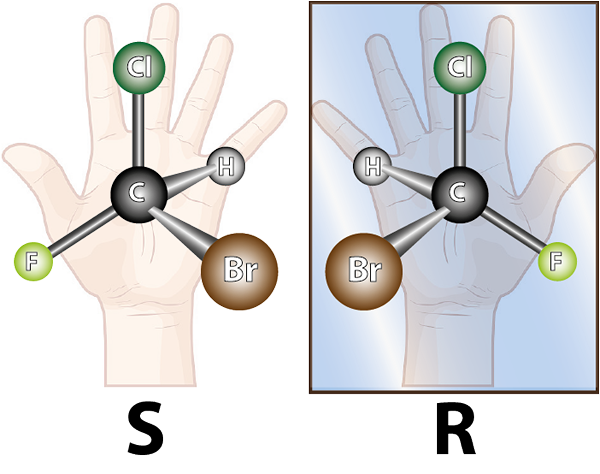
 Ti dve spojini sta enantiomeri, saj jih tvorijo isti atomi, združeni na enak način in sta spekularni podobi drug drugega
Ti dve spojini sta enantiomeri, saj jih tvorijo isti atomi, združeni na enak način in sta spekularni podobi drug drugega Kaj so enantiomeri?
The enantiomeri So pari spojin, ki medsebojno zrcalne slike ne prekrivajo. Ti pari spojin so posebna vrsta izomerov, to je različne spojine, ki imajo enako molekularno formulo.
Obstajajo različne vrste izomerov, med katerimi so stereozomeri, v katerih so vsi atomi združeni v istem vrstnem redu in z isto vrsto povezav, vendar imajo v prostoru različne usmeritve (stereo pomeni prostor).
Znotraj stereoizomerov najdemo enantiomere, katerih glavna značilnost je, da so med seboj spekularne slike.
Enantiomeri so po naravi zelo pogosti. Pravzaprav so skoraj vse organske spojine, prisotne v celicah vseh živih bitij, ena od dveh možnih enantiomerov.
Na primer, vse aminokisline, ki so del naravnih beljakovin, ustrezajo enantiomeru L ustrezne aminokisline (drugi izomer se identificira s črkam D).
Po drugi strani obstajajo tudi aktivne sestavine velike večine zdravil kot pari enantiomerov, od katerih je učinkovit le eden učinkovit. Težava pri ločevanju enantiomerov drug od drugega pomeni, da so tista zdravila, ki vsebujejo samo uporaben izomer, zelo draga.
Enantiomeri in kiralnost
Enantiomere tvorijo kiralne molekule. Kiralnost je lastnost, da se s svojo zrcalno podobo ne prekriva. Beseda kirala izvira iz grškega izraza, Kheir kar pomeni roko, če se spominjamo dejstva, da so roke tudi spekularne slike drug drugega in se ne morejo prekrivati.
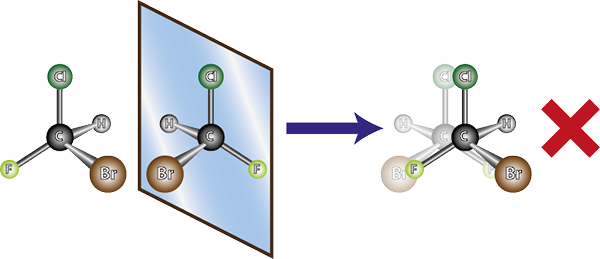 Molekula leve je kiralna, saj je pri primerjavi z zrcalno sliko videti, da se ne prekrivajo. Z drugimi besedami, ni mogoče zasukati ali obrniti tako, da se vsi atomi med seboj sovpadajo
Molekula leve je kiralna, saj je pri primerjavi z zrcalno sliko videti, da se ne prekrivajo. Z drugimi besedami, ni mogoče zasukati ali obrniti tako, da se vsi atomi med seboj sovpadajo Glede na zgoraj navedeno je mogoče ugotoviti, da mora biti za vsako kiralno molekulo še ena kiralna molekula, ki ni prekrivajoča se zrcalna slika, torej njegov enantiomer. Z drugimi besedami, kadar koli rečemo molekula.
Vam lahko služi: neodimij: struktura, lastnosti, uporabeKiralni centri
Številne kiralne spojine imajo eno ali več asimetričnih centrov, ki so odgovorni za kiralnost molekule. Temu se imenujejo kiralna središča in v mnogih organskih spojinah so sestavljeni iz ogljikovih atomov, ki so povezani s 4 atomi ali skupinami različnih atomov.
Posebna oblika, saj so te štiri skupine razporejene okoli asimetričnega ogljika, določa, kateri od obeh enantiomerov ustreza kiralni molekuli. Prisotnost enega samega Quiralnega centra zagotavlja, da je molekula kiralna, če pa jih je več, je lahko kiralna, saj morda ne.
Lastnosti Enontiomer
Večina fizikalnih in kemijskih lastnosti je enakih
Kot desna in leva roka, tudi enantiomeri prihajajo le v parih. Te spojine so med seboj praktično enake. Pravzaprav je večina njegovih fizikalnih in kemijskih lastnosti, kot so točka fuzije, vrenja, parni tlak in topnost v nekaterih topilih, med drugim enake.
Optična aktivnost
Vse kiralne spojine imajo edinstveno lastnost, ki jih razlikuje od tistih, ki niso: imajo možnost zasukanja ravnine polarizirane svetlobe. Ta lastnost se imenuje Optična aktivnost, In je ena redkih lastnosti, ki razlikuje kiralno spojino od svojega enantiomera.
Slednje je posledica dejstva, da je polarizirano svetlobno ravnino mogoče zasukati v eni od dveh smeri, bodisi v smeri uri igle (imenovanih dextrogyr in predstavljene s simbolom +) ali na uro igle (Levógiro, predstavljeno s simbol -).
Če se quiralna spojina vrti polarizirano svetlobno ravnino v eno smer, jo bo njegov enantiomer spremenil v nasprotno smer.
-
Primer
Raztopina D-glukoze vrti polarizirano svetlobno ravnino v smeri igle ure (na desni, dektrogiralna), medtem ko raztopina L-glikoze vrti v nasprotni smeri.
Lahko vam služi: Erlenmeyer Flask: Značilnosti, uporabe, metode uporabeDiferencialna reaktivnost
Druga lastnost, ki omogoča razlikovanje enega enantióna od drugega, je njegova reaktivnost proti drugim kiralnim spojinam.
Diferencialno reaktivnost je mogoče primerjati z načinom, kako rokavica izgleda samo na eni strani, ne pa tudi druge ali kot desni čevelj se dobro prilega desni nogi, ne pa na levo.
Pomembna posledica diferencialne reaktivnosti so različni učinki, ki lahko povzročijo dva enantiomera nekaterih zdravil. Te razlike so lahko neškodljive, lahko pa so tudi zelo nevarne.
-
Primeri
- Od obeh enantimerov Aspartama (ki je umetno sladilo), je eden sladka, druga pa nima okusa.
- Samo enantiomer s omeprazola je učinkovit kot želodčni zaščitnik, drugi pa ne daje nobenega učinka.
- D-penicilamin je zdravilo proti revmatoidnemu artritisu, njegov enantiomer, L-penicilamin pa je nevaren strup.
Diferencialna absorpcija
Enantiomeri se razlikujejo tudi v načinu, kako se absorbirajo v smolah ali trdnih snovi, ki so tudi kirali. Mešanico enantiomerov lahko ločimo, če jo prenesemo skozi stolpec kiralne ločitve, saj bo eden od obeh enantiomerov absorbiran močneje kot drugi.
Nomenklatura enantiomerov
Obstaja več metod za prepoznavanje enega ali drugega enantiomera, najbolj uporabljen pa je sistem Cahn-Ingold-Prelog (CIP). To je sestavljeno iz naslednjih korakov:
- Nivo hierarhije je dodeljena štirim skupinam, pritrjenim na vsak kiralni center. Prioriteta skupin je dodeljena glede na atomsko število atoma, ki je neposredno povezan s Quiralnim centrom. Če obstajata dva enaka atoma, se dodajo atomske številke atomov, ki so povezani s prvim, da dodamo atomske številke.
- Smer, v kateri se trije prednostni skupini prevozijo, ko določijo točke najnižje prednostne točke nazaj.
- Če je smer poti v smeri rok ure, je dodeljena konfiguracija R, V nasprotnem primeru je dodeljena konfiguracija S.
Primer
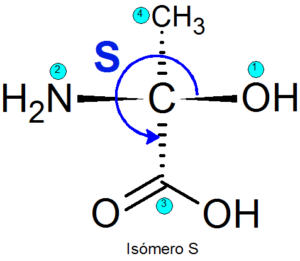
Primeri enantiomerov
D-gliceraldehid in L-gliceraldehid
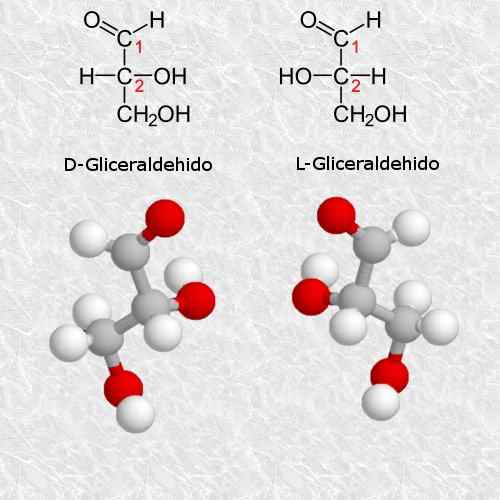
Gliceraldehid je najpreprostejši in najbolj majhen quiralni ogljikovi hidrat, ki obstaja, in je zelo pomemben za kemijo in biologijo.
V skladu s pravili sistema Cahn-Ingold-Prelog, D izomer ustreza izomeru (R) in L izomer ustreza (S) (S).
D-Alanina in L-Alanina
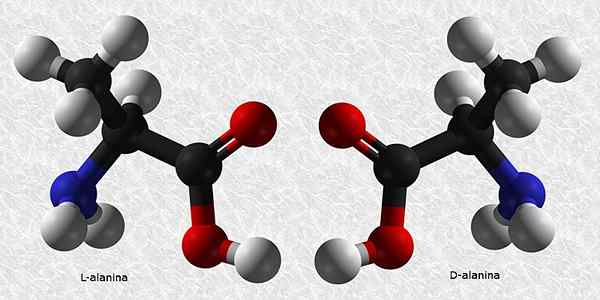
Alanin je ena od bistvenih aminokislin za gradnjo beljakovin. Kot skoraj vse aminokisline ima tudi kiralni ogljik, tako da ima dva enantiomera:
Od teh dveh je L-Alanina najpogostejša in je prisotna pri vseh živih bitjih, D-Alanina.
D-Tartarična in L-Tartarična kislina
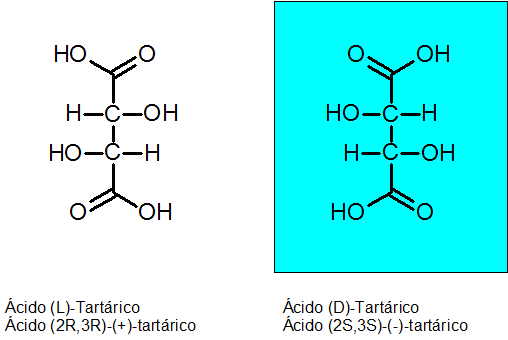
Kiralnost je Louis Pasteur odkril leta 1848 po zaslugi Tartarne kisline. Ta spojina ima 2 asimetrična karbona in lahko obstajata kot dva enantiomera in tretji izomer, ki se imenuje Meso Compion.
Absolutna konfiguracija dveh kiralnih ogljikov je R za Enantiómero Levógiro in S za dektrogyan enantiom.
2-butanol
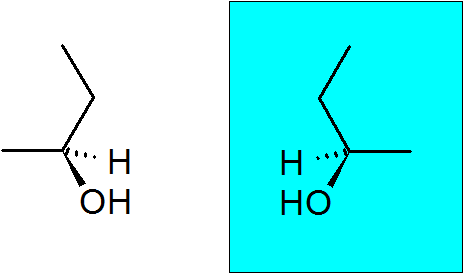
Ta alkohol ima tudi Quiralni ogljik, zaradi česar ima ta spojina dva enantiomera.
Bromokloroetan
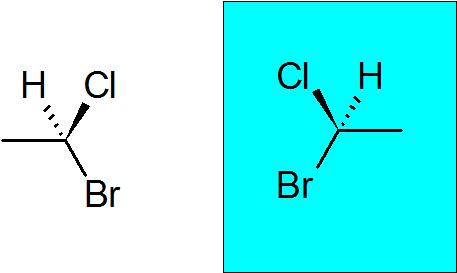
To je zelo preprosta kiralna spojina z le dvema ogljikoma. Quiral Carbon se je pridružil bromutu, kloru, metilu in vodiku.
Reference
- Kiralnost (kemija). (18. marec 2021) na Wikipediji.com
- Carey, f. Do. (2008). Organska kemija. Boston: visokošolsko šolstvo McGraw-Hill.
- Smith, m., Marec, j., & Marec, j. (2001). Marchova napredna organska kemija: reakcije, mehanizmi in spodbuda. New York: Wiley.
- M.H. Hyun (2012). 8.13 kromatografske ločitve in analiza: kiralne stacionarne faze na kiralni kroni na osnovi kiralne krone. Urednik: Erick M. Carreira, Hisashi Yamamoto. Razumevanje kiralnosti. Elsevier. Strani 263-285. ISBN 9780080951683,
- Nguyen, l. Do., On, h., & Pham-huy, c. (2006). Kiralna zdravila: pregled. International Journal of Biomedical Science: IJBS, 2(2), 85-100.

