Diastreomeres
- 3140
- 378
- Lee Farrell
Pojasnjujemo, kakšni so diastomeri, kako so prepoznane njihove lastnosti, nomenklatura in več primerov,
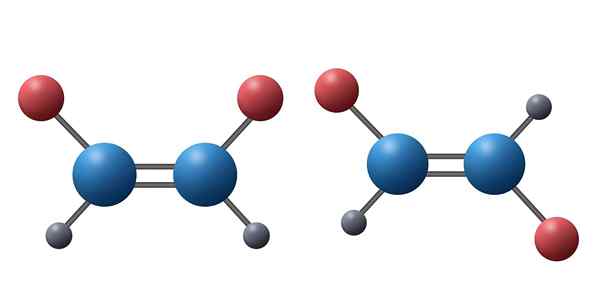
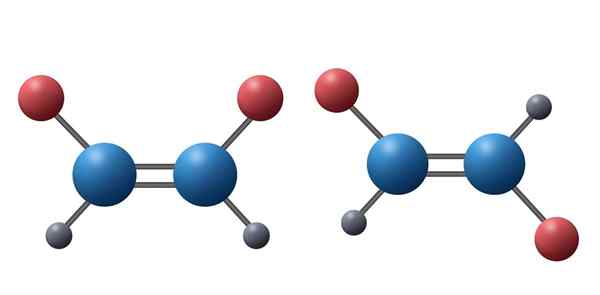 Ta dva alkena sta primer diastereomerov. Tu je razvidno, da so vsi atomi obeh molekul združeni v istem zaporedju in skozi iste vrste povezav. Vendar so v prvi spojini rdeči atomi na isti strani, medtem ko v drugi spojini kažejo v nasprotne smeri. Jasno je, da nobena od njih ni zrcalna podoba drugega
Ta dva alkena sta primer diastereomerov. Tu je razvidno, da so vsi atomi obeh molekul združeni v istem zaporedju in skozi iste vrste povezav. Vendar so v prvi spojini rdeči atomi na isti strani, medtem ko v drugi spojini kažejo v nasprotne smeri. Jasno je, da nobena od njih ni zrcalna podoba drugega Kaj so diamireomeri?
The Diastreomeres, Imenujejo se tudi Diametereoisomeres, opredeljeni so kot stereoizomeri, ki med seboj niso zrcalne slike. So posebna vrsta izomerov, kar pomeni, da gre za različne spojine, ki imajo isto molekularno formulo.
Obstajajo različne vrste izomerov, med katerimi so stereoizomeri. To so tisti, v katerih so vsi atomi združeni v istem vrstnem redu in z isto vrsto povezav, vendar imajo v prostoru različne usmeritve (stereo pomeni prostor). Znotraj stereoizomerov najdemo diamireomere, za katere je značilno, da se med seboj ne zrcalijo slike.
Z drugimi besedami, diamereomeri so Stereoizomeri to Niso enantiomeri drug z drugim.
Obstajajo različne vrste diastomera.
Kako prepoznate diamireomere?
Da bi prepoznali diastomere, najprej ugotovimo, ali gre za cis-trans izomere ali so izomerji E-Z. Če se to zgodi, potem so diastereomeri. V nasprotnem primeru se upoštevajo naslednja pravila:
- Morajo biti stereoizomeri, to je, da se morajo razlikovati le v prostorski orientaciji svojih atomov.
- Imeti morajo dva ali več kiralnih centrov.
- Imeti morajo enako konfiguracijo v vsaj enem od svojih kiralnih centrov.
- V vsaj enem od njihovih kiraralnih središč morajo imeti nasprotno konfiguracijo.
Vsak par izomerov, ki ustrezajo te značilnosti, bo nekaj diastereomerjev.
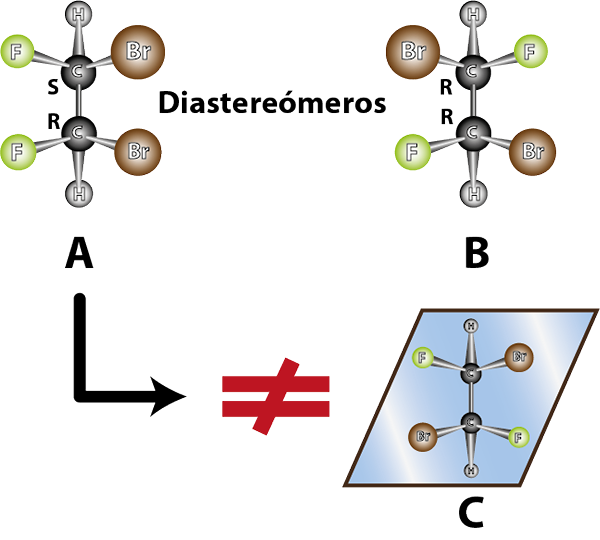 Spojine A in B sta diastomera. Poleg tega A in B nista zrcalne slike
Spojine A in B sta diastomera. Poleg tega A in B nista zrcalne slike Lastnosti diastreomerov
Njegove fizikalne in kemijske lastnosti so različne
Za razliko od enantiomerov, ki imajo isto vrelišče, fuzijo itd., Diastreomeres so precej različne spojine in imajo lahko zelo različne fizikalne in kemijske lastnosti.
Skoraj vedno imajo razlike v svoji polarnosti, v parni tlaki, v vreliščih in fuzijskih točkah ter celo v topnosti v različnih topilih.
Razlike v njihovih fizikalnih in kemičnih lastnostih omogočajo.
Lahko ali morda
Lahko je več dni iste spojine, nekateri pa so lahko kirali, drugi pa ne, odvisno od tega, ali ima molekula neko vrsto simetrije ali ne.
Dejstvo, da imajo kiralna središča, ne zagotavlja, da je molekula Quiralna. Nekatere spojine s kiralnimi središči so lahko simetrične, zato jih bodo s svojo zrcalno podobo nadrejene in zato ne bodo kirali. V teh primerih se imenujejo Mezo spojina.
-
Primer:
Naslednja slika prikazuje dva diamireomera tartarne kisline. Diastreomero A ni kiralna, saj je simetrična molekula (polovica od zgoraj je odsev spodaj). Vendar diamereomer B, če je kiralno.
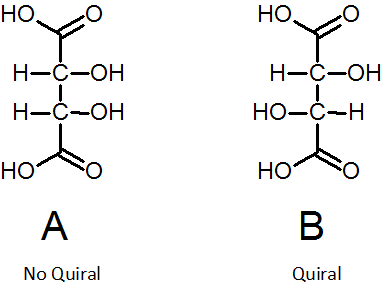
Na prejšnji sliki je Isomer A primer spojine MESO.
Lahko so cis-trans in e-z izomerji
CIS in trans izomeri, pa tudi E-Z izomeri alkena ali nadomeščenega cikla, so stereozomeri, ki med seboj niso zrcali, zato so tudi diastereomeresi.
Vam lahko služi: heksokinaza: strukture, funkcije, oblikeOptična aktivnost
Tisti diastomeri, ki imajo kiraralna središča, vendar niso MESO spojine, bodo kiralne spojine in bodo zato optično aktivne. To pomeni, da lahko vrtijo ravnino polarizirane svetlobe.
Nomenklatura diamireomerov
Nomenklatura diamireomerjev, ki imajo kiralna središča (tiste, ki niso cis-trans ali e-Z), temelji na sistematičnem imenu spojine IUPAC, pred katerim je absolutna konfiguracija vsakega kiralnega središča v vrstnem redu, v katerem se pojavijo v glavnem veriga.
Obstaja več metod za prepoznavanje enega ali drugega diastereomera, najbolj uporabljen pa je sistem Cahn-Ingold-Prelog (CIP). To je sestavljeno iz naslednjih korakov:
- Nivo hierarhije je dodeljena štirim skupinam, pritrjenim na vsak kiralni center. Prioriteta skupin je dodeljena glede na atomsko število atoma, ki je neposredno povezan s Quiralnim centrom. Če obstajata dva enaka atoma, se dodajo atomske številke atomov, ki so povezani s prvim, da dodamo atomske številke.
- Smer, v kateri se trije prednostni skupini prevozijo, ko določijo točke najnižje prednostne točke nazaj.
- Če je smer poti v smeri rok ure, je dodeljena konfiguracija r, sicer je konfiguracija S dodeljena.
Primer
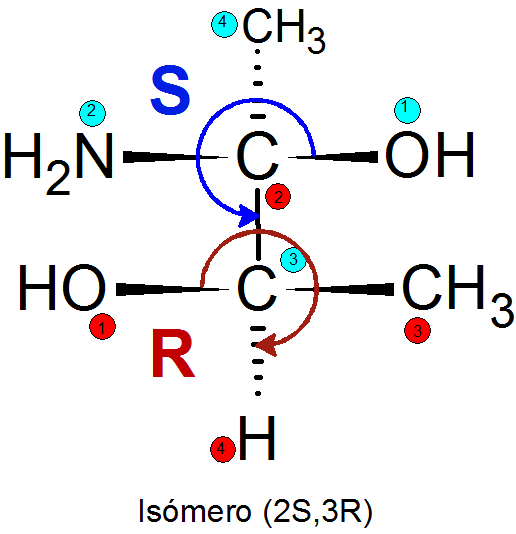
Primeri skupnih diamereomerov
Primeri dneva ogljikovih hidratov
Diastreomeres so po naravi zelo pogosti, zlasti v bioloških pomenskih spojinah. Nato so različni dnevi treh pomembnih skupin sladkorjev predstavljeni kot primeri:
-
Diastreomeri La Ribosa
Ribosa je eden najpomembnejših ogljikovih hidratov v naravi, saj je del DNK in RNA, ki tvorijo naš genetski material. Ta ogljikovi hidrat ima tri kiralna središča, ki povzročajo osem različnih izomerov. Nato so predstavljeni 4 najpomembnejši diasterji tega sladkorja:
Vam lahko služi: prenasičena rešitev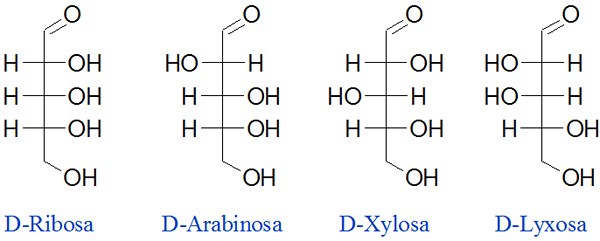
Fruktozni diastereomeri
Kot že ime pove, je fruktoza sladkor, ki ga najdemo v sadju, in ima tri kiralna središča, ki naslednje dni povzročijo
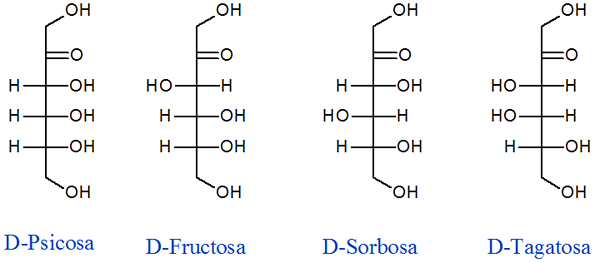
Glukozni diastereomeri
Glukoza je najpogostejši ogljik, ki obstaja in je ena najpogostejših bioloških molekul po vsej Zemlji. Skupaj je 16 izomerov, od tega je le 8 prisotnih pri večini živih bitij. Ostalih 8 je prisotnih le v nekaterih celicah. Spodaj je 8 najpogostejših diastomerov:
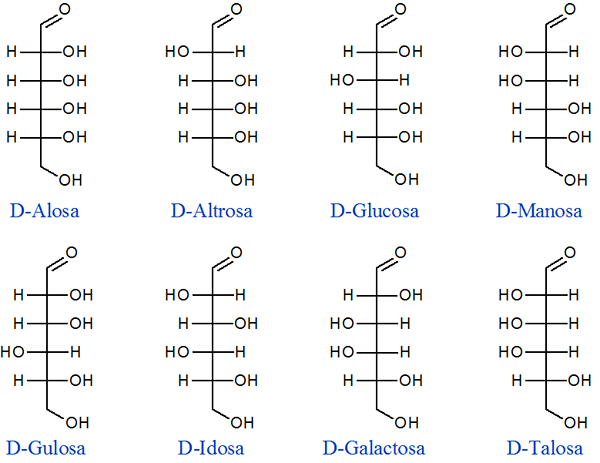
Lahko opazimo, da se pri primerjavi katerega koli para diastomerov razlikujejo po konfiguraciji vsaj enega kiralnega ogljika in delijo konfiguracijo vsaj enega kiralnega ogljika.
Primer diastereomerov cis-trans
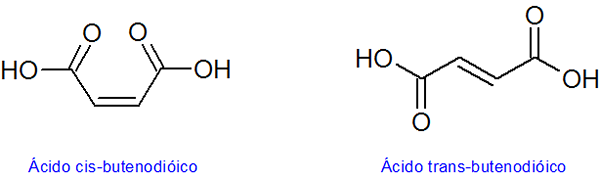
Primer diastereomerjev E-Z
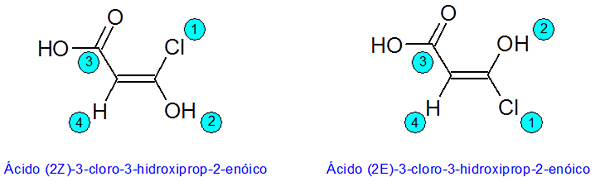
V tem primeru prikazane številke ustrezajo prednosti substituentov po pravilih sistema CIP.
Reference
- Carey f. (2008). Organska kemija. (6. izd.). MC Graw Hill.
- Diastereomer. (2021). Merriam-Webster.Com Slovar, Merriam-Webster, Merriam-Webster.com
- Graham Solomons t.W., Craig b. Fryhle. (2011). Organska kemija. (10. izd.). Wiley Plus.
- Monosaharid. (16. februar 2021). V Wikipediji.org.
- Nelson, d. L., & Cox, m. M. (2017). Lehningerjeva načela biokemije (7. izd.). W.H. Freeman.

