Struktura sulfanilne kisline, lastnosti, sinteza, uporablja
- 2548
- 764
- Dexter Koch
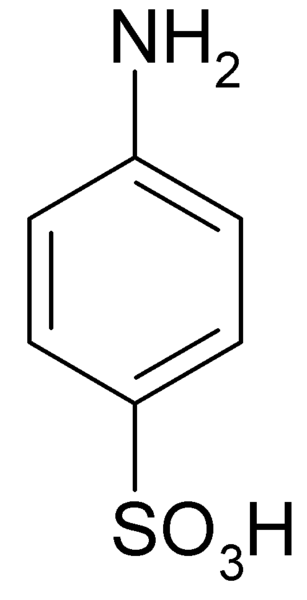
On Sulfanilna kislina Gre za kristalno spojino, katere molekulo tvori benzenski obroč, na katerega je hkrati združena osnovna skupina (-NH2) in kislinsko skupino (-SO3H). Njegova kemična formula je NH2C6H4SW3H.
Znan je tudi kot 4-aminobencenosulfonska kislina. Pripravimo ga s sulfonacijo anilina v položaju za. Njegovi kristali so beli ali beli-ugoni. Njegovo vedenje je bolj podobno soli kot pri organski spojini z NH2 medved3H. Zato je v večini organskih topil netopna.
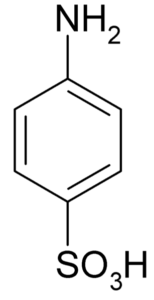 Molekularna formula sulfanilne kisline ali 4-aminobenzeulfonske kisline. Klaus Hoffmeier [javna domena]. Vir: Wikipedia kot ZDA
Molekularna formula sulfanilne kisline ali 4-aminobenzeulfonske kisline. Klaus Hoffmeier [javna domena]. Vir: Wikipedia kot ZDA Ena od njegovih glavnih uporabe je v sintezi barvil, saj zlahka tvori diazokmorano, ki je surovina za to aplikacijo.
Kot antibakterijska sredstva so bili uporabljeni tako sulfanilna kislina kot njeni derivati. Uporablja se v sintezi mukoliznih spojin, saj imajo sposobnost zmanjšanja viskoznosti sluzi ali zelo viskoznih bioloških tekočin.
Uporablja se tudi v papirni industriji in v formulah za gravure ali litografije. To je del smole, ki se uporabljajo v betonskih mešanicah ali maltah, da jim omogočajo dolgo časa ohranjanje pretočnosti, ne da bi vplivali na končni čas nastavitve.
To je ksenobiotski presnovek, to pomeni, da ga živa bitja ne proizvajajo naravno. To je dražilna koža, oči in sluznico. Poleg tega lahko kontaminirate okolje.
[TOC]
Struktura
Sulfanilna kislina ima bele kristale, ki jih tvorijo ortorrombični ali monoklinični listi. Njegova monohidrat kristalizira v vodi v obliki ortorambičnih listov. Če se kristalizacija izvaja zelo počasi, kristalizira dihidrat. Monohidrat postane brezvodni, ko je približno 100 ° C.
Nomenklatura
- Sulfanilna kislina.
- P-Amynobencenosulfonska kislina.
- 4-amibonzefonska kislina.
Lastnosti
Fizično stanje
Bela ali bela kristalna trdna.
Molekularna teža
173,19 g/mol.
Tališče
Se pokvari na približno 288 ° C, ne da bi se talil. Poroča se tudi na> 320 ° C.
Gostota
1,49 g/cm3
Topnost
Skoraj netopna v vodi: 10,68 g/l pri 20 ° C.
Netopna v etanolu, benzenu in etru. Rahlo topen v vročem metanolu.
Topno v vodnih osnovnih raztopinah. Netopne v vodnih raztopinah mineralne kisline. Topno v koncentrirani klorovodiki.
Kemične lastnosti
Njegove lastnosti se razlikujejo od lastnosti drugih aminskih ali sulfoniranih spojin, podobne lastnosti soli. To je zato, ker njegova struktura vsebuje skupine -nh3+ In tako3-, Kaj daje značilnosti dipolnega iona.
Vam lahko služi: prenasičena rešitevVsebuje kislinsko skupino in osnovno skupino v nasprotnih polov iste molekule. Toda vodikov ion je povezan z dušikom namesto s kisikom, ker skupina -NH2 Je močnejša podlaga kot skupina3-.
Ker je dipolni ion, predstavlja visoko točko združitve in netopnosti v organskih topilih.
Sulfanilna kislina je topna v alkalni raztopini, ker OH hidroksid ion-, Ker je močno osnovna, se začne vodikov ion (h+) šibke osnovne skupine -n2, tvori p-aminobencenosulfonat ion, ki je topen v vodi.
V kislinski raztopini se struktura sulfanilne kisline ne spreminja, zato ostaja netopna.
Druge lastnosti
Ko se segreje na njegovo razgradnjo, oddaja strupene hlape dušika in žveplovih oksidov.
Izpostavljenost sulfanilne kisline lahko privede do simptomov, kot so draženje kože, oči in sluznice. Je jedko spojino.
Sinteza
Pripravimo ga tako, da reagira anilin z žveplovo kislino (h2SW4) pri visokih temperaturah. Na začetku nastane anilinska kislina sulfatna sol, ki se pri segrevanju pri 180-200 ° C reorganizira, da tvori obroč, ki je zamenjan v položaju, ker je najbolj stabilen izdelek.
Za pripravo z visoko stopnjo čistosti se s H izvede sulfoniranje mešanice anilina in sulfolano2SW4 pri 180-190 ° C.
Prijave
V barvni industriji
Sulfanilna kislina se uporablja pri sintezi ali pripravi več barvil, kot sta metilna pomaranča in tartrazin. Za to je diazotizirana, ki ustvarja diazotizirano sulfanilno kislino.
Pomembno je poudariti, da je bil tartrazin uporabljen kot barvanje v hrani. Ko pa ga zaužijemo, ustvari nekatere presnovke v človeškem organizmu, vključno s sulfanilno kislino, ki so možni odgovorni za nastajanje reaktivnih kisikovih vrst. Te lahko vplivajo na ledvične (ledvice) ali jetrna tkiva (jetra).
 Karamele z rumenim barvilom. David Adam KESS [CC BY-SA 4.0 (https: // creativeCommons.Org/licence/by-sa/4.0)]. Vir: Wikipedia Commons
Karamele z rumenim barvilom. David Adam KESS [CC BY-SA 4.0 (https: // creativeCommons.Org/licence/by-sa/4.0)]. Vir: Wikipedia Commons V analitični kemiji
Uporablja se kot reagent pri določanju več kemičnih spojin, vključno z nitriji.
V medicini kot antibakterijsko sredstvo
Sulfanilamid, pridobljen iz sulfanilne kisline, ima v farmacevtski industriji nanese, ker ima protibakterijsko aktivnost.
V človeškem telesu ga bakterije zmedejo s p-aminobenzojsko kislino, ki je bistveni presnovek. Ta nadomestitev povzroča, da se bakterije ne reproducirajo in umrejo.
Vam lahko služi: vodik: zgodovina, struktura, lastnosti in uporabe Bakterija. Slika Raman Oza. Vir: Pixabay
Bakterija. Slika Raman Oza. Vir: Pixabay Druga izhaja iz sulfanilne kisline, pridobljene s kondenzacijo z drugimi spojinami, ima tudi antibakterijske lastnosti, ki temeljijo na njegovi sposobnosti izpodrivanja folne kisline (člani vitaminskega kompleksa B).
To spojino lahko jemljete peroralno, intravensko vbrizgate ali nanesemo zunaj v mazilo.
V medicini kot mukolitični sredstvo
Uporabljen je derivat sulfanilne kisline, ki ima mukolitično aktivnost. To je, da predstavlja aktivnost sluzi Licuefactiva, da se raztopi sluz ali zelo viskozne biološke tekočine.
Spojina se lahko uporablja za proizvodnjo sluzi, ki jo proizvaja tkivo zaradi patoloških pogojev. Na primer zastoje dihalnega sistema ali tistega iz vaginalnega trakta.
Ko gre za utekočinjenost sluzi v dihalnem traktu, izdelek dajemo z vdihavanjem, pade v nos, roso, aerosole ali nebulizarje. Gre za zdravljenje, ki se uporablja za človeka ali sesalce. Je močnejša spojina kot na osnovi cisteina.
 Uporaba nosnih kapljic za mraz. Slika Thorsten Frenzel. Vir: Pixabay
Uporaba nosnih kapljic za mraz. Slika Thorsten Frenzel. Vir: Pixabay Uporablja se tudi v laboratoriju, ko je zaželeno zmanjšati viskoznost bioloških tekočin, da bi olajšali analitične določitve.
V bioanalizi laboratorijev
Diazotizirana sulfanilna kislina (derivat, ki ga pripravimo z reakcijo sulfanilne kisline z natrijevim nitritom), se uporablja pri določanju bilirubina.
Bilirubin je rumeni pigment, ki ga najdemo v žolču. Presežek krvnega bilirubina je posledica jetrnih bolezni, hematoloških motenj (ali krvi) ali motenj v žolku.
Za merjenje količine bilirubina v krvi se dializa, pridobljena iz sulfanilne kisline z bilirubinom. Na ta način je vsebnost bilirubina v krvi določena v krvi.
V papirni industriji
Sulfanilna kislina vam omogoča sintezo poliranja papirja, to je spojino, ki zagotavlja optično svetlost ali beli videz, saj nevtralizira rumeno barvo naravnega ali netrganega papirja.
 Beli papirni zvezek. Vir: Pexels
Beli papirni zvezek. Vir: Pexels Prednost ima pred drugimi spojinami, saj ga je mogoče uporabiti v razmeroma visokih koncentracijah za zdravljenje papirnate kaše v pogojih z nizkim pH, ne da bi povečali papirno rumeno.
Vam lahko služi: amonijev sulfatRezultat je razviden, ko papir opazimo z UV svetlobo (ultravijolična.
V vodi je zelo topen, kar omogoča uporabo v bolj koncentriranih rešitvah. Uporablja se lahko v kateri koli vrsti papirja, vključno s papirjem, proizvedenim z ozemljitvijo lesene celuloze, sulfitne kaše ali katerega koli drugega postopka.
V vtisih, gravuri ali litografih
Sulfanilna kislina deluje kot zakisanje v koncentriranih raztopinah za litografijo, ne da bi predstavljali težave drugih kislin, kot je fosfor, manj strupene in manj onesnažujoče kot slednje.
V gradbenih materialih
Vodne raztopine melamina-formaldehidne smole, spremenjene s sulfanilno kislino. Namen je bil zmanjšati vsebnost vode in preprečiti zmanjšanje pretočnosti mešanice s časom, ne da bi se čas nastavitve zmanjšal.
Beton ali malta, pripravljena s temi rešitvami, je zelo učinkovita poleti, ko zmanjšanje tekočega sčasoma predstavlja težavo.
Če je malta ali beton pripravljen s temi rešitvami in iz kakršnega koli razloga mora biti dovoljen počivati, lahko cementno sestavo zlahka izpustimo v kalupe ali podobno, saj sčasoma ni izgubil tekočega časa.
 Betonski izcedek. Igor slika Ovsyannykov. Vir: Pixabay
Betonski izcedek. Igor slika Ovsyannykov. Vir: Pixabay Reference
- Windholz, m. et al. (uredniki) (1983). Indeks Merck. Enciklopedija kemikalij, drog in bioloških snovi. Deseta izdaja. Merck & co., Inc.
- Kirk-Othmer (1994). Enciklopedija kemijske tehnologije. Zvezek 2. Četrta izdaja. John Wiley & Sons.
- Nacionalna knjižnica medicine. (2019). Sulfanilna kislina. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Urist, h. in Martin, g.J. (1950). Derivati sulfanilne kisline. ZDA patent št. 2,504,471. Dodelitve nacionalnemu podjetju za droge. 18. aprila 1950.
- Villaume, Frederick G. (1964). Svetleča sestava za papir, ki je bila izvedena iz metanilne in sulfanilne kisline. ZDA patent št. 3,132,106. 5. maja 1964.
- Martin, Tellis a. In jej, William T. (1979). Derivat benzojske kisline in sluznic benzenesulfonske kisline. ZDA patent št. 4.132.802. 2. januar 1979.
- Druker, l.J. in Kincaid, r.B. (1979). Koncentrat litografskega vodnjaka. ZDA patent št. 4.150.996. 24. aprila 1979.
- SHULL, BRUCE C. (1983). Analiza bilirubina. ZDA patent št. 4.404.286. 13. septembra 1983.
- Uchida, j. et al. (2001). Postopek za pripravo vodne raztopine sulfanilne kisline, spremenjene z melamin-formaldehidnim smolo in cementno sestavo. ZDA patent št. 6.214.965 B1. 10. april 2001.
- Corradini, m.G. (2019). Zvezek 1. V enciklopediji kemije hrane. Okrevano od Scientirect.com.

