Kemična struktura, lastnosti, nomenklatura Cycloalquenos
- 2512
- 605
- Ms. Pablo Lebsack
The Kolesarjenje Spadajo v skupino binarnih organskih spojin; to pomeni, da jih sestavljajo le ogljik in vodik. "Jezen" odpoved kaže, da v svoji strukturi predstavljajo dvojno vez, imenovano nenasičenost ali pomanjkanje vodika (kaže, da v formuli manjkajo vodiki).
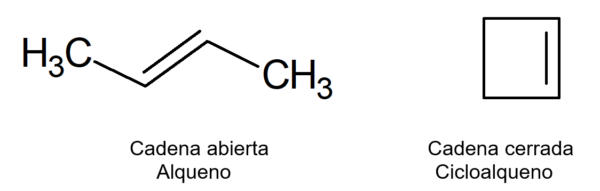
So del nenasičenih linearnih verižnih organskih spojin, imenovanih alkeni ali olefini, ker imajo mastno (mastno) videz, razlika pa je v tem, da imajo cikli zaprte verige, ki tvorijo cikle ali obroče ali obroče.
 Cycropropeno, vrsta cikloalkena
Cycropropeno, vrsta cikloalkena Tako kot v alkenih, dvojna vez ustreza σ (visoko energijsko sigma) in π (manjša energija pi) vez (manjša energija). Prav ta zadnja povezava omogoča, da se pojavi reaktivnost, da se njegova enostavnost zlomi in oblikuje proste radikale.

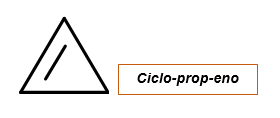
Imajo splošno formulo, ki se pojavi CnH2N-2 . V tej formuli n označuje količino ogljikovih atomov, ki jih ima struktura. Najmanjši cikel je ciklopropen, pomeni, da ima samo 3 ogljikove atome in eno samo dvojno vez.
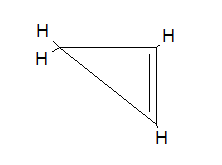
Če želite pridobiti strukturo s številnimi atomi ogljika = 3 Uporaba formule CnHN-2 Preprosto zamenjajte n Do 3, pridobivanje naslednje molekularne formule:
C3H2 (3) -2 = C3H6-2 = C3H4.
Potem je na voljo cikel s 3 ogljikovimi atomi in 4 vodiki, ki je enak temu, kako se pojavlja na sliki.
Te kemijske spojine so zelo koristne na industrijski ravni zaradi svoje enostavnosti oblikovanja novih snovi, kot so polimeri (zaradi prisotnosti dvojne vezi) ali pridobivanja cikloalkanov z enakim številom ogljikovih atomov, ki so predhodniki za nastanek druge spojine.
[TOC]
Kemična struktura ciklov
Cikloalki lahko v svoji strukturi predstavljajo eno ali več dvojnih vezi, ki jih je treba ločiti s preprosto povezavo; To je znano kot konjugirana struktura. V nasprotnem primeru se med njimi ustvarijo odbojne sile, ki povzročajo lomljenje molekule.
Lahko vam služi: transerifikacija: mehanizem, v maščobnih kislinah, v mikroalgah, uporabljaČe ima v kemični strukturi cikloalque dve dvojni vezi, je rečeno, da gre za "diena". Če imate tri dvojne vezi, je to "trieno". In če obstajajo štiri dvojne povezave, se govori o "tetranu" in tako naprej.
Najbolj stabilne strukture v svojem ciklu nimajo veliko dvojnih vezi, ker je molekularna struktura izkrivljena zaradi velike količine energije, ki jo povzročajo gibljivi elektroni, ki jih najdemo v njem.
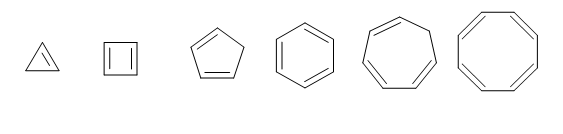
Eden najpomembnejših trienosov je cikloheksatrien, spojina, ki ima šest ogljikovih atomov in tri dvojne vezi. Ta spojina spada v skupino elementov, imenovanih pesek ali aromatična. Takšen je primer naftalena, fenantren in antraceno.
Nomenklatura
Za imenovanje ciklov je treba norme upoštevati v skladu z Mednarodno unijo čiste in uporabne kemije (IUPAC):
Cikloalken z eno samo dvojno vezjo in brez alkičnih ali radikalnih substituentov
- Število ogljika, ki se šteje cikel.
- Beseda "cikel" je zapisana, sledi korenino, ki ustreza številu ogljikovih atomov (Met, ET, rep, vendar, med drugim, je dodeljena "jeza", ker ustreza alkenu.
Cikloalki z dvema ali več dvojnimi vezmi in brez alkičnih ali radikalnih substituentov
Ogljikova veriga je navedena tako, da so dvojne vezi nameščene med dvema zaporednima številkama z najmanj možno vrednostjo.
Številke so napisane ločene z vejicami. Ko je oštevilčenje končano, se zapiše skript za ločitev številk od črk.
Beseda "cikel je nato napisan", sledi koren, ki ustreza številu atomov karbonov, ki jih ima struktura. Pismo "A" je zapisano in nato se napisano število dvojnih vezi z uporabo predpone di (dva), tri (tri), tetra (štiri), penta (pet) in tako naprej. Konča se s pripono "jezno".
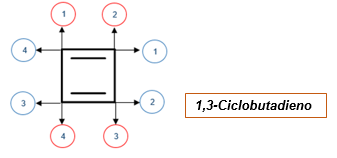
Lahko vam služi: piperidin: struktura, sinteza, derivati, reakcijeV naslednjem primeru sta prikazani dve našteti: ena zaklenjena v rdeči krog in druga zaklenjena v modri krog.
Oštevilčenje rdečega kroga kaže pravilen obrazec v skladu s standardi IUPAC, medtem ko tisti, zaprti v modrem krogu.
Cikel
Z alkičnim substituentom
Cikel je naveden, kot je že omenjeno. Radikalni propad je napisan s oštevilčenjem, ki ustreza in ločuje scenarij imena glavne verige:
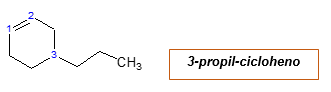 Z dvema alkiličnimi substituent
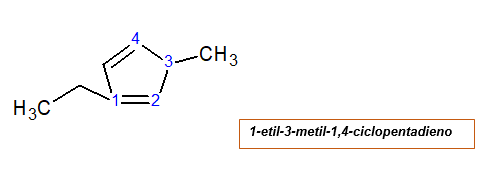
Z dvema alkiličnimi substituent
Oštevilčenje se začne z ogljikom, ki ga ima eden od radikalov. To daje najmanjšo možno vrednost, radikalno in dvojno vez. Radikali so poimenovani po abecednem vrstnem redu.
Lastnosti cikloalk
Fizične lastnosti
Fizikalne lastnosti cikloala, ki so odvisne od molekulske mase, količine dvojnih vezi, ki jih ima, in radikalov, ki so združeni z njimi.
Fizično stanje prvih dveh ciklov (c3 in c4) So plini, do c10 So tekoči in od takrat naprej so trdni.
Vrelišča cikloalquenosa je večja v primerjavi s cikloalkanosom istega števila ogljikovih atomov. To je posledica elektronske gostote, ki jo povzročajo π (PI) vezi dvojne vezi, medtem ko se tališče zmanjšuje.
Gostota se povečuje, ko se molarna teža ciklične spojine poveča in se lahko poveča, ko se dvojne vezi povečujejo.
Za kolesarjenje je gostota 0,744 g/ml, medtem ko je za ciklopentadien gostota 0,789 g/ml.
Vam lahko služi: heterogene mešaniceV obeh spojinah je enako število ogljikovih atomov; Vendar ima Cyclopentadieno manjšo molsko težo zaradi odsotnosti vodikov, vendar ima dve dvojni vezi. Zaradi tega je njegova gostota nekoliko večja.
Cikloalki niso zelo topni v vodi, še posebej zato, ker je njihova polarnost zelo nizka v primerjavi z vodo.
So topni v organskih spojinah in tako izpolnjujejo načelo, ki kaže, da je "podobno raztopljen". To na splošno pomeni, da so snovi, ki imajo podobno medmolekularno strukturo in sile, medsebojno bolj mešane od tistih, ki niso.
Kemične lastnosti
Tako kot alkeni linearne verige imajo tudi cikloalki dodane reakcije na dvojni vezi, da imajo večjo energijo in manjšo dolžino kot preprosta ali sigma (σ) vez (σ).
Glavne reakcije cikloala, ki so dodajanje, hkrati pa kažejo tudi oksidacije, redukcije in halogenacijske reakcije.
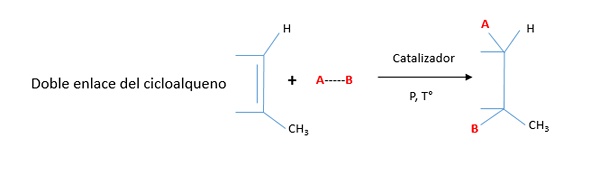
Naslednja tabela prikazuje najpomembnejše reakcije cikloral:
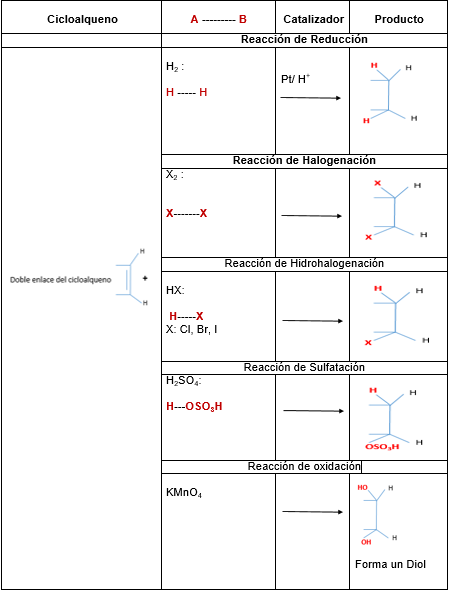
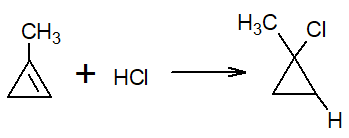
Če enega od ogljikov, ki ima dvojno vez, nadomesti z radikalom, se vodik iz reagenta veže na ogljik, ki ima največje število vodikovih atomov. Temu se imenuje Markovnicovo pravilo.
Primeri kolesarjenja
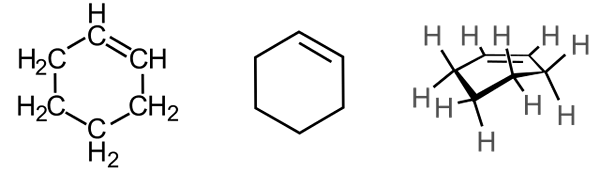 Cikloheksen
Cikloheksen - Cyclohexen: C6H10.
- Ciklobuteno: C4H6.
- Kolesarjenje: C5H8.
- 1.5-ciklooktadieno: C8H12.
- 1.3-ciklobutadieno: C4H4.
- 1.3-ciklopentadieno: C5H6.
- 1,3,5,7-ciklooktaterano: C8H8.
- Cicropropeno.
- Ciklohepteno.
Reference
- Tierney, J, (1988, 12), Markownikoffovo pravilo: Kaj je rekel in kdaj je rekel?.J.Kem.Educa. 65, str.1053-1054.
- Hart, h; Craine, l; Hart, d. Organska kemija: kratek tečaj, (deveta izdaja), Mehika, McGraw-Hill.
- Garcia, a., Aubad, a., Zapata, r.,(1985), proti kemiji 2, Bogota: Temis
- Pine, s.,Hammond, g.,Hendrickson, j., Cram, d.,(1980), Organska kemija (4. izdaja), Mehika: McGraw-Hill.
- Morrison, r.,Boyd, r.,(1998), organska kemija, (5. izdaja), Španija, Addison Wesley Iberoamericana
- « 20 domačih zdravil za znižanje sladkorja (naravno)
- Značilnosti družbeno -kritičnih paradigmov, metode, predstavniki »