Struktura kalcijevega karbonata, lastnosti, tvorba, uporabe

- 4022
- 499
- Stuart Armstrong
On kalcijev karbonat To je anorganska spojina, katere kemijska formula je Caco3. Najdemo ga predvsem v mineralih, kot sta kalcit in aragonit. Prav tako je sestavljen apnenec, sedimentna skala, v kateri je prisoten mineral kalcita.
Ta pomemben kovinski karbonat dobimo industrijsko z ekstrakcijo in brušenjem mineralov, ki ga vsebujejo; V ta namen se v glavnem uporablja marmor. Drug postopek je pri uporabi kalcijevega oksida, ki postane kalcijev hidroksid, ki obori kalcijev karbonat z dodatkom ogljikovega dioksida. Na ta način se kristali pridobijo iz širokega razpona velikosti.
 Polževa lupina je sestavljena predvsem iz kalcijevega karbonata. Vir: Pixabay.
Polževa lupina je sestavljena predvsem iz kalcijevega karbonata. Vir: Pixabay. Uporabljajo se lahko tudi za industrijsko proizvodnjo Caco3, V majhnem obsegu školjke školjk, jajčne lupine in ostrige, v katerih je prisotna.
Kalcijev karbonat, prisoten v apnencu, raztopimo z ogljikovim dioksidom v vodi, ki ustvarja kalcijev bikarbonat. To dejanje lahko povzroči kaverne in je vzrok za alkalinacijo vode; dogodek velikega pomena pri vzdrževanju življenja v njem.
Uporablja se pri gradnji in izdelavi skulptur; Primeri tega so partner Aten, katedrala v Krakovu in skulptura Abrahama Lincolna v Washingtonu. Vendar je njegova dovzetnost za kisli dež zmanjšala njegovo uporabo pri gradnji.
Kalcijev karbonat je imel več aplikacij v industriji kot material za polnjenje plastike in papirja. V medicini se uporablja za nadzor želodčne kislosti; kot prehransko dopolnilo kalcija; za nadzor fosfatije pri bolnikih s kronično ledvično odpovedjo itd.
[TOC]
Struktura
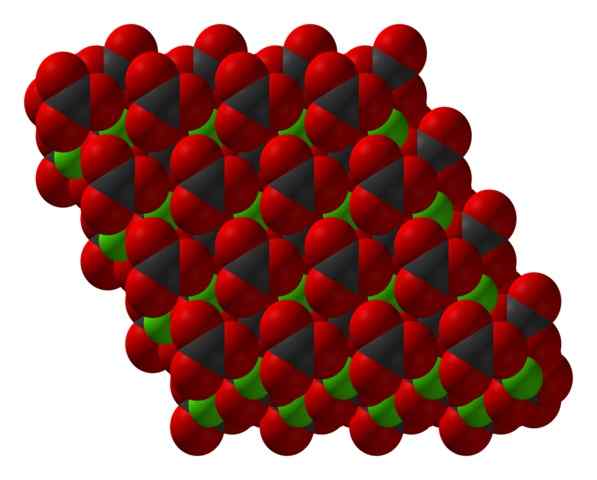 Chanco3 kristalna struktura, predstavljena z modelom polnjenja prostora. Vir: CCOIL [CC BY-SA 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)]
Chanco3 kristalna struktura, predstavljena z modelom polnjenja prostora. Vir: CCOIL [CC BY-SA 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)] Formula kalcijevega karbonata, caco3, označuje, da je delež med Ca ioni2+ in co32- Je 1: 1; to je za vsako ca2+ Obstaja co32- kolega, ki elektrostátično komunicira z njim. Tako se ionska vez na koncu ti ioni tvorijo strukturne vzorce, ki definirajo kristal.
Na vrhunski sliki je prikazana struktura caco3. Zelene sfere ustrezajo kationom2+, in rdeča in črna krogla do anionov32-. Upoštevajte, da se zdi, da struktura tvori več plasti: eden od kalcija in drug karbonat; kar pomeni, da se kristalizira v kompaktni šesterokotni strukturi.
Lahko vam služi: amonijev klorid (NH4Cl)Ta šesterokotna faza (β-kako3) Ustreza polimorfu. Obstajata še dva: ortorrombic (λ-caco3) in še bolj gosto šesterokotno (μ-caco3). Spodnja slika pomaga bolje vizualizirati srečni šesterokotnik:
 Šesterokotna struktura kalcita. MaterialScientist pri angleški Wikipediji [CC BY-SA 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)]
Šesterokotna struktura kalcita. MaterialScientist pri angleški Wikipediji [CC BY-SA 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)] Vendar se, odvisno od temperature (in za to sol), se ioni v njihovih vibracijah prilagodijo drugim strukturam; To so prej omenjeni polimorfi (β, λ in μ).
Ker zvenijo, niso dobro znani, razen če jih v naslednjem razdelku omenjajo s svojimi mineraloškimi imeni.
Trdota beljakovin
Cacovi kristali3 Niso sami: lahko gostijo nečistoče kot druge kovinske katione, ki jih barvajo v barvah; o beljakovine, ki vključujejo organsko matrico, ki nekako prispeva k njegovi naravni trdoti.
Beljakovine zmanjšujejo napetost, ki jo kristali doživljajo drug od drugega pred pritiskom ali udarcem. Kot? Ko se prepletate med kristali, ki deluje, kot da bi šlo.
Zato je ta spojina ali mineral biokompatibilna in ni presenečena, da je del nohtov, morskih školjk, školjk ali kosti ježkov. To je bil vir navdiha za tiste, ki so namenjeni razvoju novih materialov.
Lastnosti
Druga imena
-Aragonit
-Kalcito
-Volterit
-Kalcijevo mleko
-Bela tabla
-Marmor
Molarna masa
100.086 g/mol.
Fizični opis
WHET WAIT WAIT.
Okus
Podobno kot kreda, brez okusa.
Fusion in vrelišča
Se pokvari, ker sprošča co2 preden se sploh taljenje ali vrelo.
Topnost
Praktično netopna v vodi in alkoholu. Raztopljen je z efekti v razredčenem ocetnem in klorovodiku. Hidroksidi pa zmanjšujejo topnost. Medtem amonijeve soli in ogljikov dioksid povečajo topnost kalcijevega karbonata v vodi.
Gostota
2,7 do 2,95 g/cm3.
Razgradnja
Približno 825 ° C se razgradi na kalcijev oksid (apno) in ogljikov dioksid (CO2).
ph
8 do 9
Lomni količnik
-1.7216 do 300 nm in 1.6584 do 589 nm (kalcita).
-1,5145 do 300 nm in 1.4864 do 589 nm (aragonit).
Nezdružljivosti
S kislinami, aluminijem in amonijevo soljo.
Fuzijska entalpija
36 kJ/mol pri 800 ° C (kalcit).
Vam lahko služi: molarnost: koncentracija, enote, izračun, vajeKonstantna topnost
3,36 · 10-9 pri 25 ° C.
Trdota
-3.0 (kalcit)
-3.5 - 4.0 (aragonit) na lestvici MOHS.
Fazni prehodi
Aragonit je metastabilen in nepovratno spremeni v kalcit, ko ga segreje na suhem zraku na 400 ° C.
Reaktivnost
Kalcijev karbonat reagira s kislinami, sprošča ogljikov dioksid, ionski kalcij in vodo.
Kalcijev karbonat se kombinira z nasičeno vodo z ogljikovim dioksidom, kar je enakovredno ogljikove kisline (H2Co3), Da tvori kalcijev bikarbonat.
Usposabljanje
Kreda, marmorja in apnenca, prva dva minerala in skalnat material, tretji, vsebujejo kalcijev karbonat in so sedimentnega izvora, mislijo, da jih tvorijo sedimentacija polžev že milijone let leta.
PH bi lahko bil najpomembnejši dejavnik pri tvorbi polimorfov pri temperaturi 24 ° C. Vaterita je glavni izdelek v različnih pH med 8,5 in 10; Aragonit je pH 11; in kalcit na ph> 12.
Znano je tudi, da številne alge sladke vode gradijo kristale kalcita, ko rastejo v kalcijevem nasičenem okolju. Poleg tega lahko mikroalge povzročijo padavine kalcijevega karbonata.
Oblike kalcijevega karbonata
Na spodnjih slikah bodo za kalcijev karbonat prikazane tri glavne oblike ali polimorfi:
 Kalcita kristal. Vir: starš Géry [javna domena]
Kalcita kristal. Vir: starš Géry [javna domena] Aragonit kristal. Vir: Battistini Riccardo [CC BY-SA 4.0 (https: // creativeCommons.Org/licence/by-sa/4.0)]
Aragonit kristal. Vir: Battistini Riccardo [CC BY-SA 4.0 (https: // creativeCommons.Org/licence/by-sa/4.0)] Vaterita kristali. Vir: Rob Lavinsky, Irocks.com-cc-by-sa-3.0 [cc by-sa 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)]
Vaterita kristali. Vir: Rob Lavinsky, Irocks.com-cc-by-sa-3.0 [cc by-sa 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)]
Od zgoraj navzdol so polimorfi kalcita, aragonita in Vaterita. Upoštevajte razliko med morfologijo njihovih kristalov (barva je značilna za njegov izvor in značilnosti njegovega okolja).
Vaterita je bolj neprozorna od kalcita, slednja postane celo popolna. Medtem kristali aragonita spominjajo na majhne podolgovate monolite.
Če vzorce teh treh polimorfov opazimo pod elektronskim mikroskopom, njihovimi kristali (sivkastih tonov, ker tehnika ne omogoča ločljivosti barve), bi bile enake morfologije najdene kot v makroskopskih lestvicah; to je na prvi pogled.
Med temi tremi polimorfi je kalcit najpogostejši in stabilen, sledita aragonit in na koncu Vaterita, najredkejša oblika Caco3
Vam lahko služi: kalorimetrija: kakšne študije in aplikacijePrijave
Industrijalisti
Kalcijev karbonat poveča odpornost na torzijo in vleko sintetičnega in naravnega guma, kar ohranja njegovo prožnost. Uporablja se v gradbeni industriji kot cementna sestavina in kot surovina za apno. Njegova uporaba se je zmanjšala, ker jo poškoduje kisli dež.
Kalcijev karbonat se uporablja pri čiščenju železa. V obliki apna odpravlja žveplov dioksid, ki je prisoten v kovini. Uporablja se čiščenje sladkorja iz pese. Uporabljali so ga kot kredo za skrilavce, vendar ga je za to aplikacijo zamenjal omet.
Kalcijev karbonat se meša s kiti, ki se uporablja pri namestitvi stekla. Ground se uporablja kot polnjenje materiala v mikroporoznem filmu, ki se uporablja v plenicah. Uporablja se tudi kot polnjenje materiala v plastiki, kot je PVC. Poleg tega se moč plastike poveča.
Kalcijev karbonat se uporablja za povečanje zmogljivosti pokritosti slik. Uporablja se kot material za polnjenje papirja, ker je cenejši od lesenih vlaken, saj lahko predstavlja več kot 10% papirja.
Zdravniki
Uporablja se kot antacid za boj proti želodčni hiperacidnosti in lajšanje prebavne motnje. Uporablja se kot prehranski dodatek kalcija in pri zdravljenju in preprečevanju osteoporoze. Uporablja se pri zdravljenju hiperfosfatije pri bolnikih s kronično odpovedjo ledvic.
Uporablja se za zmanjšanje neželenih učinkov zaviralcev proteaze, ki se uporabljajo pri zdravljenju HIV, pri bolnikih pa opazuje zmanjšanje driske.
Zniža krvni tlak pri nosečnicah s hipertenzijo in preeklampsijo, saj bi lahko oba povezana s povečanjem povpraševanja po kalcija.
Drugi
Kalcijev karbonat se v kmetijstvu uporablja kot gnojilo in za boj proti kislosti tal. Uporablja se kot konzervans, zadržek barv in ponovno potrditev hrane.
Poleg tega je sestavina zobne paste in služi kot abrazivna pri prahu pri čiščenju in pranju.
Reference
- Shiver & Atkins. (2008). Anorganska kemija. (Četrta izdaja). MC Graw Hill.
- Wikipedija. (2019). Karbonatni kalcij. Pridobljeno iz: v.Wikipedija.org
- Nacionalni center za informacije o biotehnologiji. (2019). Karbonatni kalcij. Baza podatkov Pubchem., Cid = 10112. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Kai-yin Chong, Chin-Hua Chia in Sarani Zakaria. (2014). Polimorfs kalcijev karbonat na temperaturni reakciji. Zbornik AIP konference 1614, 52; doi.org/10.1063/1.4895169
- Greg Watry. (1. november 2016). Odkrivanje kristalov s karbonatom Howum dobi moč. Prednost poslovno trženje. Okreval od: rdmag.com
- Ameriški elementi. (2019). Karbonatni kalcij. Pridobljeno od: Americanments.com
- Elsevier. (2019). Karbonatni kalcij. Znanstveno. Pridobljeno iz: SCINCEDIRECT.com
- Kemijska knjiga. (2017). Karbonatni kalcij. Obnovi se od: Kemicalbook.com

