Srebrna struktura Bromuro (AGBR), lastnosti in uporabe
- 2484
- 42
- Percy Feeney
On Srebrni bromid To je anorganska sol, katere kemična formula je AGBR. Njegova trdna snov je sestavljena iz ag kationov+ In Br Aniss- v deležu 1: 1, ki ga privlačijo elektrostatične sile ali ionske povezave. Videti je, kot da je kovinsko srebro dal enega od svojih valenčnih elektronov do molekularnega broma.
Njegova narava spominja na njegove "brate" kloride in srebro Yoduro. Tri soli so netopne v vodi, imajo podobne barve, poleg tega pa so občutljive na svetlobo; to pomeni, da trpijo fotokemične reakcije. Ta lastnost je bila uporabljena pri pridobivanju fotografij, kar je rezultat zmanjšanja Ag ionov+ do kovinskega srebra.
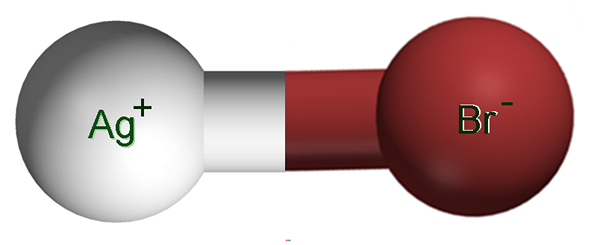
 Srebrni bromidni ioni. Vir: Claudio Pistilli [CC BY-SA 4.0 (https: // creativeCommons.Org/licence/by-sa/4.0)]
Srebrni bromidni ioni. Vir: Claudio Pistilli [CC BY-SA 4.0 (https: // creativeCommons.Org/licence/by-sa/4.0)] Na zgornji sliki je prikazan ag ionski par+Br-, v katerem bele in rjave sfere ustrezajo ag ionom+ in br-, oziroma. Tu predstavljajo ionsko vez kot AG-BR, vendar je treba navesti, da takšne kovalentne vezi med obema ionoma ni takšne kovalentne vezi.
Morda se zdi nasprotujoče si, da je srebro tisti, ki zagotavlja črno barvo brezbarvnih fotografij. To je zato, ker AGBR reagira s svetlobo in ustvarja latentno sliko; ki se nato poveča s povečanjem zmanjšanja srebra.
[TOC]
Srebrna bromidna struktura
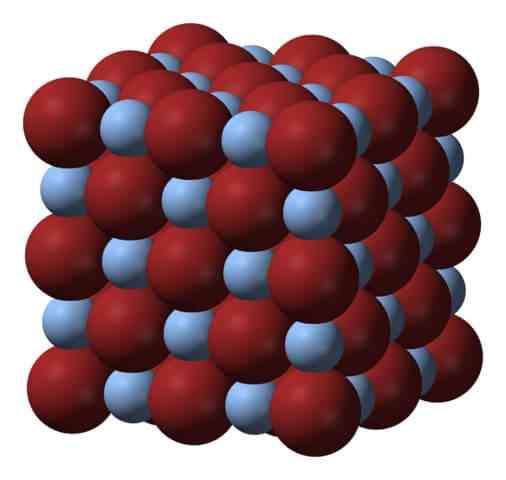 Kristalna struktura srebrnega bromida. Vir: Benjah-BMM27 prek Wikipedije.
Kristalna struktura srebrnega bromida. Vir: Benjah-BMM27 prek Wikipedije. Nad omrežjem ali kristalno strukturo srebrnega bromida. Tu je prikazana bolj zvesta predstavitev razlike v velikosti med ionskimi radijskimi napravami Ag+ in br-. BR Anions-, Bolj zajetno, pustite interstike, kjer se nahajajo ag kationi+, ki je obkrožen s šestimi BR- (in obratno).
Ta struktura je značilna za kubični kristalni sistem, zlasti tip soli; Enako, na primer, da za natrijev klorid, NaCl. Pravzaprav slika to olajša tako, da ima popolno kubično mejo.
Vam lahko služi: referenčna elektroda: značilnosti, funkcija, primeriNa prvi pogled je mogoče opozoriti, da je med ioni nekaj razlike v velikosti. To in morda elektronske značilnosti Ag+ (in o možnem učinku nekaterih nečistoč) vodi do kristalov AGBR, ki predstavljajo napake; Se pravi, mesta, na katerih je zaporedje naročanja ionov v prostoru "zlomi".
Kristalne napake
Te napake so sestavljene iz vrzeli, ki jih puščajo odsotni ali razseljeni ioni kraja. Na primer med šestimi anioni- Običajno bi moral biti Crution AG+; Toda namesto tega lahko obstaja vakuum, ker se je srebro premaknilo na drugo Intersticij (napaka Frenkel).
Čeprav vplivajo na kristalno omrežje, dajejo prednost srebrnim reakcijam s svetlobo; In večji kot so kristali ali njihova grozda (velikost zrn), večje je število napak, zato bo bolj občutljiv na svetlobo. Prav tako nečistoče vplivajo na strukturo in to lastnost, zlasti tiste, ki jih je mogoče zmanjšati z elektroni.
Zaradi slednjih veliki kristali AGBR potrebujejo manjšo izpostavljenost svetlobi, da se zmanjša; to pomeni, da so bolj zaželeni za fotografske namene.
Sinteza
V laboratoriju lahko sintetizirate srebrno bromid, ki meša vodno raztopino srebrnega nitrata, Agno3, Z natrijevo bromidno soljo, Nabab. Prva sol prinaša srebro in drugi bromid. Sledi reakcija z dvojnim premikom ali metatezo, ki jo je mogoče predstaviti s spodnjo kemijsko enačbo:
Agno3(aq) + nabab (s) => nano3(aq) + agbr (s)
Lahko vam služi: natrijev bromid (NABR)Upoštevajte, da sol nitratna sol, nano3, V vodi je topen, medtem ko se AGBR obori kot trdno s trdno barvo z rahlo rumeno barvo. Kasneje se trdna snov opere in podvrže vakuumu. Poleg NABB bi lahko KBR uporabili tudi kot vir bromuroznih anionov.
Po drugi strani pa lahko AGBR pridobimo prek minerala Bromirita in njegovih postopkov čiščenja.
Lastnosti
Videz
Glinena rumena trdna snov, podobno glini.
Molekularna masa
187,77 g/mol.
Gostota
6.473 g/ml.
Tališče
432 ° C.
Vrelišče
1502 ° C.
Topnost vode
0,140 g/ml pri 20 ° C.
Lomni količnik
2.253.
Toplotna zmogljivost
270 j/kg · k.
Občutljivost svetlobe
V prejšnjem razdelku je bilo rečeno, da v kristalih AGBR obstajajo napake, ki spodbujajo občutljivost te soli v svetlobi, saj ujamejo oblikovane elektrone; In tako jim teoretično preprečujejo, da bi reagirali z drugimi vrstami na sredini, kot je zračni kisik.
Elektron se sprosti iz reakcije BR- S fotonom:
Br- + Hv => 1/2br2 + in-
Upoštevajte, da obstaja a2, ki bo barvilo trdno rdečo, če se ne odstrani. Osvobodeni elektroni zmanjšujejo agrotione+, V svojih intersticah kovinsko srebro (včasih predstavljeno kot Ag0)::
Ag+ + in- => Ag
Potem ima neto enačbo:
Agbr => ag + 1/2br2
Ko se oblikujejo "prve plasti" kovinskega srebra na površini, se reče, da obstaja latentna podoba, še vedno nevidna. Ta slika je narejena na milijonekrat bolj vidna, če druga kemična vrsta (na primer hidrokinon in fenidon v razvojnem procesu) poveča zmanjšanje kristalov AGBR na kovinsko srebro
Lahko vam služi: Carbon 12: Jedrski zapis, zgodovina, komentarjiPrijave
 Fotografija črno -bele žepne ure. Vir: Pexels.
Fotografija črno -bele žepne ure. Vir: Pexels. Srebrni bromid se najbolj uporablja od vseh halogenidov na področju razodetja fotografskih filmov. AGBR se uporablja za te filme, narejen s celuloznim acetatom, suspendiran v želeju (fotografska emulzija) in v prisotnosti 4- (metilacije) fenolnega sulfata (metola) ali fenidona in hidrokinona.
Z vsemi temi reagenti lahko življenje damo latentni podobi; Zaključite in pospešite preoblikovanje ionskega v kovinsko srebro. Če pa ne nadaljujete z določeno oskrbo in izkušnjami, se bo vse površinsko srebro oksidaliralo in kontrast med črno -belo barvo se bo končal.
Zato so ključnega pomena v kopalnicah brezposelnosti, fiksacije in pranja, fotografskih filmov.
Obstajajo umetniki, ki se s temi procesi igrajo tako, da ustvarjajo sive odtenke, ki obogatijo lepoto podobe in svojo zapuščino; In vse to, včasih tudi brez suma, zahvaljujoč kemičnim reakcijam, katerih teoretična osnova lahko postane nekoliko zapletena, in svetlobno občutljiv AGBR in to označuje izhodišče.
Reference
- Wikipedija. (2019). Srebrni bromid. Pridobljeno iz: v.Wikipedija.org
- Michael w. Davidson . (13. november 2015). Galerija polariziranih svetlobnih digitalnih slik: srebrni bromid. Olympus. Okrevano od: mikro.Magnet.Fsu.Edu
- Crystran Ltd. (2012). Srebrni bromid (AGBR). Okrevano od: Crystran.co.Združeno kraljestvo
- Lothar Duenkel, Juergen Eichler, Gerhard Ackermann in Claudia Schneeweiss. (29. junij 2004). Emulzije, ki temeljijo na srebro-bromidu, za uporabnike v holografiji: Proizvodnja, predelava in uporaba, Proc. SPIE 5290, praktična holografija xviii: materiali in aplikacije; Doi: 10.1117/12.525035; https: // doi.org/10.1117/12.525035
- Alan G. Oblika. (1993). Anorganska kemija. (Druga izdaja.). Uredništvo se je vrtelo.
- Carlos Güido in Ma Eugenia Bautista. (2018). Uvod v fotografsko kemijo. Okrevano od: fotografija.Ceduc.com.mx
- Garcia d. Lepo. (9. januar 2014). Kemija, fotografija in kemija madoz. Okrevano od: dimetilsulfuro.je
- « Kako ustrezno poučiti otroka 13 praktičnih nasvetov
- Ciklobutanska struktura, lastnosti, uporabe in sinteza »

