Natrijeva benzoatna struktura, lastnosti, uporabe in tveganja
- 2917
- 280
- Mr. Shane Larkin
On Natrijev benzoat Gre za organsko sol, katere kemična formula je c6H5Pot. Pojavi se ali ustvarja z nevtralizacijsko reakcijo med benzojsko kislino in natrijevim hidroksidom. Rezultat je bela trdna (spodnja slika) v vodi in se razgradi s segrevanjem pri 120 ° C.
To sol lahko najdemo naravno v več sadju in drugih delih zelenjave, kot so: borovnice, slive, rozine, cimet, vonj in jabolka. Je tudi presnovek alg in rastlin.
 Natrijev benzoat. Vir: Chemik10 na Poljski Wikipediji [CC BY-SA 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)]
Natrijev benzoat. Vir: Chemik10 na Poljski Wikipediji [CC BY-SA 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)] Natrijev benzoat se ne kopiči v telesu, saj ga hitro kombiniramo z glicinom aminokislino, da tvori hippursko kislino, ki se prosto izloča v urinu.
Ta spojina se uporablja s konzervansom hrane, njegovo delovanje pa je učinkovitejše pri kislem pH. To je posledica prisotnosti organskih kislin, ki hrani dajejo pH, primerno za delovanje natrijevega benzoata; Da se kot taka konča v benzojski kislini.
Ta sol se uporablja tudi pri zdravljenju dednih presnovnih motenj cikla sečnine, ki povzroča kopičenje vmesnega presnovka, za katerega encim, ki je slab.
Mednarodni program za kemijsko varnost ni našel škodljivega učinka natrijevega benzoata na ljudi, za porabo med 647 - 825 mg/kg telesne mase.
Vendar poročajo, da lahko natrijev benzoat ustvari psevdoalergične reakcije in poslabša simptome pri bolnikih s pogostimi epizodami urtikarije in astmo.
[TOC]
Struktura natrijevega benzoata
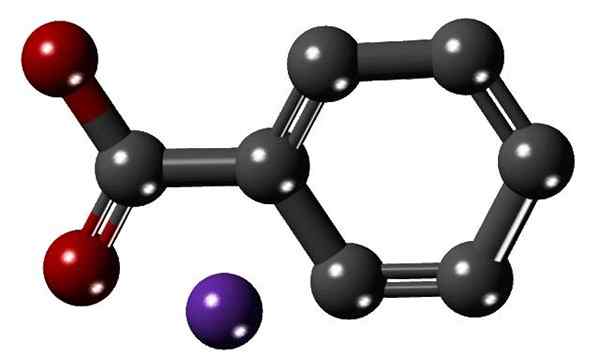
 Struktura natrijevega benzoata. Vir: Kamil9243 [CC BY-SA 4.0 (https: // creativeCommons.Org/licence/by-sa/4.0)]
Struktura natrijevega benzoata. Vir: Kamil9243 [CC BY-SA 4.0 (https: // creativeCommons.Org/licence/by-sa/4.0)] Zgornja slika prikazuje strukturo natrijevega benzoata z modelom kroglic in palic. Aromatični obroč s karboksilatno skupino -lahko opazimo s karboksilatom-, povezan z njim (rdeče sfere); in slednji pa elektrostátično privlači na kation+ (vijolična krogla).
Ker je razlika v velikosti med obema ionoma velika (primerjava na sliki), ni čudno, da je retikularna energija kristalov natrijevega benzoata nizka. To povzroči, da imajo njihovi kristali naravno nagnjenost k solubilizaciji v polarnih topilih ali trpijo vrsto kemičnih reakcij.
Vam lahko služi: plinasta država: značilnosti, splošni zakon, primeriC6H5COO- Lahko sprejmete dva vodikova mostova iz dveh vodnih molekul, ki daje prednost njegovi hidraciji. Medtem Na+ Prav tako se konča raztopljeno z vodo, premagovanje elektrostatičnih sil, ki jih ohranjajo skupaj s C6H5COO-.
Tako je ta sol sestavljena iz C ionov6H5COO- in na+, ki so urejeni na urejen način za izgradnjo kristalov. V literaturi se informacije ne dosežejo v zvezi z njegovo kristalno strukturo, zato ni znano, kakšna je vrsta enotne celice za to sol.
[TOC]
Lastnosti
Kemična imena
-Natrijev benzoat
-Natrijeva sol benzojske kisline
-Sobenato
-Antimol.
Fizični opis
Bela zrnca ali kristalni prah. Brezbarven kristalni prah.
Vonj
Stranišče.
Okus
Grenka, adstrigentna in neprijetna.
točka vžiga
> 100 ° C.
Samožitev
> 500 ° C.
Gostota
1,50 g/cm3.
Topnost
-Topno v tekočem amoniju in piridinu.
-Malo topno v etanolu: 8,22 g/100 g pri 25 ° C.
-V metanolu je bolj topen kot v etanolu: 8,22 g/100 g pri 15 ° C.
Stabilnost
Je stabilen v priporočenih pogojih skladiščenja. Lahko je občutljiv na vlago, hidroliziranje na benzojsko kislino. Nezdružljivo z močnimi oksidacijskimi sredstvi, alkaliji in mineralnimi kislinami.
Razgradnja
Ko se segreje, da se razgradi na 120 ° C (248 ° F), oddaja dim natrijevega oksida in drugih komponent, ki so lahko strupene in rakotvorne.
Z razpadom 120 ° C preprečuje natančno določitev njegovih vrelišč in fuzijskih točk, poročane vrednosti teh parametrov teoretične ocene so.
ph
Blizu 8, raztopljeno v vodi. To pomeni, da je osnovna sol. To je zato, ker je hidrolizirano za sproščanje ionov Oh-.
Površinska napetost
72,9 mn/cm pri 20 ° C v raztopini 1 g/l vode.
Sinteza
Benzojska kislina, ki je vključena v sintezo natrijevega benzoata, nastaja predvsem s tremi metodami:
-Naftalen je oksidiran z vanadijevim pentoksidom, da tvori ftálic anhidrid. Ta spojina lahko premalo vboksika, da izvira v benzojski kislini, saj se v svoji strukturi z dvema aromatičnima obročema zdi, da imata dve skupini -kondenzatni avtomobil drug z drugim.
-Toluen se oksidira v benzojsko kislino z dodajanjem dušikove kisline. V tej reakciji "preprosto" Metilo skupina oksidira karboksilno skupino:
C6H5Pogl3 => C6H5COOH
-In končno se benzotririd hidrolizira z delovanjem mineralnih kislin, kar povzroča benzojsko kislino.
Vam lahko služi: keramični materiali: značilnosti, vrste, primeriDobimo benzojsko kislino s katero koli od teh treh metod, nato pa se raztopi v natrijevem hidroksidu. Te spojine doživljajo nevtralizacijsko reakcijo, ki proizvaja natrij in vodni benzoat.
C6H5COOH +NAOH => C6H5Pot +h2Tudi
Reakcijo lahko izvedemo tudi z natrijevim karbonatom, čeprav je njegova zmogljivost lahko manjša od želenih.
Prijave
V hrani
Natrijev benzoat je sredstvo za konzervans s hrano, ki lahko zavira ali odloži postopek fermentacije, zakisanja ali katerega koli procesa, ki jih poslabša. Poleg tega ima natrijev benzoat akcijo fungicida.
Ta sol lahko odpravi kvasovke, bakterije in glive, ki so prisotne v hrani. Njegovo konzervaktivno delovanje je učinkovitejše za pH < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Natrijev benzoat se uporablja tudi pri ohranjanju gaziranih in brezalkoholnih pijač, v katerih je prisotna ogljikova kislina. Tudi pri marmeladi, bogato s citronsko kislino in na splošno v hrani s kislinami, ki vzpostavljajo kisli medij.
Poleg tega se uporablja v krmi s koncentracijo natrijevega benzoata 0,1 %. Najvišja količina uporabljene benzojske kisline in natrijevega benzoata kot kondomi v hrani ne presega 2.000 mg/kg hrane.
Zdravljenje
Akutna hiperamonemija
Natrijev fenilaceat in natrijev benzoat se uporabljata v obliki adjuvantnih terapij pri zdravljenju akutne hiperamonemije in s tem povezano flusopatijo pri bolnikih s spremembami cikla sečnine.
Te spojine so razvrščene kot sirota. To poimenovanje velja za zdravila, ki z ekonomskega vidika niso donosna.
Shizofrenija
Natrijev benzoat se eksperimentalno uporablja pri zdravljenju shizofrenije. Osrednji del preiskave je vloga, da inhibicija encimov oksidaze D-aaminokislin, aktivnost, ki jo natrijev benzoat ustreza zdravljenju pri zdravljenju.
Arginosuccin kisli
Natrijev benzoat se uporablja pri zdravljenju arginosukcinske kisle kisline, dedne presnovne motnje, ki lahko pri bolnikih povzroči zvišanje koncentracije amonija, ki lahko vpliva na centralni živčni sistem.
Vam lahko služi: benzična kislina: sinteza, prenos in uporabaZaviralec
-To je zaviralec encima Araquidonato 15-lipoksigenasa, encima, ki ga farmacevtska industrija preiskuje, ker je vključena v koronariopatije.
-Zavira delovanje trihacilglicerid lipaznega encima, encima, ki deluje v sproščanju glicerola in maščobnih kislin v tankem črevesju, kar omogoča absorpcijo teh lipidov, ki so prisotni v hrani.
Morda je mogoče uporabo natrijevega benzoata za uravnavanje črevesne absorpcije lipidov, kot so triacilgliceridi.
Dedne motnje
Natrijev benzoat se uporablja pri zdravljenju več dednih motenj, povezanih s presnovo aminokislin, med katerimi se navajajo: zdravljenje hiperargininemije in zdravljenje pomanjkanja translokaznega encima ornitina.
Drugi
-Uporablja se v izpiranju na osnovi alkohola in v srebrnem laku. Poleg tega se uporablja pri izdelavi pirotehničnih spojin, ki je odgovoren za žvižga.
-Uporablja se kot antikorozivno, kar je ena glavna zahteva pri proizvodnji te soli. Uporablja se tudi v hladilnih sredstvih, antifriznih in drugih sistemih na osnovi vode.
-V formulaciji plastike, kot je polipropilen, se uporablja za izboljšanje njegove odpornosti in jasnosti.
-Služi kot stabilizator v kopalnicah in fotografskih procesih.
Tveganja
Natrijev benzoat uvršča FDA kot "na splošno varen", pri odmerku 0,1 % teže hrane. Za stik s kožo in očmi se ne zdi razdražljivo, zato lahko rečemo, da je akutna strupenost nizka.
Vendar lahko natrijev benzoat povzroči neimunološke reakcije (pseudoalergia) s stikom. Ta učinek je redek pri normalnih ljudeh, toda pri bolnikih z epizodami pogostih urtikarij ali simptomov astme se lahko poveča pogostost teh simptomov.
V študijah, opravljenih pri podganah in miših.
Neprijetnost njegove uporabe v prisotnosti askorbinske kisline, ki bi lahko proizvedla benzen; Strupena spojina, označena kot rakotvorna.
Reference
- Neto industrija. (2019). Proizvodnja natrijevega benzoata. Okrevano od: znanost.Jank.org
- Wikipedija. (2019). Natrijev benzoat. Pridobljeno iz: v.Wikipedija.org
- Pubchem. (2019). Natrijev benzoat. Okrevano od: pubchem.NCBI.Nim.ameriški nacionalni inštitut za zdravje.Gov
- Hanes t. (2019). Dejstva o natrijevem benzoatu. Livestrong. Okrevano od: Livestrong.com
- Kemijska knjiga. (2017). Natrijev benzoat. Obnovi se od: Kemicalbook.com
- Lane H. in zelje. (2013) Jama Psichiatry. 70 (12): 1267 - 1275.
- Svetovna zdravstvena organizacija Ženeva. (12. april 2005). Benzojska kislina in natrijev benzoat. [PDF]. Okreval od: kdo.int
- « Malojillo koristi, prehranski podatki, kontraindikacije
- 16 najnevarnejših zdravil in njihovih učinkov »

