Linearna struktura Alcanos, lastnosti, nomenklatura, primeri

- 3872
- 1159
- Ricky Dach
The Linearne alkane So nasičeni ogljikovodiki, katerih splošna kemična formula je n-CnH2N+2. Ker so nasičeni ogljikovodiki, so vse njegove vezi preproste (C-H) in so sestavljene samo iz atomov ogljika in vodika. Prejmejo tudi ime parafinov in jih razlikujejo od razvejanih toumov, na katere se imenujejo izoparafinas.
Teh ogljikovodikov nimajo posledic in obročev. Ta družina organskih spojin bolj kot linije bolj spominja na verige (ravna veriga alkane); ali iz kulinaričnega kota, do špagete (surove in kuhane).
 Če bi bili surovi špageti manj krhki, bi imeli še podrobnejšo podobnost z linearnimi alkani. Vir: Pixabay.
Če bi bili surovi špageti manj krhki, bi imeli še podrobnejšo podobnost z linearnimi alkani. Vir: Pixabay. Surovi špageti predstavljajo idealno in osamljeno stanje linearnih alkanov, čeprav z izrazito nagnjenostjo k prekinitvi; Medtem ko so kuhani, ne glede na to, ali se približujejo svojemu naravnemu in sinergističnemu stanju: nekateri sodelujejo z drugimi v celoti (na primer testeninsko jed).
Te vrste ogljikovodikov seveda najdemo v nahajališčih zemeljskega plina in nafte. Najlažje imajo mazalne lastnosti, medtem ko se težke obnašajo kot nezaželeni asfalt; topno pa v parafinih. Zelo dobro služijo kot topila, maziva, goriva in asfalt.
[TOC]
Struktura linearnih alkanov
Skupine
Omenjeno je bilo, da je splošna formula teh alkanov cnH2N+2. Ta formula je v resnici enaka za vse alkane, bodisi linearne ali razvejane. Razlika nato v n- To je pred alcanovo formulo, katere označevanje pomeni "normalno".
To bo videti pozneje kot to n- Za alkane je nepotrebno z ogljikovo številko, ki je enaka ali manj kot štiri (n ≤ 4).
Linija ali veriga ne moreta sestavljati enega samega ogljikovega atoma, zato se metan izključi za razlago (ch4, n = 1). Če je n = 2, imamo etana, cho3-Pogl3. Upoštevajte, da je ta alkan sestavljen iz dveh metilnih skupin, CHO3, povezani drug z drugim.
Povečanje števila ogljika, n = 3, dobimo alkanski propan, CHO3-Pogl2-Pogl3. Zdaj se pojavi nova skupina, Cho2, imenovan metilen. Ne glede na to, kako velik je linearni alkan, vedno ne boste imeli dveh skupin: Cho3 in pogl2.
Vam lahko služi: iterbio: struktura, lastnosti, uporabe, pridobivanjeDolžine njihovih verig
Ko se število ogljika linearnega alkana poveča, je v vseh nastalih strukturah konstanta: število metilenskih skupin se poveča. Recimo na primer linearne alkane z n = 4, 5 in 6:
Pogl3-Pogl2-Pogl2-Pogl3 (n-Busana)
Pogl3-Pogl2-Pogl2-Pogl2-Pogl3 (n-Pentano)
Pogl3-Pogl2-Pogl2-Pogl2-Pogl2-Pogl3 (n-heksan)
Verige postanejo daljše, ker dodajajo v svoje strukturne skupine zbole2. Tako se obsežen ali kratek linearni alkan razlikuje po tem, koliko CHO2 loči dve skupini terminalov3. Vsi ti alkani nimajo ničesar plus dva3: Na začetku verige in na koncu iste. Če bi imel več, bi to pomenilo prisotnost posledic.
Prav tako je mogoče opaziti popolno odsotnost CH skupin, ki so prisotne le v posledicah ali kadar obstajajo nadomestne skupine, povezane z enim od ogljika verige.
Strukturno formulo lahko povzamemo na naslednji način: CH3(Pogl2)N-2Pogl3. Poskusite se prijaviti in ponazoriti.
Skladnosti
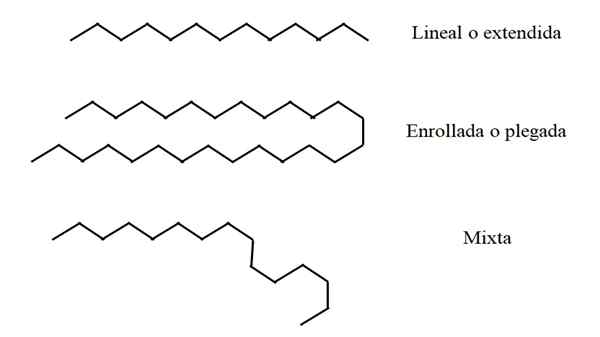 Strukturne skladbe linearnih alkanov. Vir: Gabriel Bolívar.
Strukturne skladbe linearnih alkanov. Vir: Gabriel Bolívar. Nekateri linearni alkani so lahko daljši ali krajši od drugih. Tako ima lahko N vrednost od 2 do ∞; to pomeni, da neskončna sestavljena veriga CH skupine2 in dve skupini CH3 terminali (teoretično je možno). Vendar pa vse verige "ne sprejmejo" enako v vesolju.
Tu nastanejo strukturne skladnosti alkanov. Kaj dolgujejo? Do vrtljivosti povezav C-H in prilagodljivosti istega. Ko se te povezave vrtijo ali gnijo.
Linearno
Na zgornji sliki je na primer veriga trinajstih ogljikov, ki ostane linearna ali razširjena. Ta konformacija je idealna, saj se domneva, da molekularno okolje zmanjša prostorsko razporeditev verižnih atomov. Nič je ne moti in se ni treba upogniti.
Lahko vam služi: propilen glikol: struktura, lastnosti, sinteza in uporabeValjana ali zložena
Na sredini slike se enaindvajset ogljikovih verig doživi zunanjo motnjo. Struktura, da bi bila bolj "udobna", vrti svoje povezave tako, da se zloži nase; Tako kot dolgi špageti.
Računalniške študije so pokazale, da je največje število ogljikov, ki jih ima linearna veriga, n = 17. Od n = 18 je nemogoče, da se ne začne zložiti ali valjati.
Mešano
Če je veriga zelo dolga, lahko obstajajo regije, ki ostanejo linearne, medtem ko so druge upognjene ali vpisane. Od vsega je to morda konformacija, ki je najbližje resničnosti.
Lastnosti
Fizično
Ker so ogljikovodiki, so v apolarnem bistvu in zato hidrofobni. To pomeni, da jih ni mogoče pomešati z vodo. So malo goste, ker njihove verige med njimi puščajo preveč praznih prostorov.
Tudi njihova fizična stanja segajo od sode (za n < 5), líquidos (para n < 13) o sólidos (para n ≥ 14), y dependen de la longitud de la cadena.
Interakcije
Molekule linearnih alkanov so apolarne, zato so njihove medmolekularne sile disperzijske vrste Londona. Verige (verjetno sprejemajo mešano konformacijo), nato pritegnejo delovanje njihovih molekulskih mas in takojšnje inducirane dipole njihovih vodikovih in ogljikovih atomov.
Zaradi tega, ko veriga postane daljša, in zato težje, se njene vrelišča in fuzija povečata na enak način.
Stabilnost
Dlje kot veriga, bolj nestabilna je. Običajno trpijo porušitve svojih povezav, da povzročajo manjše verige iz velikega. Pravzaprav je ta postopek znan kot Craqueo, Zelo uporabljen pri rafiniranju nafte.
Nomenklatura
Če želite poimenovati linearne alkane, je dovolj, da pred imenom dodamo indikator N-. Če je n = 3, kot je to pri propanu, je nemogoče, da bi ta alkana predstavil katero koli vejo:
Vam lahko služi: anorganske spojinePogl3-Pogl2-Pogl3
Stvar, ki se ne zgodi od n = 4, torej z N-Blutanom in drugimi alkani:
Pogl3-Pogl2-Pogl2-Pogl3
Tudi
(Pogl3)2Ch-ch3
Druga struktura ustreza izobutanu, ki ga sestavlja strukturni izomer butana. Za razlikovanje enega od drugega, indikator n se začne igrati-. Tako, n-Butano se nanaša samo na linearni izomer, brez posledic.
Večji kot je N, večje je število strukturnih izomerov in največji pomen bo moral uporabiti N- za sklicevanje na linearni izomer.
Na primer oktana, c8H18 (C8H8 × 2 + 2), predstavlja do trinajst strukturnih izomerov, saj je možno veliko posledic. Linearni izomer pa je poimenovan: n-Octane in njegova struktura je:
Pogl3-Pogl2-Pogl2-Pogl2-Pogl2-Pogl2-Pogl2-Pogl3
Primeri
Spodaj so omenjeni in končajo nekaj linearnih alkanov:
-Etano (c2H6): Pogl3Pogl3
-Propan (c3H8): Pogl3Pogl2Pogl3
-n-Heptano (c7H16): Pogl3(Pogl2)5Pogl3.
- n-Dean (c10H22): Pogl3(Pogl2)8Pogl3.
-n-Hexadecano (c16H3. 4): Pogl3(Pogl2)14Pogl3.
-n-Nonadecano (c19H40): Pogl3(Pogl2)17Pogl3.
-n-Eicosan (cdvajsetH42): Pogl3(Pogl2)18Pogl3.
- n-Hektan (c100H202): Pogl3(Pogl2)98Pogl3.
Reference
- Carey f. (2008). Organska kemija. (Šesta izdaja). MC Graw Hill.
- Morrison, r. T. in Boyd, r, n. (1987). Organska kemija. (5. izdaja). Uredništvo Addison-Wesley Interamerican.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Organska kemija. Amine. (10. izdaja.). Wiley Plus.
- Jonathan m. Dober človek. (1997). S čim je dolgi nerazvejeni alkan do linearne globalne minimalne konformacije? J. Kem. Inf. Računalnik. Sci. 1997, 37, 5, 876-878.
- García nissa. (2019). Kaj so alkani? Študij. Okrevano od: študij.com
- gospod. Kevin a. Boudreaux. (2019). Alkani. Okreval od: Angelo.Edu
- Seznam alkenov z ravno verigo. [PDF]. Okreval od: Laney.Edu
- Čelada, Anne Marie, ph.D. (7. septembra 2018). Poimenujte prvih 10 alkanov. Okreval od: Thoughtco.com
- Čudna znanost. (20. marec 2013). Alkani z ravno verigo: napovedovanje lastnosti. Okrevano od: quirkyscience.com
- Wikipedija. (2019). Višji alkani. Pridobljeno iz: v.Wikipedija.org
- « Izhaja iz izračuna Cotangent, demonstracije, vaje
- Struktura in pomen ciklopentanoperhidofenantrena »

