Kalijev acetat struktura, lastnosti, uporabe, pridobivanje
- 1628
- 68
- Ms. Pablo Lebsack
On kalijev acetat Gre za organsko spojino, ki jo tvori ionski kalij k+ in ionski acetat cho3COO-. Njegova kemična formula je CHO3Kuhamo ali kch3COO, ali tudi c2H3Ko2. Je brezbarvna ali bela kristalna trdna, zelo topna v vodi.
Uporablja se za uravnavanje kislosti nekaterih industrijsko predelanih živil. Zaradi velike naklonjenosti z vodo se uporablja v laboratorijih ali v določenih procesih, da absorbira vodo iz drugih spojin, na primer za dehidriranje alkohola.
 KCH kalijev acetat3CO služi za uravnavanje kislosti nekaterih predelanih živil. Avtor: Ritae. Vir: Pixabay.
KCH kalijev acetat3CO služi za uravnavanje kislosti nekaterih predelanih živil. Avtor: Ritae. Vir: Pixabay. Kalijev acetat sodeluje v nekaterih kemičnih reakcijah, kot so njihov pospeševalnik in sinteza organskih spojin. Omogoča tudi povečanje nastajanja protiteles (naravne snovi, ki se borijo proti okužbam) v industrijskih metodah, da jih proizvajajo.
Njegove lastnosti pri zelo nizkih temperaturah omogočajo, da se v mešanicah uporablja za taljenje ledu na betonskih cestah v zelo hladnih podnebjih. Po mnenju virov, ki so se posvetovali, se uporablja tudi v opremi za boj proti požarom in sklopom za opazovanje celic v mikroskopih.
[TOC]
Struktura
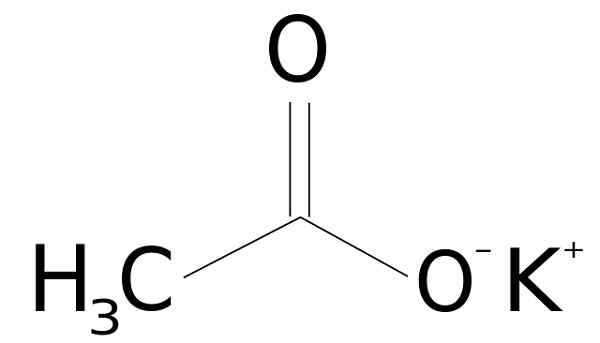
Kalijev acetat tvori kalijev kation k+ in anion acetat cho3COO-. Slednje je konjugirana podlaga ocetne kisline CH3COOH. Acetat cho3COO- je sestavljen iz metil -ch3 skupaj s karboksilatom -coo-.
Zveza med obema ionoma je elektrostatična ali ionska, to je zveza med pozitivnim in negativnim ionom.
 Kalijev acetat struktura ch3Kuhar. Sssilver [javna domena]. Vir: Wikimedia Commons.
Kalijev acetat struktura ch3Kuhar. Sssilver [javna domena]. Vir: Wikimedia Commons. Nomenklatura
- Kalijev acetat
- Kalijev etanoat
- Kalijeva sol ocetne kisline
- Acok
- Koac
Lastnosti
Fizično stanje
Brezbarvna trdna ali kristalno bela.
Molekularna teža
98,14 g/mol
Tališče
292 ° C
Gostota
1,6 g/cm3
Topnost
Zelo topno v vodi: 256 g/100 ml pri 20 ° C.
ph
5% vodna raztopina kalijevega acetata ima pH 7,5-9,0.
Druge lastnosti
Včasih ima šibek vonj kisa. V 10% raztopini ne napade aluminija pri sobni temperaturi, ampak pri 60-70 ° C kovina zatemni in trpi ugrize.
V koncentracijah 20% ali več se površinski napad na aluminij pojavi pri kateri koli temperaturi.
Vam lahko služi: HydraceKalijev acetat (ACOK) je zelo topen v vodi. Ima hidrat: kch3COO.1.5H2Ali, ki je trdna snov, ki jo dobimo s kristalizacijo iz vodnih raztopin ACOK.
Vedenje pri segrevanju
Če se kalijev acetat (ACOK) (KCH (KCH) predloži ogrevanju (KCH3COO.1.5H2O) Po doseganju 40 ° C se hidracijska voda začne izgubljati.
Kch3COO.1.5H2O → kch3COO + 1,5H2Ali ↑
Če se brezvodni kalijev acetat segreje (brez vode: KCH3COO), ko doseže 340 ° C, začne razpadati, ki tvori kalijev karbonat K2Co3 Glede na naslednjo reakcijo:
2 kch3COO + 4 o2 → k2Co3 + 3 h2O + 3 co2↑
Pridobivanje
Pripravimo ga lahko z delovanjem Koh kalijevega hidroksida na več spojinah, kot je Cho kislina3COOH, ocetni anhidrid (ch3Co)2O in amonijev acetat cho3Poonh4.
Koh +ch3COOH → Ch3Kuhar + h2Tudi
Dobimo ga lahko tudi z reakcijo kalijevega karbonata K2Co3 o KHCO kalijev bikarbonat3 Z ocetno kislino ch3COOH.
Khco3 + Pogl3COOH → Ch3Kuhar +h2Ali + co2↑
Kalijev acetat lahko kristaliziramo iz vodne raztopine, da ga dobimo z visoko čistostjo.
Prijave
V več aplikacijah
Kalijev acetat se v predelani prehrambeni industriji uporablja kot regulator kislosti. Za merjenje prepustnosti vodne pare se uporablja kot sušilna metoda v kemičnih metodah.
Služi kot dehidrirajoči sredstvo etanola pri proizvodnji tega alkohola, ki temelji na lignocelulozi, materialu, pridobljenem iz lesa.
Uporablja se za proizvodnjo antibiotikov in se pogosto uporablja v gasilski bojni opremi.
V polimerni industriji
Uporablja se za recikliranje poliuretanov, ker služi katalizaciji ali pospeševanju reakcij hidrolize in glikolize takšnih polimerov, da postanejo alkoholi in amini.
Uporablja se tudi pri proizvodnji organskih silikonskih smol.
V znanstvenih in medicinskih raziskovalnih laboratorijih
Kalijev acetat z visoko čistostjo se uporablja v laboratorijih kot analitični kemijski reagent. Tudi za izvajanje medicinskih raziskav.
Vam lahko služi: Neon: Zgodovina, lastnosti, struktura, tveganja, uporabeV histopatoloških laboratorijih služi za zagotavljanje nevtralnega pH medija v sklopih mikroskopa.
 Kalijev acetat ima različne namene v kemijskih in medicinskih raziskovalnih laboratorijih. Avtor: Michal Jarmoluk. Vir: Pixabay.
Kalijev acetat ima različne namene v kemijskih in medicinskih raziskovalnih laboratorijih. Avtor: Michal Jarmoluk. Vir: Pixabay. Uporablja se za sintezo heterocikličnih organskih spojin, ki so spojine s cikli različne velikosti.
Nekatere mikroelektrode, ki služijo za preučevanje električnih lastnosti celic, so napolnjene s koncentrirano raztopino kalijevega acetata.
V industrijski proizvodnji protiteles
Kalijev acetat služi veliki proizvodnji monoklonskih protiteles (ki so tista, ki prihajajo iz iste matične celice) v celičnih kulturah. Omogoča spodbujanje sinteze ali tvorbe protiteles.
Protitelesa so snovi, ki jih proizvajajo nekatere krvne celice za boj proti okužbam z virusom ali bakterijami.
 Slika umetniškega protiteles. KCH natrijev acetat3CO služi pri proizvodnji protiteles v velikih količinah. Blitzkrieg1982 [CC BY-SA (https: // creativeCommons.Org/licence/by-sa/4.0)]. Vir: Wikimedia Commons.Čeprav kalijev acetat (ACOK) zavira ali zavira rast celic in zmanjšuje gostoto celic, se produktivnost protiteles za vsako celico poveča.
Slika umetniškega protiteles. KCH natrijev acetat3CO služi pri proizvodnji protiteles v velikih količinah. Blitzkrieg1982 [CC BY-SA (https: // creativeCommons.Org/licence/by-sa/4.0)]. Vir: Wikimedia Commons.Čeprav kalijev acetat (ACOK) zavira ali zavira rast celic in zmanjšuje gostoto celic, se produktivnost protiteles za vsako celico poveča.
 Napad na protitelesa, ki črpa nekaj bakterij. SA1590 [CC BY-S (https: // creativeCommons.Org/licence/by-sa/4.0)]. Vir: Wikimedia Commons.
Napad na protitelesa, ki črpa nekaj bakterij. SA1590 [CC BY-S (https: // creativeCommons.Org/licence/by-sa/4.0)]. Vir: Wikimedia Commons. V Antihielo mešanicah
Kalijev acetat je bil uporabljen v mešanicah antihielo (angleški prevod Proti iciranju), da jih uporabite za taljenje cestnih in cementnih pločnikov ter tako omogočite varno uporabo le -teh.
 Med zimsko postajo so ceste napolnjene s snegom in ledom. Kalijev acetat je lahko koristen v takih primerih. Avtor: s. Hermann & F. Richter. Vir: Pixabay.
Med zimsko postajo so ceste napolnjene s snegom in ledom. Kalijev acetat je lahko koristen v takih primerih. Avtor: s. Hermann & F. Richter. Vir: Pixabay. Izbira kalijevega acetata (ACOK) za to uporabo je posledica 50% vodne raztopine s težo ACOK je evktika in ima fuzijsko točko -62 ° C. To pomeni, da tudi pri temperaturah, ki so nizke od -62 ° C.
Euttic je homogena mešanica komponent, ki ima najmanjšo talilno točko vseh možnih mešanic, vključno s čistimi komponentami.
Kako deluje kot antihielo
Kalijev acetat (ACOK) ima zelo dobro zmogljivost za taljenje ledu.
A -5 ° C se lahko za vsak kg ACOK stopi 11,5 kg ledu. Ta lastnost se zmanjšuje z znižanjem temperature, vendar ima tudi na -50 ° C možnost, da za vsak kg ACOH tapi 1,3 kg ledu.
Vam lahko služi: kristalne trdne snovi: struktura, lastnosti, vrste, primeriA -5 ° C Ta zmogljivost je primerljiva s sposobnostjo natrijevega klorida ali namizne soli (NACL), medtem ko je od -30 ° C daleč.
 Kalijev acetat vam omogoča, da led stopi na zamrznjenih cestah. Avtor: Markus Sch. Vir: Pixabay.
Kalijev acetat vam omogoča, da led stopi na zamrznjenih cestah. Avtor: Markus Sch. Vir: Pixabay. Vendar pa so v testih, ki so bili izvedeni z ACOK skupaj z drugimi spojinami, opazili določeno stopnjo korozije cementnih površin.
Po drugi strani je mešanica kalijevega acetata (ch3Kuhar) z oblikovanjem kalija (HCOOK) je odličen antihielo in ne potrebuje antikorozivnega.
Reference
- Baker, f.J. et al. (1976). Postopki obarvanja. Vodni montants. V uvodu v medicinsko laboratorijsko tehnologijo (peta izdaja). Okrevano od Scientirect.com.
- Hassan, a.Do. et al. (2018). Inzoli: heterociklizacija, ki tvori sintezo in vez. V napredku v heterociklični kemiji. Okrevano od Scientirect.com.
- Ali.S. Nacionalna knjižnica medicine. (2019). Kalijev acetat. Okrevano od PubChema.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Das, a. in alagirusamy, r. (2010). Prenos vlage. Metoda sušilne obrnjene skodelice. V znanosti v udobju oblačil. Okrevano od Scientirect.com.
- Vargel, c. (2004). Karboksilne kisline in njihovi derivati. Acetate. V koroziji aluminija. Okrevano od Scientirect.com.
- Cuevas, j. (2014). Elektrofiziološke tehnike snemanja. Medcelične tehnike snemanja. V referenčni modulaciji v biomedicinskih znanostih. Okrevano od Scientirect.com.
- Fink, j.K. (2018). Poli (uretan) s. Recikliranje. Solvoliza. V reaktivnih polimerih: temeljne in aplikacije (tretja izdaja). Okrevano od Scientirect.com.
- Fong, w. et al. (1997). Optimizacija proizvodnje monoklonskih protiteles: kombinirani učinki kalijevega acetata in perfuzije v mešanem rezervoarju. Citotehnologija 24: 47–54. Povezava je bila obnovljena.Springer.com.
- Danilov, v.Str. et al. (2012). Nizkotemperaturne reagente proti zapisovanju v vodnih solnih sistemih, ki vsebujejo acetate in formate. Teoretični temelji kemijskega inženirstva, 2012, Vol 46, št. 5, str. 528-535. Povezava je bila obnovljena.Springer.com.
- Lažni, a.Do.et al. (2012). Raziskave in razvoj metode za kalijev acetat visoke čistosti. Journal of Applied Chemistry, 2012, Vol. 85, ne.12, str. 1807-1813. Povezava je bila obnovljena.Springer.com.
- « Magnetni udarni enote, formule, izračun, primeri
- Značilnosti vhodne naprave, kakšne so uporabe, tipi, primeri »

