Železni oksid

- 1662
- 480
- Mr. Shane Larkin
 Železni oksid je kemična spojina med železom in kisikom
Železni oksid je kemična spojina med železom in kisikom Kaj je železni oksid?
On železni oksid To je katera od spojin, ki nastane med železom in kisikom. Zanje je značilno, da so ionski in kristalni, ležijo pa raztreseni kot posledica erozije njihovih mineralov, sestavljanja tal, rastlinskih mase in celo notranjosti živih organizmov.
To je ena od družin spojin, ki prevladujejo v zemeljski skorji. Železni oksidi so znani do danes, večina pa je naravnega izvora in drugih sintetiziranih pod ekstremnim tlakom ali temperaturnim pogojem.
Na zgornji sliki je prikazan del železovega oksida v prahu. Njegova značilna rdeča barva zajema železo več arhitekturnih elementov v tem, kar je znano kot Rust. Prav tako ga opazimo na pobočjih, gorah ali tleh, pomešanih z mnogimi drugimi minerali, kot je rumeni prah goethite (α-feooh).
Najbolj znani železovi oksidi so hematit (α-FE2Tudi3) in maghemita (ϒ-FAITH2Tudi3), oba polimorfa železovega oksida; In nenazadnje, magnetit (vera3Tudi4).
Njihove polimorfne strukture in njegovo veliko površinsko območje so narejene z zanimivimi materiali, kot je Sorbentes, ali za sintezo nanodelcev s širokimi aplikacijami.
Struktura železovih oksidov
Zgornja slika je reprezentacija kristalne strukture grdega, enega od železnih oksidov, kjer ima železo valenco +2. Rdeče sfere ustrezajo anionom oz2-, Medtem ko rumene do vere2+.
Upoštevajte, da vsaka vera2+ je obdan s šestimi oz2-, oblikovanje oktaedrske koordinacijske enote.
Zato lahko grda struktura v grdih enotah "sesuje"6, Kjer je osrednji atom vera2+. V primeru oksihidroksidov ali hidroksidov je oktaedrska enota grda3(OH)3.
Vam lahko služi: kalcijev peroksid (caO2): lastnosti, tveganja in uporabeV nekaterih strukturah namesto oktaedra obstajajo tetraedrske enote, grde4. Zaradi tega so železovi oksidi običajno predstavljeni z oktonico ali tetraedri z železnimi središči.
Strukture železovih oksidov so odvisne od tlačnih ali temperaturnih pogojev, od vere/ali razmerju (torej koliko kisika je za železo in obratno) ter Valencia del Hierro (+2, +3 in, zelo redko v sintetičnih oksidih , +4).
Na splošno veliki anioni oz2- Poravnajo oblikovanje listov, katerih luknje gostijo vere kations2+ ali vera3+. Tako obstajajo oksidi (na primer magnetit), ki imajo likalnike z obema valencami.
Polimorfizem
Železni oksidi imajo polimorfizem, to je različne strukture ali kristalne ureditve za isto spojino. Železni oksid, vera2Tudi3, ima do štiri možne polimorfe. Hematit, α-Fe2Tudi3, Je najbolj stabilen od vseh; sledi Maghemita, ϒ-Faith2Tudi3, in za sintetično β-vero2Tudi3 in ε- vera2Tudi3.
Vsi imajo svoje vrste kristalnih struktur in sistemov. Vendar delež 2: 3 ostane konstanten, zato obstajajo trije anioni oz2- Za vsaka dva kationa vera3+.
Razlika je v tem, kako se nahajajo grde oktaedrske enote6 v vesolju in kako se združijo.
Strukturne povezave
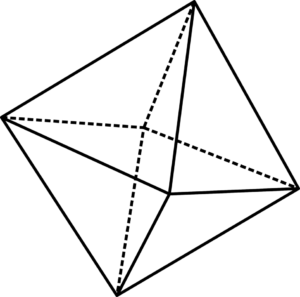 Grda oktaedralna enota6
Grda oktaedralna enota6 Grde oktaedrske enote6 lahko vizualiziramo s pomočjo nadrejene slike. V vogalih oktaedra so oz2-, Medtem ko je v središču vera2+ ali vera3+(V primeru vere2Tudi3). Način, kako so te oktaede razporejene v vesolju, razkriva strukturo rje.
Vendar vplivajo tudi na to, kako so se povezali. Na primer, dve oktahedri se lahko pridružita dvema njunima točkama, kar je predstavljeno s kisikovim mostom: Fe-O-Fe. Podobno se lahko oktahedra pridruži skozi robove (ob drugem). Nato bi bil predstavljen z dvema kisikovih mostovih: Fe- (O)2-Vera.
Vam lahko služi: klor oksid (v): lastnosti, struktura, uporabeIn končno lahko oktaedra komunicirajo skozi njihove obraze. Tako bi bila reprezentacija zdaj s tremi mostovi kisika: Fe- (O)3-Vera. Način, kako so oktaedre povezane, bi se med internuklearnimi razdaljami Fe -fe razlikovali in s tem fizikalne lastnosti oksida.
Lastnosti železovih oksidov
Železni oksid je spojina z magnetnimi lastnostmi. To so lahko anti, feroro ali ferimagnetni in so odvisni od valen vere in kako kationi sodelujejo v trdnem delu.
Ker so trdne strukture zelo raznolike, na enak način so njihove fizikalne in kemijske lastnosti.
Na primer polimorfi in hidrati vere2Tudi3 Imajo različne vrednosti tališč (ki segajo med 1.200 in 1.600 ° C) in gostote. Vendar imajo malo topnosti, ki sledijo vere3+, Ista molekularna masa je rjavih barv in se komaj raztopi v kislih raztopinah.
Nomenklatura železovih oksidov
IUPAC nastavi tri načine, kako poimenovati železov oksid. Tri so zelo koristne, čeprav za zapletene okside (na primer vera7Tudi9) Sistematika nad drugimi ureja zaradi svoje preprostosti.
Sistematična nomenklatura
Številke kisika in železa se upoštevajo, pri čemer jih poimenujemo s predponami mono-mono-, di-, tri- itd. Po tej nomenklaturi vera2Tudi3 je poklican: Trioksid dallikalnik. In za vero7Tudi9 Njegovo ime bi bilo: Heptahierro noneasid.
Nomenklatura zalog
To upošteva Valencia del Hierro. Če je to vera2+, Iron oksid je napisan ... in njena valenca z rimskimi številkami, zaklenjenimi v oklepajih. Za vero2Tudi3 Njegovo ime je: železov oksid (iii).
Vam lahko služi: parni tlak: koncept, primeri in vaje rešeneUpoštevajte to vero3+ Določi ga lahko algebrske vsote. DA2- Ima dve negativni naboji in tri sta, dodajte -6. Za nevtralizacijo tega -6 potrebujejo +6, vendar obstajata dve veri, tako da ju morata razdeliti z dvema, +6/2 = +3:
2x (kovina valencia) + 3 (-2) = 0
Preprosto čiščenje valence vere v oksid. Če pa X ni celo število (kot pri skoraj vseh preostalih oksidih), potem obstaja mešanica vere2+ in vera3+.
Tradicionalna nomenklatura
Pripona -ico je podeljen predpona Ferr-, ko ima vera Valencia +3, in -tako, ko je valencia 2+. Tako vera2Tudi3 se imenuje: železni oksid.
Železni oksidi uporabljajo
Nanodelci
Železni oksidi imajo visoko energijo kristalizacije, ki omogoča ustvarjanje zelo majhnih kristalov, vendar z veliko površino.
Zaradi tega so zelo zanimivi za polja nanotehnologije, kjer oblikujejo in sintetizirajo oksidno nanodelce (NP) za posebne namene:
- Kot katalizatorji.
- Kot rezervoar z zdravili ali geni v telesu.
- Pri zasnovi senzoričnih površin za različne vrste biomolekul: beljakovine, sladkorji, maščobe.
- Za shranjevanje magnetnih podatkov.
Pigmenti
Ker so nekateri oksidi zelo stabilni, služijo za barvanje tekstila ali dajejo svetle barve površinam katerega koli materiala. Iz mozaikov tal -rdečih, rumenih in oranžnih (celo zelenih) slik -, plastike, usnja do arhitekture.
Reference
- Skrbniki Dartmouth College (18. marec 2004). Stoihiometrija železovih oksidov. Vzet od: Dartmouth.Edu
- Ryosuke sinmyo et al. (8. septembra 2016). Odkritje fe7Tudi9: Nov železov oksid s kompleksno monoklinično strukturo. Okrevano od: Narava.com
- M. Cornell, u. Schwertmann. Železni oksidi: struktura, lastnosti, reakcija, pojavi in uporabe [PDF]. Wiley-VCH. Vzet od: epsc511.Wustl.Edu

