Berlijev oksid (Beeo)
- 3660
- 123
- Raymond Moen
 Kemična struktura beril oksida
Kemična struktura beril oksida Kaj je beril oksid?
On Berlijev oksid (Beeo) je keramični material, ki ima poleg visoke trdnosti in električne upornosti tako visoko zmogljivost toplotne prevodnosti, da so del jedrskih reaktorjev, celo presegajo kovine v tej zadnji nepremičnini.
Poleg svoje uporabnosti kot sintetičnega materiala ga lahko najdemo tudi v naravi, čeprav je redko. Njegovo upravljanje je treba izvesti skrbno, saj ima sposobnost resno poškodovanja zdravja ljudi.
V sodobnem svetu so opazili, kako so znanstveniki, povezani s tehnološkimi podjetji.
Rezultat tega je bilo odkritje snovi, ki so nam zaradi izjemno uporabnih lastnosti in njihove visoke vzdržljivosti omogočile napredovanje sčasoma, kar nam je omogočilo, da našo tehnologijo dosežemo na višji ravni.
Kemična struktura beril oksida
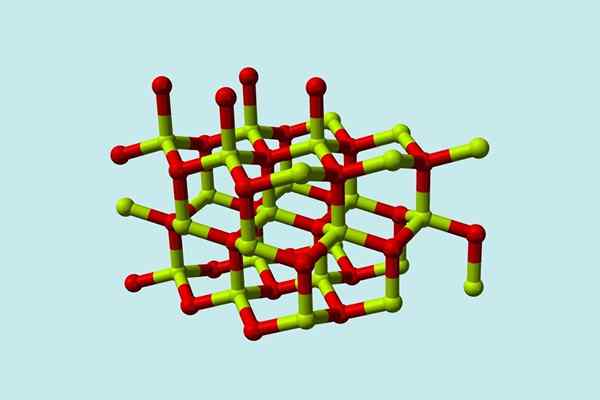
Molekula beril oksida (imenovana tudi Berilia) Sestavljen je iz atoma berilija in enega kisika, oba usklajena v tetraedrski orientaciji, in kristalizira v šestkotni kristalni strukturi, imenovani Wurtzitas.
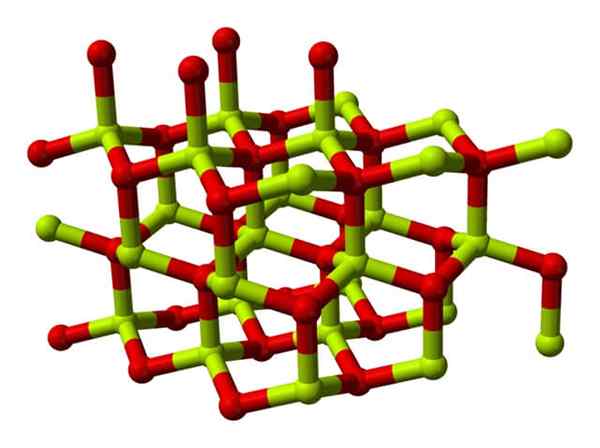 Model kristalne strukture beril oksida. Vir: Wikimedia Commons
Model kristalne strukture beril oksida. Vir: Wikimedia Commons Ti kristali imajo tetraedrska središča, ki jih zaseda2+ jaz2-. Pri visokih temperaturah struktura berilijevega oksida postane tetragonalni tip.
Pridobivanje berilnega oksida dosežemo s tremi metodami: kalcinacija beril ogljika, dehidracija berilnega hidroksida ali z vžigom kovinskega berilija. Berlijev oksid, ki nastane pri visokih temperaturah, je inerten, vendar ga lahko raztopi več spojin.
Vam lahko služi: klorogena kislinaBeco3 + Toplota → čebela + co2 (Kalcinacija)
Biti (oh)2 → Beeo + H2O (dehidracija)
2 Be + oz2 → 2 Beeo (vžig)
Končno lahko berilijev oksid izhlapimo in v tem stanju bo predstavljen v obliki diatomskih molekul.
Lastnosti Breary Oxide
Berillijev oksid je v naravi predstavljen kot bromellita, beli mineral, ki ga najdemo v nekaterih zapletenih nahajališčih mangana-hidrero, vendar ga pogosteje najdemo v svoji sintetični obliki: bela amorfna trdna snov, ki se pojavlja v obliki prahu.
Tudi nečistoče, ki so bile ujete med proizvodnjo.
Njegova tališča se nahaja v 2.507 ° C, njegova vrelišče v 3.900 ° C in ima gostoto 3,01 g/cm3.
Podobno je njegova kemična stabilnost znatno visoka, le reagira z vodno paro pri temperaturah blizu 1.000 ° C in lahko prenese procese zmanjšanja ogljika in napade na staljene kovine pri visokih temperaturah.
Poleg tega je njegova mehanska odpornost spodobna in jo je mogoče izboljšati z dizajni in ustrezno proizvodnjo za komercialne namene.
Električna prevodnost
Berillijev oksid je izjemno stabilen keramični material, zato ima precej visoko električno upornost, zaradi česar je eden najboljših električnih izolacijskih materialov, skupaj z glinico.
Zaradi tega se običajno uporablja za visokofrekvenčno specializirano električno opremo.
Toplotna prevodnost
Berillijev oksid ima veliko prednost pri svoji toplotni prevodnosti: znan je kot drugi najboljši toplotni prevodni material med ne -kometami, ki ga premagajo le diamant, precej dražji in redek material.
Vam lahko služi: tiolesKar zadeva kovine, samo baker in srebro bolje prenašata toploto z vožnjo kot berilijevi oksidi, zaradi česar je zelo zaželen material.
Ta snov je bila zaradi odličnih lastnosti toplotnega ravnanja vključena v proizvodnjo ognjevzdržnih materialov.
Optične lastnosti
Zaradi istih kristalnih lastnosti se za uporabo prozornega materiala na ultravijolični zasloni in fotonapetostnim celicam uporablja berilijev oksid.
Prav tako se lahko pojavijo zelo kakovostni kristali, zato se te lastnosti izboljšajo glede na uporabljeni proizvodni postopek.
Zdravstvena tveganja
Berillijev oksid je spojina, ki jo je treba manipulirati z veliko previdno, saj ima najprej rakotvorne lastnosti, ki so bile povezane z neprekinjenim vdihavanjem praškov ali hlapov tega materiala.
Majhni delci v teh fazah oksida se oprimejo pljuč in lahko ustvarijo tvorbo tumorjev ali bolezni, znano kot bellioza.
Berilaiosis je bolezen s srednjo stopnjo umrljivosti, ki povzroča neučinkovito dihanje, kašelj, izgubo teže in vročino ter tvorbo granulomov v pljučih ali drugih prizadetih organih.
Obstajajo tudi nevarnosti, da bi se s kožo usmeril v stik z berilijevim oksidom, saj je jedko in razdražljivo ter lahko poškoduje površino kože in sluznice. Dihalne ceste in roke je treba zaščititi pri delu s tem materialom, zlasti v njihovi obliki prahu.
Uporablja berilijev oksid
Uporaba beril oksida so razdeljena predvsem na tri: elektronske aplikacije, jedrske in druge.
Vam lahko služi: kaj je erristeneo?Elektronske aplikacije
Sposobnost prenosa toplote na visoko raven in njena dobra električna upornost je zaradi toplotnega disipatorja pridobila veliko koristnost kot toplotni disipator.
Njegova uporaba v vezjih znotraj računalnikov z visoko zmogljivostjo je bila dokazana, poleg opreme, ki obravnava visoke električne tokove.
Berillijev oksid je prozoren za x -rays in mikrovalovno pečico, zato se uporablja v oknih proti tem vrstam sevanja, poleg antene, komunikacijskih sistemov in mikrovalovnih pečic.
Jedrske aplikacije
Njegova sposobnost zmernega nevtronov in vzdrževanja njihove strukture pod sevalnim bombardiranjem.
Druge aplikacije
Nizka gostota berilijevega oksida je vzbudila zanimanje za vesoljsko in vojaško tehnološko industrijo, saj lahko v motorjih za rakete in Antibala v jopiču predstavlja možnost nizke teže.
Končno se je v zadnjem času uporabil kot ognjevzdržni material pri zlitju kovin v metalurški industriji.
Reference
- Pubchem (s.F.). Berlijev oksid. Pridobljeno iz PubChem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Reade (s.F.). Beryllia/Berlijevi oksid (čebela). Reade iz Readea.com
- Raziskave, c. (s.F.). Berlijev oksid - Beryllia. Pridobljeno iz azoma.com
- Storitve, n. J. (s.F.). Berlijev oksid. Okreval od NJ.Gov
- Wikipedija (s.F.). Berlijev oksid. Pridobljeno iz in.Wikipedija.org

