Tritio
- 1382
- 364
- Ricky Dach
Kaj je tritij?
On Tritio To je ime, ki je bilo dodeljeno enemu od izotopov kemičnega elementa vodika, katerega simbol je običajno t ali 3H, čeprav se imenuje tudi vodik-3. To se pogosto uporablja v velikem številu aplikacij, zlasti v jedrskem polju.
Tudi v tridesetih letih prejšnjega stoletja je ta izotop prvič nastal na podlagi bombardiranja z visokoenergetskimi delci (imenovanimi deuteroni) drugega izotopa istega elementa, imenovanega Deuterium, zahvaljujoč znanstvenikom P. Harteck, m. L. Oliphant in E. Rutherford.
Ti raziskovalci kljub njihovim esejem niso bili uspešni pri izolaciji tritija, ki so pokazali konkretne rezultate v rokah Cornoga in Álvareza, kar je odkrilo radioaktivne lastnosti te snovi.
Na tem planetu je proizvodnja tritija izjemno redka narave, ki izvira le v tako majhnih razmerjih, ki jih sledi upoštevajo z atmosferskimi interakcijami s kozmičnim sevanjem.
Tritio struktura
Ko govorimo o tritijevi strukturi, je prva stvar, ki jo je treba opaziti.
Ta izotop ima fizikalne in kemijske lastnosti, ki ga razlikujejo od drugih izotopskih vrst od vodika, kljub strukturnim podobnostim.
Poleg atomske teže ali mase približno 3 g, ta manifestna radioaktivna snov, katere kinetične značilnosti kažejo približno 12,3 leta pol življenja.

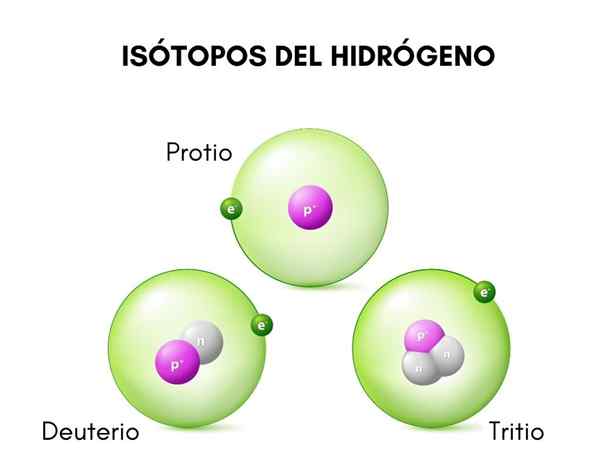
Na zgornji sliki primerjamo strukture treh znanih izotopov vodika, imenovane Proto (vrsta večje številčnosti), devterij in tritij.
Lahko vam služi: križarjenje po lončku: značilnosti, funkcije, uporabite primereStrukturne značilnosti tritija mu omogočajo, da soobstaja z vodikom in devterijem v vodi, ki izvira iz narave, katere proizvodnja je morda posledica interakcije med kozmičnim sevanjem in dušikom atmosferskega izvora.
V tem smislu je ta snov predstavljena v vodi naravnega izvora v deležu 10-18 v zvezi z navadnim vodikom; to je zelo majhno obilje, ki ga je mogoče prepoznati le kot sledi.
Nekaj podatkov o tritiju
Zaradi velikega znanstvenega interesa za radioaktivne in porabe energije, ki jih predstavlja, je bilo raziskanih in uporabljenih več načinov za izdelavo tritija, ki jih predstavlja.
Na ta način naslednja enačba kaže na splošno reakcijo, s katero se pojavlja ta izotop, od bombardiranja devterijskih atomov z visoko energijskimi deuteroni:
D + D → T + H
Izvaja se lahko tudi kot eksotermična ali endotermična reakcija s postopkom, imenovanim nevtronska aktivacija nekaterih elementov (na primer litij ali borov), in odvisno od elementa, ki se zdravi.
Poleg teh metod lahko Tritio redko od jedrske cepitve, ki je sestavljena iz delitve jedra atoma, ki velja za težko (v tem primeru izotopov urana ali plutonije energije.
V tem primeru je pridobitev tritio podana kot zavarovalni ali s proizvodnimi proizvodi, vendar ni namen tega mehanizma.
Z izjemo postopka, ki je bil prej opisan, se vsi ti proizvodni procesi te izotopske vrste izvajajo v jedrskih reaktorjih, v katerih so pogoji vsake reakcije.
Vam lahko postreže: Pyrex GlassTritio Lastnosti
- Proizvaja ogromno energije, ko izvira iz devterije.
- Predstavlja radioaktivne lastnosti, ki še naprej vzbujajo znanstveno zanimanje za raziskave jedrske fuzije.
- Ta izotop je v molekularni obliki predstavljen kot t2 tudi 3H2, katere molekulska teža je približno 6 g.
- Podobno kot Protio in Deuterium ima ta snov težave pri zaprtju.
- Ko je ta vrsta kombinirana s kisikom, izvira oksid (predstavljen kot t2O) ki je v tekoči fazi in je splošno znana kot voda Superpesada.
- Zlitje z drugimi svetlobnimi vrstami je sposoben doživeti lažje, kot je prikazan navaden vodik.
- Predstavlja nevarnost za okolje, če se množično uporablja, zlasti v reakcijah fuzijskih procesov.
- Lahko se tvori s kisikom še eno snov, znano kot pol -perpetirana voda (predstavljena kot HTO), ki je tudi radioaktivna.
- Velja za nizkoenergijski generator delcev, znan kot beta sevanje.
- Ko so predstavljeni primeri zdrobljene porabe vode, je bilo ugotovljeno, da se njegovo polovico v telesu vzdržuje v območju od 2,4 do 18 dni, nato pa se izloči.
Uporaba/aplikacije
Med aplikacijami Tritium so procesi, povezani z reakcijami jedrskega tipa. Nato je prikazan seznam z najpomembnejšo uporabo:
- Na območju radioluminiscence se Tritium uporablja za izdelavo instrumentov, ki omogočajo osvetlitev, zlasti nočno, v različnih napravah za komercialno uporabo, kot so ure, noži, strelno orožje, med drugim prek samo -hrane.
Lahko vam služi: cerio oksid (iv): struktura, lastnosti, uporabe- Na področju jedrske kemije se tovrstne reakcije uporabljajo kot vir energije pri proizvodnji jedrskega in termonuklearnega orožja, poleg tega pa se uporabljajo v kombinaciji z deuterijem za jedrske fuzijske procese, ki so pod nadzorom.
- Na področju analitične kemije lahko ta izotop uporabimo v postopku radioaktivnega označevanja, kjer je Tritio nameščen v določeno vrsto ali molekulo in lahko spremljate študije, ki jih želite izvajati pri tem.
- V primeru biološkega okolja se Tritij uporablja kot prehodni sledilnik v oceanskih procesih, kar omogoča preiskavo evolucije oceanov na zemlji v fizikalni, kemični in celo biološki sferi.
- Med drugimi aplikacijami je bila ta vrsta uporabljena za izdelavo atomske baterije za proizvodnjo električne energije.

