Struktura aluminijevega sulfida (AL2S3), lastnosti, uporabe
- 1816
- 125
- Percy Feeney
On Aluminijast sulfid (Do2S3) Gre za svetlo sivo kemično spojino, ki jo tvori oksidacija kovinskega aluminija, ko izgubljajo elektrone zadnje stopnje energije in postanete kation ter z zmanjšanjem nemetalnega žvepla.
Da se to zgodi in aluminij lahko prinese svoje elektrone, je potrebno, da predstavite tri hibridne orbitale sp3, ki dajejo možnost oblikovanja povezav do elektronov iz žvepla.
Občutljivost za vodni aluminijast sulfid pomeni, da lahko v prisotnosti vodne pare, ki jo najdemo v zraku3), vodikov sulfid (h2S) in vodik (h2) plinasto; Če se slednji kopiči, lahko povzroči eksplozijo. Zato je treba aluminijevo sulfidno embalažo opraviti s hermetičnimi posodami.
Po drugi strani pa, ker ima aluminijev sulfid reaktivnost z vodo, je to element, ki nima topila za topilo.
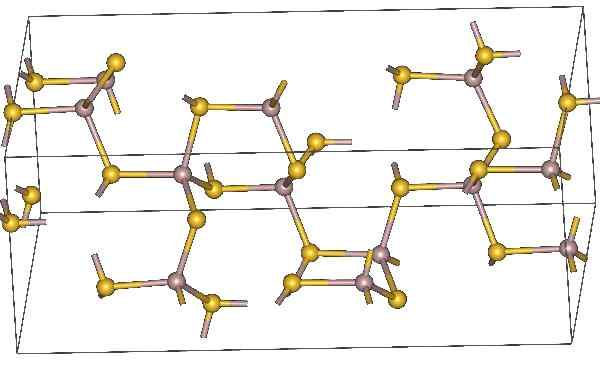
Kemična struktura
 Kemična struktura aluminijevega sulfida. Rumeni atomi predstavljajo žveplo. Vir: MaterialScientist, CC BY-SA 3.0, prek Wikimedia Commons
Kemična struktura aluminijevega sulfida. Rumeni atomi predstavljajo žveplo. Vir: MaterialScientist, CC BY-SA 3.0, prek Wikimedia Commons Molekularna formula
Do2S3
Strukturna formula
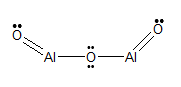 Nomenklatura
Nomenklatura
- Aluminijast sulfid.
- Di aluminijast trisulfid.
- Aluminijev sulfid (III).
- Aluminijev sulfid.
Lastnosti aluminija sulfida
 Videz aluminijevega sulfida
Videz aluminijevega sulfida Kemične spojine imajo večinoma dve vrsti lastnosti: fizikalne in kemične.
Fizične lastnosti
Molarna masa
150,158 g/mol
Gostota
2,02 g/ml
Tališče
1100 ° C
Topnost vode
Nerešljiv
Kemične lastnosti
Ena glavnih reakcij aluminijevega sulfida je z vodo, kot sta substrat ali glavni reaktivni:

V tej reakciji lahko opazimo tvorbo aluminijevega hidroksida in na vodikovega sulfida, če je v obliki plina ali sulfidne kisline, če se raztopi v vodi v obliki raztopine. Njegova prisotnost je prepoznan z vonjem gnilo jajc.
Vam lahko služi: kemične rešitveUporaba in aplikacije
V super kartici
Aluminijev sulfid se uporablja pri proizvodnji struktur nano mrež, ki izboljšujejo specifično površinsko površino in električno prevodnost, tako da je mogoče doseči visoko kapacitivnost in gostoto energije.
Grafenski oksid (GO) - Graphene je ena od alotropnih oblik ogljika - je služil kot aluminijasta sulfidna podpora (Al2S3) S hierarhično morfologijo, podobno kot nanorambután, izdelana po hidrotermalni metodi.
Dejanje grafenskega oksida
Značilnosti grafenskega oksida kot podpore, pa tudi visoka električna prevodnost in površino naredijo nanorambutan2S3 biti elektrokemično aktivni.
Specifične krivulje CV kapacitivnosti z dobro definiranimi redoks vrhovi potrjujejo psevdokapativno vedenje nanorambutana2S3 Hierarhični, vzdržen v grafenskem oksidu v elektrolitu NaOH 1M. Specifične vrednosti CV kapacitivnosti, pridobljene iz krivulj, so: 168,97 pri hitrosti raziskovanja 5mV/s.
Poleg tega so opazili dober galvanostatični čas praznjenja 903 µs, kar je velika specifična kapacitivnost 2178,16 do toka 3 Ma/cm toka2. Gostota energije, izračunana iz galvanostatskega izpusta, je 108,91 WH/kg, do trenutne gostote 3 Ma/cm2.
Elektrokemijska impedanca tako potrjuje psevdokapaktivno naravo hierarhične nanorambutanske elektrode do2S3. Test stabilnosti elektrode kaže 57,84 % zadrževanje specifične kapacitivnosti do 1000 ciklov.
Eksperimentalni rezultati kažejo, da nanorambutane2S3 Hierarhična je primerna za aplikacije za nadzor.
Vam lahko služi: kromijev hidroksid: struktura, lastnosti, sinteza, uporabaV sekundarnih litijevih baterijah
Z namenom razviti sekundarno litijevo baterijo z visoko energijsko gostoto so preučevali aluminijev sulfid (Al2S3) kot aktivni material.
Začetni ukrep zmogljivosti za prenos2S3 Je bilo približno 1170 mAh g-1 do 100 m g-1. To ustreza 62 % teoretične zmogljivosti za sulfid.
Al2S3 Izkazal je slabo zadrževanje zmogljivosti v potencialnem območju med 0,01 V in 2,0 V, predvsem zaradi strukturne nepovratnosti postopka obremenitve ali ekstrakcije Li.
Analiza XRD in K-XES za aluminij in žveplo je pokazala, da je površina Al2S3 med postopki nalaganja in razkladanja reagira reverzibilno, jedro al2S3 Pokazal je strukturno nepovratnost, ker Lial in Li2S so bili oblikovani iz al2S3 V začetnem prenosu in potem so ostali takšni, kot so.
Tveganja
- V stiku z vnetljivimi plini, ki lahko spontano sproščajo vode.
- Povzroči draženje kože.
- Povzročajo hudo draženje očesa.
- Lahko povzroči draženje dihal.
Informacije se lahko razlikujejo med obvestili, odvisno od nečistoč, dodatkov in drugih dejavnikov.
Postopek prve pomoči
Splošno zdravljenje
Poiščite zdravniško pomoč, če simptomi obstajajo.
Posebno zdravljenje
Nobenega
Pomembni simptomi
Nobenega
Vdihavanje
Vzemite žrtev zunaj. Dobava kisika, če je dihanje težko.
Zaužitje
Upravljajte eno ali dve kozarci vode in sprožite bruhanje. Nikoli ne sprožite bruhanja ali dajanja ničesar v usta nezavedni osebi.
Krzno
Operite prizadeto območje z mehkim milom in vodo. Izbrišite kakršna koli onesnažena oblačila.
Oči
Oči umijte z vodo, pogosto utripajte nekaj minut. Odstranite kontaktne leče v primeru, da jih imate, in še naprej sperite.
Lahko vam služi: križarjenje po lončku: značilnosti, funkcije, uporabite primereUkrepi za gašenje požarov
Vnetje
Ni vnetljivo.
Sredstva izumrtja
Reagirati z vodo. Ne uporabljajte vode: uporabite aparat za apart za pesek in prah.
Boj za boj
Uporabite avtonomni dihalni aparat s popolno zaščito. Nosite oblačila, da se izognete stiku s kožo in očmi.
Reference
- Zdravje in tveganja.com, (s.f), definicija, koncepti in članki o zdravju, tveganjih in okolju. Pridobljeno: zdravje in tveganja.com
- Aluminijast sulfid. (s.F). V wikiwandu. Pridobljeno 9. marca 2018: Wikiwand.com
- Spletni elementi.(s.F).Dialminium trisulpfide, obnovljen 10. marca 2018: WebElements.com
- LTS Research Laboratories, Inc (2016), varnostni podatkovni list aluminijski sulfid: Ltschem.com

