Hipertonska rešitev
- 4878
- 322
- Barry Ernser
Pojasnjujemo, kaj so hipertonične rešitve, njihove značilnosti, kakšne so uporabe, razlike s hipotoniko in dajejo več primerov
Mnogi bodo presenečeni, ko bodo vedeli, da način, kako rastline absorbirajo vodo skozi korenine in način, kako se prsti rok nagubajo, ko se kopajo v morski vodi, so tesno povezane.
Obe se zgodita zahvaljujoč obstoju membrane, ki deluje kot filter, in hipertonično rešitev, ki dobesedno sesa vodo skozi njega. Kaj pa je hipertonska rešitev?
V tem članku bo odgovorjeno na to vprašanje in predstavljene bodo tudi najpomembnejše značilnosti hipertonskih rešitev, za kaj so, kako se razlikujejo od drugih vrst rešitev in nekaj primerov istega.
Kaj je hipertonska rešitev?
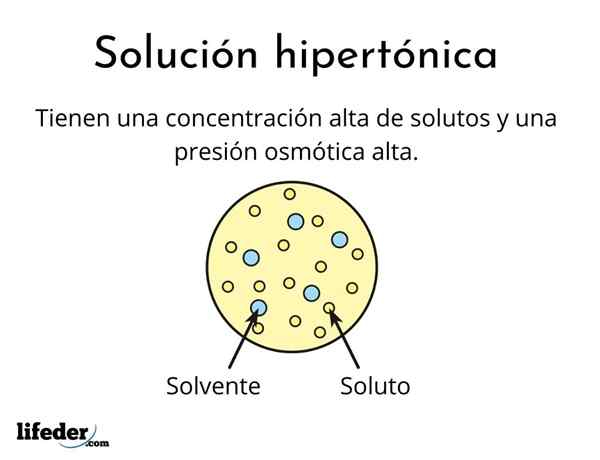
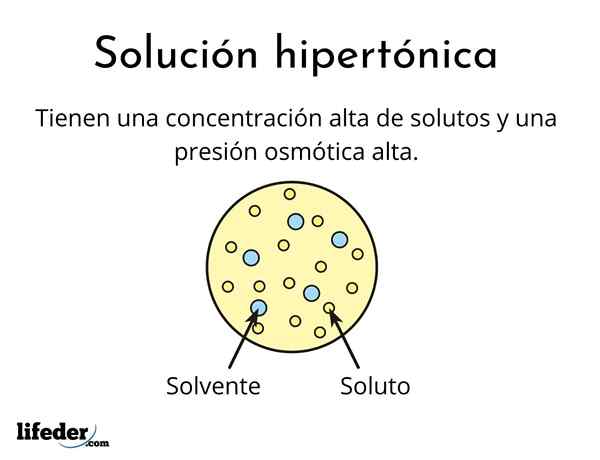
A hipertonska rešitev To je ena, ki vsebuje skupno koncentracijo osmolalno aktivnih topljencev, večje od koncentracije druge referenčne raztopine. Osmolarno aktivno pomeni, da topilo ne more prečkati posebne vrste membrane (podobne tkanini), ki deluje kot cedilo ali filter, to je, naj voda prehaja in ne na delce topljencev.
Ta visoka koncentracija topljencev povzroči, da imajo hipertonične raztopine visok osmotski tlak. Ta pritisk je tisto, kar praktično sesa vodo skozi membrano, ki se imenuje osmoza.
Hipertonska beseda izvira iz grške predpone hiper-, kar pomeni "vklopljeno ali nad" in "toni", kar pomeni napetost ali pritisk, zato hipertonic dobesedno pomeni, da "ima večji pritisk ali napetost".
Pomembno je upoštevati, da se v biologiji in medicini pod pogojem, da se govori o hipertonični raztopini, se nanaša na raztopino, ki je bolj koncentrirana od raztopine, ki jo vsebuje kri, ki jo imenujemo krvna plazma.
Značilnosti hipertonskih rešitev
Hipertonske rešitve imajo nekaj osnovnih značilnosti:
Oblikova jih s topilom in vsaj eno topilo
Ni nobena rešitev lahko hipertonična, čeprav je zelo koncentrirana. Topilo ne sme prečkati membrane, medtem ko mora biti voda brez težav prenesti, sicer pa osmotski tlak ne ustvari.
Imajo visoko koncentracijo topljencev
To je tisto, zaradi česar so hipertonične rešitve. Kot smo že omenili, so hipertonske rešitve bolj koncentrirane kot kri.
Lahko vam služi: delna destilacija: postopek, oprema, aplikacije, primeriImajo lahko različne sestave
Hipertonična raztopina lahko vsebuje eno topilo, kot je sol, ali vsebuje mešanico topljencev, kot so soli in sladkorji, na primer.
Solutos so lahko ionski, nevtralni ali oboje
Prodaja vsebuje ione z električnimi naboji, ki jim ne dovolijo, da prečkajo membrano, zato so majhne. Drugi topili nimajo ionov, vendar so veliki in debeli in se ne prilegajo skozi luknje.
Imajo visok osmotski tlak
Kot že omenjeno, imajo hipertonske rešitve osmotski tlak večji od krvi.
Lahko dehidrirajo celice
Hipertonske raztopine izvlečejo vodo iz celic, ki jih puščajo kot rozine. Zato so naše roke in noge nagubane, ko se kopamo na plaži.
Za kaj so hipertonične rešitve?
Hipertonične rešitve imajo številne namene v vsakdanjem življenju in tudi v medicini. Nekatere najpogostejše uporabe so:
Uporabljajo se za ohranjanje hrane
- Primer: Breskve v sirupu ne gnile, ker ima sirup veliko raztopljenega sladkorja in je zelo hipertonična raztopina. Z dehidrirajočimi celicami hipertonične raztopine ne dovoljujejo gliv in bakterij v hrani, ker umrejo od žeje. To omogoča, da živila traja več.
Služijo za zmanjšanje vnetja
- Primer: Ko ima nekdo nesrečo in udari po glavi, je v možganih velikokrat vnetje. Za zdravljenje pacienta zdravniki vbrizgajo 7,5% raztopino raztopine soli. Ta rešitev praktično sesa vodo, kar zmanjšuje vnetje v možganih.
Služijo za zamenjavo elektrolitov.
- Primer: natrij je elektrolit, ki ga moramo živeti, in ko ima bolnik malo natrija v krvi, se vbrizga 7,5% fiziološka raztopina, da se natrije izgubljeni natrij.
Uporabljajo se za parenteralno hrano
- Primer: Ko ljudje ne morejo jesti skozi usta ali skozi cev, se hranijo v hipertonični raztopini, ki vsebuje vrsto sladkorja, imenovano glukoza.
Razlike s hipotoničnimi in izotoničnimi rešitvami
Tako kot obstajajo hipertonične rešitve, obstajajo tudi hipotonične in izotonične rešitve. Razlika med slednjo in hipertoničnimi rešitvami je njegova koncentracija. Hipotonične raztopine so tiste, ki so manj koncentrirane kot kri, in izotonične imajo enako koncentracijo kot kri.
Na primer, čista voda, saj nima nič topne, je hipotonična, kokosova voda.
Poleg tega, da se razlikujejo po njihovi koncentraciji, se hiper, hipo in izotonične raztopine razlikujejo v načinu, kako vplivajo na celice.
Naslednja slika prikazuje učinek različnih vrst raztopin na rdeče krvne celice (majhne celice, zaradi katerih je kri rdeča).
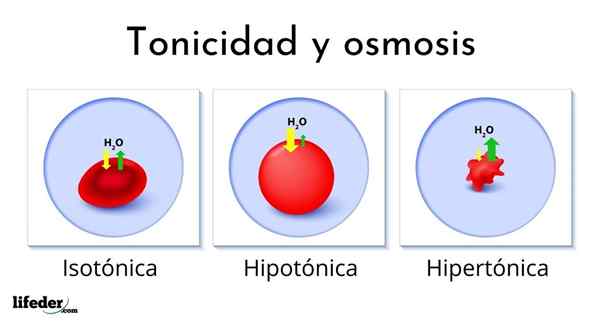
Če se rdeče krvne celice vnesejo v hipertonično raztopino, izvleče vodo, jih dehidrira in pusti naguban kot prehod.
Po drugi strani pa, če jih vnesejo v hipotonično raztopino, rdeče krvne celice absorbirajo vodo in nabrekne, celo razpoka. Nazadnje, če se vnesejo v izotonično raztopino, bo voda znotraj in zunaj rdečih krvnih celic v ravnovesju, tako da se nič ne zgodi.
Primeri hipertonskih rešitev
Sladkorni sirup
 Breskve v sirupu
Breskve v sirupu Sirup, v katerem se ohranjene breskve in drugo sadje, vsebuje zelo visoke koncentracije sladkorja, zato je hipertonska raztopina.
Slanica
Slanica je raztopina vode in soli z zelo visokimi koncentracijami med 3,5% in 25%, kar lahko postane skoraj 30 -krat bolj koncentrirano kot kri (to je zelo hipertonična).
Kis
Skupni kis je hipertonična raztopina, saj ima koncentracijo med 3% in 5% ocetne kisline. Zmanjšanje balzamičnega kisa je še bolj koncentrirano.
Vam lahko služi: dimetilamin ((CH3) 2NH): struktura, lastnosti, uporabe, tveganjaIsta kri naših žil, potem ko smo se veliko znojili.
Pri vadbi in znojenju telo odpravi vodo in soli, vendar odpravlja več vode kot soli (znoj je hipotoničen), tako da se krvna koncentrira in postane hipertonična.
Morska voda
Morska voda vsebuje veliko raztopljenih soli s skupno koncentracijo približno 3,5%, zaradi česar je hipertonična. Zato nam morska voda nariše prste.
Sladke pijače
Cola pijače in druge sladke pijače lahko vsebujejo do 10% sladkor, pa tudi soli in druge topljene s koncentracijami, večjimi od krvi.
5% raztopina dekstroze in 0,45% natrijevega klorida (d5 ½ ns)
To je primer hipertonične raztopine, ki se uporablja za hranjenje ljudi, ki običajno ne morejo jesti ob ustih.
25% Mannitol
To je rešitev, ki se pogosto uporablja za zdravljenje udarcev na glavi. Je štirikrat bolj koncentriran kot kri.
7,5% fiziološka raztopina
Gre.
Komercialni sokovi
Vsi sokovi, kupljeni v supermarketu in niso naravni, imajo zelo visoko koncentracijo sladkorja, zaradi česar so hipertonični.
Reference
- Sweeney J. Upravljanje hipernatremije. Zdravstvena nega. September 2010; 40 (9): 63.
- Slanica. Wikipedija. 2021. Odvzet od.Wikipedija.org/wiki/slanica.
- Morska voda. Wikipedija. 2021. Odvzet od.Wikipedija.Org/wiki/morska voda.
- Chavaltamrong B, Pidatcha P, Thavisri U. Elektroliti, sladkor, kalorije, osmolarnost in pH pijač in kokosove vode. Javno zdravje jugovzhodne Azije J Trop Med. September 1982; 13 (3): 427–431.
- 5% dekstroza in 0.45% vbrizgavanje natrijevega klorida, USP. FDA. 2006. Vzeti iz AccessData.FDA.Gov/drogsatfda_docs/label/2006/017607S123LBL.PDF.
- Llorente G, Niño MC. Manitol proti hipertonični fiziološki raztopini v nevronesteziji. Kolumbijska revija za anesteziologijo. Januar-marec 2015; 43 (1): 29–39.
- Svetniki mm, e. Zdravljenje akutne laktične acidoze z intravenskim hipertoničnim natrijevim kloridom ali bikarbonatnimi raztopinami, zajebanimi z intrauminalno vodo. Raziskave veterinarskih znanosti. Februar 2020; 128: 24–34.
- Dini-g. E, Abreu-C. JD, López-m. In. Osmolalnost pogostih uživanja pijač. Klinične raziskave. December 2004; 45 (4).

