Renio Discovery, lastnosti, struktura, uporabe

- 3412
- 235
- Barry Ernser
On Renio To je kovinski element, katerega kemični simbol je ponovno in se nahaja v skupini 7 periodične tabele, dva položaja pod manganom. Delite s tem in TechniCio lastništvo več številk ali oksidacijskih stanj, od +1 do +7. Prav tako tvori anion, imenovan Perrenato, zapornik4-, Analogno s permanganatom, MNO4-.
Ta kovina je ena najbolj redkih in redkih narave, zato je njegova cena visoka. Izvleče se kot stranski produkt molibdena in bakra. Ena najpomembnejših lastnosti Renia je njegova visoka tališče, ki ga komaj premagajo ogljik in volframo.
 Kovinska sfera Renio. Vir: Hi-Res Slike kemičnih elementov/cc by (https: // createCommons.Org/licence/by/3.0
Kovinska sfera Renio. Vir: Hi-Res Slike kemičnih elementov/cc by (https: // createCommons.Org/licence/by/3.0 Njegovo odkritje ima sporne in nesrečne odtenke. Ime 'Renio' izhaja iz latinske besede 'Rhenus', kar pomeni Rin, znamenito nemško reko v bližini mesta, kjer so nemški kemiki, ki so izolirali in identificirali ta novi element, deloval.
Renio ima številne namene, med katerimi stoji izpopolnjevanje oktana bencina.
[TOC]
Odkritje
Obstoj dveh težkih elementov s kemičnimi značilnostmi, podobnimi tistim manganom. Vendar do takrat še ni bilo znano, kakšna naj bi bila njihova atomska številka; In bilo je leta 1913, ko je bil predstavljen napoved angleškega fizika Henryja Moseleyja.
Po Moseleyju morata ta dva elementa, ki pripadata Manganovi skupini, imeti atomske številke 43 in 75.
Nekaj let pred tem pa je japonska kemika Masataka Ogawa odkrila domnevni element 43 v vzorcu minerala Torianita. Potem ko je leta 1908 objavil svoje rezultate, je želel ta element krstiti z imenom "Niponio". Na žalost so kemiki takrat pokazali, da Ogawa ni odkrila elementa 43.
Lahko vam služi: cikloalki: kemična struktura, lastnosti, nomenklaturaIn tako so minila druga leta, ko so leta 1925 tri nemške kemike: Walter Noddack, Ida Noddack in Otto Berg, našli Element 75 v vzorcih mineralov Columbita, Gadolinita in Molybdenita. Ti mu je dal ime Renio v čast nemškemu Rin Rin ('rena', v latinščini).
Napaka Masataka Ogawa je bila, da se pri identifikaciji elementa prenaša: Odkril je Renio, ne element 43, imenovan Tecnecio danes.
Renio lastnosti
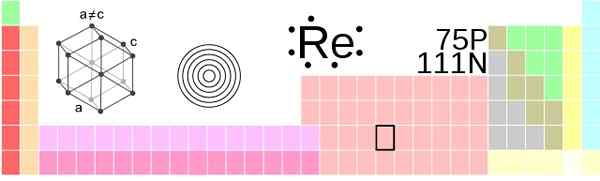 Razmere za renio v periodični tabeli. !Izvirnik: AhoteseierVector: Sushant Savla/CC by-S (https: // createCommons.Org/licence/by-sa/3.0
Razmere za renio v periodični tabeli. !Izvirnik: AhoteseierVector: Sushant Savla/CC by-S (https: // createCommons.Org/licence/by-sa/3.0 Fizični videz
Renio se običajno trži v obliki sivkastega prahu. Njeni kovinski kosi, običajno sferične kapljice, so srebrno sivi, ki so tudi zelo svetli.
Molarna masa
186,207 g/mol
Atomska številka
75
Tališče
3186 ° C
Vrelišče
5630 ° C
Gostota
-Pri sobni temperaturi: 21.02 g/cm3
-Desno na talilni točki: 18,9 g/cm3
Renio je kovina, ki je skoraj dvakrat bolj gosta od istega vodstva. Tako lahko renio krogla, ki tehta 1 gram.
Elektronegativnost
1.9 na lestvici Pauling
Ionizacijske energije
Najprej: 760 kJ/mol
Drugi: 1260 kJ/mol
Tretjič: 2510 kJ/mol
Molarna toplotna sposobnost
25,48 j/(mol · k)
Toplotna prevodnost
48,0 w/(m · k)
Električna upornost
193 nω · m
Mohs trdota
7
Izotopi
Atomi Renio so v naravi predstavljeni kot dva izotopa: 185Re, z obilico 37,4%; in 187Re, z obilico 62,6%. Renio je eden tistih elementov, katerih najpogostejši izotop je radioaktiven; Vendar čas pol življenja 187Re je zelo velik (4,12 · 1010 leta), zato se praktično šteje za stabilno.
Vam lahko služi: nikelj: zgodovina, lastnosti, struktura, uporabe, tveganjaReaktivnost
Kovinski renio je material, odporen na oksidacijo. Ko to stori, njegov oksid, re2Tudi7, Je hlapljivo pri visokih temperaturah in opeklinah z rumenkasto zelenim plamenom. Reniovi deli se upirajo HNO -jevemu napadu3 koncentrirano; Toda vroče, raztopi za ustvarjanje renenske kisline in dušikovega dioksida, ki barvno porjavi raztopino:
Re + 7Hno3 → hreo4 + 7 Ne2 + 3H2Tudi
Reniova kemija je ogromna, saj lahko tvori spojine s širokim spektrom oksidacijskih številk, pa tudi vzpostavi kvadrupolovo vez med dvema atoma renio (štiri kovalentne vezi).
Elektronska struktura in konfiguracija
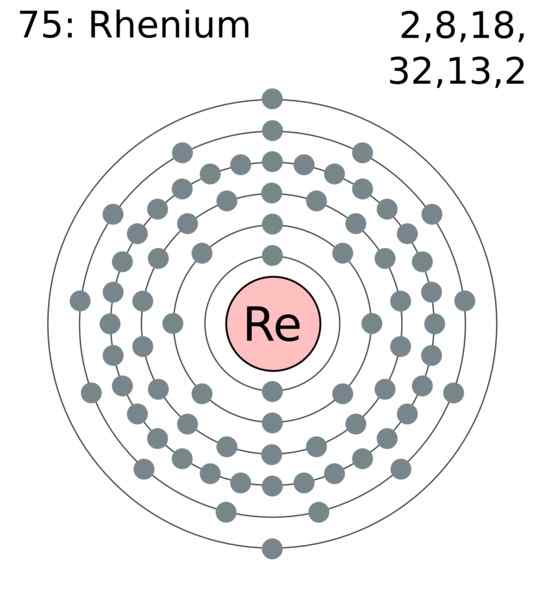 Elektronski sloj Renio. Avtor: Uporabnik: Gregrobson (Greg Robson). Wikimedia Commons
Elektronski sloj Renio. Avtor: Uporabnik: Gregrobson (Greg Robson). Wikimedia Commons Atomi Renio so združeni v svoje kristale, da povzročijo kompaktno šesterokotno strukturo, HCP, za katero je značilno, da je zelo gosta. To se strinja z dejstvom, da je kovina velike gostote. Kovinska povezava, produkt prekrivanja zunanjih orbital, atomi ohranja močno kohezivno.
V tej kovinski povezavi sodelujejo elektroni Valencije, ki so po elektronski konfiguraciji:
[Xe] 4f14 5 d5 6s2
Načeloma je 5D in 6S orbital, ki se prekrivajo, da bi v strukturi HCP kompaktni atomi RE. Upoštevajte, da vaši elektroni dodajo skupno 7, kar ustreza številki vaše skupine v periodični tabeli.
Oksidacijske številke
Elektronska konfiguracija Renio, ko enkrat pogleda, da je njen atom sposoben izgubiti do 7 elektronov, da postane hipotetični kation7+. Ko se domneva obstoj RE7+ V kateri koli renio spojini, na primer v Re,2Tudi7 (Re27+Tudi72-), Pravi se, da ima oksidacijsko številko +7, re (vii).
Druge pozitivne oksidacijske številke za Renio so: +1 (re+), +2 (re2+), +3 (re3+) In tako naprej do +7. Prav tako lahko Renio pridobi elektrone, ki postanejo anion. V teh primerih se reče, da ima negativno oksidacijsko številko: -3 (re3-), -2 (re2-) in -1 (re-).
Lahko vam služi: hidroliza: kaj je to in primeri reakcijPrijave
Bencin
Renio se skupaj s platino uporablja za ustvarjanje katalizatorjev, ki povečujejo stopnjo oktana bencina, hkrati pa zmanjšajo njegovo vsebnost svinca. Po drugi strani so renio katalizatorji namenjeni večkratnim hidrogenacijskim reakcijam, kar je zaradi njihove odpornosti na zastrupitev dušika, fosforja in žvepla.
Ognjevzdržne nadstropje
Renio je ognjevzdržni kovinski izdelek z visoko talilno točko. Zato se dodajajo nikljeve zlitine, da se spremenijo v ognjevzdržne in odporne na velike pritiske in temperature. Te presežne točke se večinoma uporabljajo za oblikovanje turbin in motorjev za vesoljske ladje.
Volframove nitke
Renio lahko oblikuje tudi zlitine z volframom, kar izboljša njegovo duktilnost in zato olajša proizvodnjo filamentov. Te renio-tungstenske filamente se uporabljajo kot rentgenski viri in za zasnovo termokuplanov, ki so sposobne meriti temperature do 2200 ° C.
Prav tako so bile te renio filamente enkrat uporabljene za utripe arhaičnih kamer in trenutno za prefinjene svetilke za opremo; kot je masni spektrofotometer.
Reference
- Shiver & Atkins. (2008). Anorganska kemija. (Četrta izdaja). MC Graw Hill.
- Sarah Pierce. (2020). Renium: uporaba, zgodovina, dejstva in izotopi. Študij. Okrevano od: študij.com
- Nacionalni center za informacije o biotehnologiji. (2020). Renij. Baza podatkov Pubchem., Cid = 23947. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Wikipedija. (2020). Renij. Pridobljeno iz: v.Wikipedija.org
- Doktor. Doug Stewart. (2020). Dejstva o renijevem elementu. Okrevano od: Chemicool.com
- Eric Scerri. (18. november 2008). Renij. Kemija v svojih elementih. Okrevano od: ChemistryWorld.com

