Kakšna je izdaja emisije? (S primeri)
- 4698
- 10
- Don Nitzsche
On Emisijski spekter To je spekter valovnih dolžin svetlobe, ki ga oddajajo atomi in molekule pri prehodu med dvema stanje energije. Bela svetloba ali vidna svetloba, ki vpliva na prizmo, se razgradi na različne barve s specifičnimi valovnimi dolžinami za vsako barvo. Pridobljen barvni vzorec je vidni spekter sevanja, imenovan emisijski spekter.
Atomi, molekule in snovi imajo tudi emisijski spekter zaradi emisije svetlobe, ko absorbirajo ustrezno količino energije v tujini za potovanje med dvema energetskima stanjem. S prehodom te svetlobe skozi prizmo se razgradi v spektralnih barvnih črtah z različnimi valovnimi dolžinami vsakega elementa.
Pomen emisijskega spektra je, da omogoča določitev sestave neznanih snovi in astronomskih predmetov z analizo njegovih spektralnih linij z uporabo tehnik emisijske spektroskopije.
Nato je razloženo, iz česa je sestavljen iz emisijskega spektra, nekaj primerov in razlike med emisijskim spektrom in absorpcijo so omenjene.
[TOC]
Kaj je emisijski spekter?
Atomi elementa ali snovi imajo elektrone in protone, ki ostanejo združeni zaradi sile elektromagnetne privlačnosti. Po modelu Bohr so elektroni pripravljeni tako, da je energija atoma čim bolj nizka. Na tej ravni energetske energije se imenuje temeljno stanje atoma.
Ko atomi pridobijo energijo iz tujine, se elektroni premaknejo proti višji ravni energije in atom spremeni svoj temeljni status v vzbujeno stanje.
Vam lahko služi: elektromagnet: sestava, deli, kako deluje in aplikacijeV vzbujenem stanju je čas stalnosti elektrona zelo majhen (≈ 10-8 s) (1), atom je nestabilen in se po potrebi vrne na temeljno stanje, ki se po potrebi vrne z vmesnimi ravnmi energije.
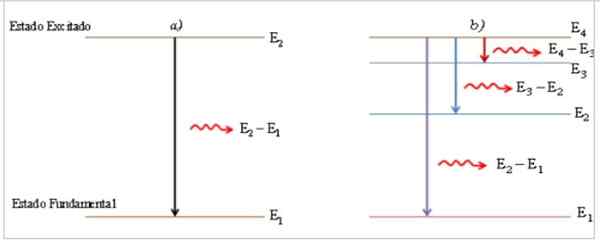
 Slika 1. a) Emisija fotona zaradi prehoda atoma med stopnjo vzbujevalne energije in temeljno raven energije. b) Emisija fotonov zaradi prehoda atoma med vmesno raven energije.
Slika 1. a) Emisija fotona zaradi prehoda atoma med stopnjo vzbujevalne energije in temeljno raven energije. b) Emisija fotonov zaradi prehoda atoma med vmesno raven energije. V procesu prehoda vzbujenega stanja v temeljno stanje atom oddaja foton svetlobe z energijo, ki je enaka razlika v energiji med obema stanjem, saj je neposredno sorazmerna s frekvenco V in obratno sorazmerna z njegovo valovno dolžino λ λ λ.
Izpuščeni foton je prikazan kot briljantna črta, imenovana spektralna črta (2), spektralna porazdelitev energije zbirke fotonov v atomskih prehodih pa je emisijski spekter.
Razlaga emisijskega spektra
Nekatere prehode atoma povzročajo povišana temperatura ali prisotnost drugih zunanjih virov energije, kot so žarek svetlobe, tok elektronov ali kemična reakcija.
Če se plin, kot je vodik.
Pri prehodu izpuščene svetlobe skozi prizmo namesto pridobivanja mavrice svetlobe dobimo diskretne enote v obliki barvnih linij s specifičnimi valovnimi dolžinami, ki prenašajo diskretne količine energije.
Emisijske spektralne črte so edinstvene v vsakem elementu in njihova uporaba iz tehnike spektroskopije omogoča določitev elementarne sestave neznane snovi in sestave astronomskih predmetov z analizo valov.
Vam lahko služi: akutni zvoki: značilnosti in primeriRazlika med emisijskim spektrom in absorpcijskim spektrom.
V procesih absorpcije in emisije ima atom prehode med dvema energetskima stanjem, vendar v absorpciji pridobi zunanjo energijo in doseže stanje vzbujanja.
Linija spektralne emisije nasprotuje neprekinjenemu spektru bele svetlobe. V prvem se spektralna porazdelitev opazi v obliki svetlih črt, v drugem.
Če beli svetlobni žarek vpliva na plin, kot je vodik, zaklenjen v komoro z nizkim pritiskom, bo plin absorbiral le del svetlobe, preostali.
Ko prenosna svetloba prečka prizmo, se razgradi v spektralnih linijah, vsak z drugačno valovno dolžino in tvori spekter absorpcije plina.
Absorpcijski spekter popolnoma nasprotuje emisiji in je tudi značilen za vsak element. Pri primerjavi obeh spektrov istega elementa opažamo, da so spektralne emisijske črte tiste, ki manjkajo v absorpcijskem spektru (slika 2).
 Slika 2. a) Emisijski spekter in b) absorpcijski spekter (avtor: STKL. Vir: https: // commons.Wikimedia.org/wiki/main_page)
Slika 2. a) Emisijski spekter in b) absorpcijski spekter (avtor: STKL. Vir: https: // commons.Wikimedia.org/wiki/main_page) Primeri emisijskih spektrov kemičnih elementov
a) Spektralne črte vodikovega atoma v vidnem območju spektra so 656 rdeča črta.3 nm, svetlo modra 486.1nm, temno modra 434nm in zelo šibka vijolična 410nm. Te valovne dolžine dobimo iz Balmer - Rydbergova enačba v svoji sodobni različici (3).
To je valovno število spektralne črte
Lahko vam služi: Slišite silo: površinske in masne sileTo je Rydbergova konstanta (109666.56 cm-1)
je najvišja raven energije
je najvišja raven energije
 Slika 3. Spekter emisij vodika (avtor: Adrignola. Vir: Commons.Wikimedia.org
Slika 3. Spekter emisij vodika (avtor: Adrignola. Vir: Commons.Wikimedia.org b) Spekter emisij helija ima dve seriji glavnih linij, eno v vidnem območju in eno blizu ultravijoličnega. Peterson (4) je uporabil model BOHR, da je izračunal niz emisijskih linij helija v vidnem delu spektra, kar je posledica več hkratnih prehodov dveh elektronov v stanje n = 5, in pridobilo vrednosti valovne dolžine, sestavljene iz eksperimentalne dolžine rezultati. Valovne dolžine, ki so bile pridobljene, so 468.8nm, 450.1NM, 426.3NM, 418.4nm, 412.2NM, 371.9nm.
C) Spekter natrijevega emisije ima dve zelo briljantni 589Nm in 589 vrstic.6nm, imenovane črte D (5). Druge črte so veliko šibkejše od teh in za praktične namene velja, da vsa natrijeva svetloba izvira iz D črta.
Reference
- Merjenje življenjskih življenj vzbujenega stanja vodikovega atoma. V. Do. Ankudinov, s. V. Bobashev in e. Str. Andreev. 1, 1965, Sovjetska fizika JETP, Vol. 21, str. 26-32.
- Demtröder, w. Laserska spektroskopija 1. Kaiserslautern: Springer, 2014.
- D.K.Rai, s.N Thakur in. Atom, laser in spektroskopija. New Delhi: Phi Learning, 2010.
- Bohr Revidid: Model Adespektralne linije helija. Peterson, c. 5, 2016, Journal of Young Insproutors, Vol. 30, str. 32-35.
- Journal of Chemical Education. J.R. Uporabi, f. J. Yonke, r. Do. Edgington in s. Jacobs. 3, 1993, Vol. 70, str. 250-251.
- « 18 najbolj zasvojenih snovi in njihovih učinkov
- Za vedno sam, kaj pomeni in za kaj se uporablja »

