Nitruro de boro (BN) struktura, lastnosti, pridobivanje, uporabe
- 4566
- 1016
- Mr. Shane Larkin
On Bonski nitrid Gre. Njegova kemična formula je bn. Je zelo odporna bela trdna snov pri visokih temperaturah in je dober vročinski voznik. Uporablja se na primer za izdelavo laboratorijskih krozol.
Boro nitruro (BN) je odporen na številne kisline, vendar ima nekaj šibkosti do napadov fluoridne kisline in staljenih baz. Je dober izolator električne energije.
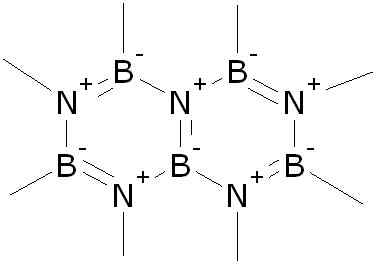
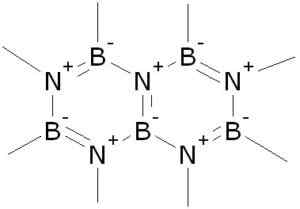 Struktura boro nitrida (BN). Akeramop [javna domena]. Vir: Wikimedia Commons.
Struktura boro nitrida (BN). Akeramop [javna domena]. Vir: Wikimedia Commons. Dobimo ga v različnih kristalnih strukturah, od katerih sta najpomembnejša šesterokotna in kubična. Šesterokotna struktura spominja na grafit in je spolzka, zato se uporablja kot mazivo.
Kubična struktura je skoraj tako trda kot diamant in se uporablja za izdelavo orodij za rezanje in za izboljšanje trdote drugih materialov.
Z bonskim nitridom lahko izdelate mikroskopske cevi (izjemno tanke), imenovane nanocevke, ki imajo medicinske aplikacije, na primer za prevoz znotraj telesa in sproščanje zdravil proti tumorjem raka.
[TOC]
Struktura
Boro Nitruro (BN) je spojina, kjer sta atomi bora in dušika kovalentno povezani s trojno povezavo.
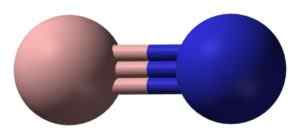 Molekula izolirane borove nitrida ima dušikov dušik atom združenega s trojnim vezjem. Benjah-BMM27 [javna domena]. Vir: Wikimedia Commons.
Molekula izolirane borove nitrida ima dušikov dušik atom združenega s trojnim vezjem. Benjah-BMM27 [javna domena]. Vir: Wikimedia Commons. V trdni fazi je Bn oblikovan z enakim številom atomov bora in dušika v obliki 6 obročev članov.
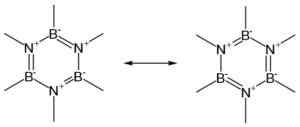 Resonančne strukture bn obroča. Avtor: Teachi. Vir: Wikimedia Commons.
Resonančne strukture bn obroča. Avtor: Teachi. Vir: Wikimedia Commons. Bn obstaja v štirih kristalnih oblikah: šesterokotni (H-bn), podobno grafitnemu, kubičnemu (c-bn), podobno kot Diamond, Rhomboédica (R-BN) in Wurtzita (W-BN).
Struktura H-BN je podobna strukturi grafita, to je, da ima letale šesterokotne prstane, ki imajo atome bora in dušika, ki se izmenjujejo.
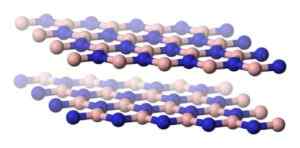 Struktura v obliki ločenih ravnin šesterokotnega borovega nitrida. Benjah-BMM27 [javna domena]. Vir: Wikimedia Commons.
Struktura v obliki ločenih ravnin šesterokotnega borovega nitrida. Benjah-BMM27 [javna domena]. Vir: Wikimedia Commons. Med ravninami H-BN je velika razdalja, ki nakazuje, da so združeni le prek sil Van Der Waals, ki so zelo šibke sile privlačnosti in načrti zlahka drsijo drug na drugega.
Vam lahko služi: sonceZaradi tega je H-bn neobljuden na dotik.
Struktura kubičnega bn c-bn je podobna diamantu.
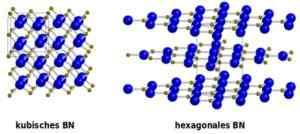 Primerjava med kubičnim nitrurojem (levo) in šesterokotno (desno). Od: Benutzer: Oddball, vektorska različica Chrisa 論 [Public Domain]. Vir: Wikimedia Commons.
Primerjava med kubičnim nitrurojem (levo) in šesterokotno (desno). Od: Benutzer: Oddball, vektorska različica Chrisa 論 [Public Domain]. Vir: Wikimedia Commons. Nomenklatura
Bonski nitrid
Lastnosti
Fizično stanje
Maščobna ali spolzka bela trdna snov, ki jih je treba dotikati.
Molekularna teža
24,82 g/mol
Tališče
Sublima pri približno 3000 ° C.
Gostota
Šesterokotni Bn = 2,25 g/cm3
Kubični Bn = 3,47 g/cm3
Topnost
Rahlo topen v vročem alkoholu.
Kemične lastnosti
Zaradi močne povezave med dušikom in borom (trojna vez) borani nitrid ima visoko odpornost proti kemičnemu napadu in je zelo stabilen.
Je netopna v kislinah, kot so HCl klorovodikova kislina, dušikova kislina HNO3 in žveplova kislina h2SW4. Je pa topna v staljenih bazah, kot so lioh litijev hidroksid, koh kalijev hidroksid in NaOH natrijev hidroksid.
Ne reagira z večino kovin, stekla ali soli. Včasih reagira s fosforno kislino h3Po4. Oksidacijo se lahko uprete pri visokih temperaturah. Bn je stabilen v zraku, voda pa počasi hidrolizira.
BN napade fluori2 in s HF fluorhorhoric kislina.
Druge fizikalne lastnosti
Ima visoko toplotno prevodnost, visoko toplotno stabilnost in visoko električno upornost, to je dober izolator električne energije. Ima visoko površino.
H-bn (šesterokotni BN) je trden neobreten za dotik, podobno kot grafit.
Pri segrevanju H-bn pri visoki temperaturi in tlaku postane kubična oblika C-Bn, ki je izjemno trda. Po nekaterih virih lahko opraska diamant.
Materiali, ki temeljijo na BN, imajo anorganska onesnaževala sorpcijsko sposobnost (na primer ioni težkih kovin) in organska onesnaževala (kot so barvila in molekule).
Sorción pomeni, da z njimi komunicira in jih lahko adsorbira ali absorbira.
Pridobivanje
H-bn prah pripravimo z reakcijo med boronskim bioksidom B2Tudi3 ali borna kislina h3BO3 Z amonijakom NH3 ali s sečnino NH2(CO) NH2 Pod dušikovo atmosfero n2.
Vam lahko postreže: Mount Olympus (Mars)BN lahko dobimo tudi z reakcijo bora z amoniakom pri zelo visoki temperaturi.
Drug način za pripravo je iz Diborano B2H6 in amonijak NH3 Uporaba inertnega plina in visokih temperatur (600-1080 ° C):
B2H6 + 2 NH3 → 2 bn + 6 h2
Prijave
H-BN (šesterokotni boron nituro) ima različne pomembne aplikacije, ki temeljijo na njegovih lastnostih:
-Kot trdno mazivo
-Kot dodatek za kozmetiko
-Pri visoko temperaturi električnih izolatorjev
-V lončkih in reakcijskih posodah
-V izhlapevanju plesni in posode
-Za shranjevanje vodika
-Na katalizi
-Za adsorbiranje onesnaževal odpadne vode
Kubični bonski nitruro (c-bn) za svojo trdoto, ki je skoraj enaka kot diamant, se uporablja:
-V rezanju orodij za obdelavo trdih železovih materialov, kot so trde jeklene zlitine, litoželeb in orodja
-Izboljšati trdoto in odpornost na nošenje drugih trdih materialov, kot je določena keramika za rezanje orodij.
 Nekatera orodja za rezanje lahko vsebujejo borovo nitruro, ki kaže večjo trdoto. Avtor: Michael Schwarzenberger. Vir: Pixabay.
Nekatera orodja za rezanje lahko vsebujejo borovo nitruro, ki kaže večjo trdoto. Avtor: Michael Schwarzenberger. Vir: Pixabay. - Uporaba tankih filmov Bn
Zelo so koristne v tehnologiji polprevodniških naprav, ki so komponente elektronske opreme. Služijo na primer:
-Za izdelavo ravnih diod; Diode so naprave, ki v enem smislu omogočajo kroženje električne energije
-V spominskih diodah od kovine do polprevodnika, kot je al-bn-sio2-Ja
-V integriranih vezjih kot omejevalnik napetosti
-Povečati trdoto določenih materialov
-Za zaščito nekaterih oksidacijskih materialov
-Povečati kemijsko stabilnost in električno izolacijo številnih vrst naprav
-V kondenzatorju tankega filma
 Nekatere diode in kondenzatorji lahko vsebujejo bonski nitrid. Avtor: Sinisa Maric. Vir: Pixabay.
Nekatere diode in kondenzatorji lahko vsebujejo bonski nitrid. Avtor: Sinisa Maric. Vir: Pixabay. - Uporaba bn nanocevk
Nanocevke so strukture, ki so na molekularni ravni oblikovane kot cevi. So cevi, ki so tako majhne, da jih lahko vidimo le s posebnimi mikroskopi.
Spodaj je nekaj značilnosti nanocevk Bn:
-Imajo visoko hidrofobnost, torej odbijajo vodo
-Imajo visoko odpornost na oksidacijo in toploto (oksidacija se lahko upira do 1000 ° C)
-Imajo visoko zmogljivost za shranjevanje vodika
-Absorbirajo sevanje
-So zelo dobri izolatorji električne energije
Vam lahko služi: termometer upora: značilnosti, delovanje, uporabe-Imajo visoko toplotno prevodnost
-Njegova odlična odpornost na oksidacijo z visokimi temperaturami pomeni, da jih je mogoče uporabiti za povečanje stabilnosti na površinsko oksidacijo.
-Zaradi svoje hidrofobnosti jih lahko uporabimo za pripravo super hidrofobnih površin, to pomeni, da nimajo afinitete do vode in vode ne prodre.
-Bn nanocevke izboljšujejo lastnosti nekaterih materialov, na primer, uporabljene so bile za povečanje trdote in odpornosti proti zlomu stekla.
 Nitubos iz Nitruro iz Bora, ki so ga opazili z mikroskopom. Keun njegov Kim et al. [CC do 4.0 (https: // creativeCommons.Org/licence/by/4.0)]. Vir: Wikimedia Commons.
Nitubos iz Nitruro iz Bora, ki so ga opazili z mikroskopom. Keun njegov Kim et al. [CC do 4.0 (https: // creativeCommons.Org/licence/by/4.0)]. Vir: Wikimedia Commons. V medicinskih aplikacijah
BN nanocevke so bile testirane kot nosilci zdravil za raka, kot je doksorubicin. Nekatere sestave s temi materiali so povečale učinkovitost kemoterapije z omenjenim zdravilom.
V več izkušnjah se je pokazalo, da imajo nanocevke BN potencial za prevoz novih zdravil in jih pravilno sprostiti.
Uporaba nanocevk Bn v polimernih biomaterialih je bila raziskana za povečanje njihove trdote, razgradnje in trajnosti. To so materiali, ki se uporabljajo na primer v ortopedskih vsadkih.
Kot senzorji
BN nanocevke so bile uporabljene za izdelavo novih naprav za odkrivanje vlage, ogljikovega dioksida2 in za klinične diagnoze. Ti senzorji so pokazali hiter odziv in kratek čas okrevanja.
Možna strupenost materialov BN
Nekaj skrbi zaradi možnih strupenih učinkov nanocevk Bn. O njeni citotoksičnosti ni jasnega soglasja, ker nekatere študije kažejo, da so strupene za celice, druge.
To je posledica njegove hidrofobnosti ali netopnosti v vodi, saj otežuje izvajanje študij v bioloških materialih.
Nekateri raziskovalci so pokrivali površino nanocevk Bn z drugimi spojinami, ki dajejo prednost njihovi topnosti v vodi, vendar je to dodalo večjo negotovost pri izkušnjah.
Čeprav večina raziskav kaže, da je njihova stopnja toksičnosti nizka, se ocenjuje, da je treba izvesti natančnejše raziskave.
Reference
- Xiong, J. et al. (2020). Šesterokotni adsorbent borovega nitrida: sinteza, prilagoditev zmogljivosti in aplikacije. Journal of Energy Chemistry 40 (2020) 99-111. Okreval od bralca.Elsevier.com.
- Mukasyan, a.S. (2017). Bonski nitrid. V jedrnati enciklopediji samoodpadanja visokotemperaturne sinteze. Okrevano od Scientirect.com.
- Kalay, s. et al. (2015). Sinteza nanocevk borovega nitrida in njihovih aplikacij. Beilstein J. Nanotehnol. 2015, 6, 84-102. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Arya, s.Str.S. (1988). Priprava, lastnosti in uporabe tankih filmov borovega nitrida. Tanki trdni filmi, 157 (1988) 267–282. Okrevano od Scientirect.com.
- Zhang, J. et al. (2014). Keramični matrični kompoziti, ki vsebujejo kubične borove, za rezanje orodij. V napredku v kompozitih keramične matrice. Okrevano od Scientirect.com.
- Bombaž, f. Albert in Wilkinson, Geoffrey. (1980). Napredna anorganska kemija. Četrta izdaja. John Wiley & Sons.
- Suanarsan, v. (2017). Materiali za sovražno kemično okolje. V materialih v ekstremnih pogojih. Okrevano od Scientirect.com
- Dean, J.Do. (Urednik) (1973). Langeov priročnik kemije. McGraw-Hill Company.
- Mahan, b.H. (1968). Univerzitetna kemija. Interameriški izobraževalni sklad, s.Do.

