Meniskus (kemija)
- 3941
- 260
- Percy Feeney
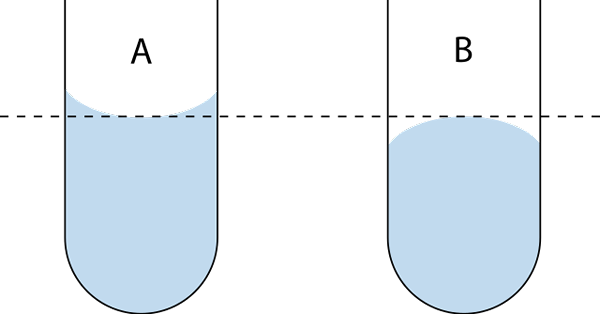
 Konkavni in konveksni meniskus. Vir: Wikimedia Commons
Konkavni in konveksni meniskus. Vir: Wikimedia Commons Kaj je meniskus (kemija)?
On meniskus Je ukrivljenost površine tekočine. Je tudi prosta površina tekočine v vmesniku tekočine in zraka. Za tekočine je značilno, da ima fiksno glasnost, ki je nekokompresivna.
Vendar se oblika tekočin razlikuje in sprejme obliko posode, ki jih vsebuje. Ta značilnost je posledica naključnega gibanja molekul, ki jih tvorijo.
Tekočine imajo sposobnost, da se pretakajo, visoko gostoto in hitro širijo v drugih tekočinah, s katerimi se zmešajo.
Zasedejo najnižje območje posode, na vrhu pa ostanejo prosti ne povsem ravno površino. V nekaterih okoliščinah lahko sprejmejo posebne oblike, kot so kapljice, mehurčki in mehurčki.
Lastnosti tekočin, kot so tališče, parni tlak, viskoznost in toplota uparjanja, so odvisne od intenzivnosti medmolekulskih sil, ki dajejo kohezijo tekočine.
Vendar tekočine delujejo tudi s posodico prek adhezijskih sil.
Denisk nato izhaja iz teh fizičnih pojavov: razlika med kohezijskimi silami med tekočimi delci in oprijem, ki jim omogoča, da navlažijo stene.
Kaj je meniskus?
Kot je razloženo, je meniskus rezultat več fizičnih pojavov, med katerimi lahko omenimo tudi površinsko napetost tekočine.
Kohezijske sile
Kohezijske sile so fizični izraz, ki pojasnjuje medmolekularne interakcije znotraj tekočine. V primeru vode so kohezijske sile posledica interakcije dipola-dipolo in vodikovih mostov.
Vam lahko služi: klor oksid (iii): lastnosti, struktura, uporabeMolekula vode je bipolarna narava. To je zato, ker je kisik molekule elektronegativen, ker ima večjo avidnost zaradi elektronov kot vodikov, kar določa, da kisik ostane z negativno obremenitvijo in vodiki se pozitivno nabijejo.
Obstaja elektrostatična privlačnost med negativno obremenitvijo molekule vode, ki se nahaja v kisiku, in pozitivno obremenitvijo druge molekule vode, ki se nahaja v vodiki.
Ta interakcija je tisto, kar pozna kot interakcija ali sila dipola, ki prispeva k koheziji tekočine.
Adhezijske sile
Po drugi strani lahko molekule vode v interakcijo s steklenimi stenami z delno obremenitvijo vodikovih atomov molekul vode, ki vežejo kisikove atome površine stekla stekla v atomih kisika.
To predstavlja adhezijsko silo med tekočino in togo steno, kar pogovorno pomeni, da tekočina moči steno.
Ko je silikonska raztopina nameščena na stekleni površini, voda kozarca ne popolnoma impregnira, ampak se na teh kapljicah oblikuje.
Tako je navedeno, da se s tem zdravljenjem adhezijska sila med vodo in steklom zmanjša.
Zelo podoben primer se pojavi, ko so roke mastne, in pri pranju z vodo lahko na koži namesto na navlažene kože opazimo zelo definirane kapljice.
Vrste meniska
Obstajata dve vrsti meniskusa: konkava in izboklina. Na vrhunski sliki je konkava a in konveksna B. Pikčaste črte označujejo pravilno izpiranje pri branju mera glasnosti.
Vam lahko služi: nevtralni atomKonkavni meniskus
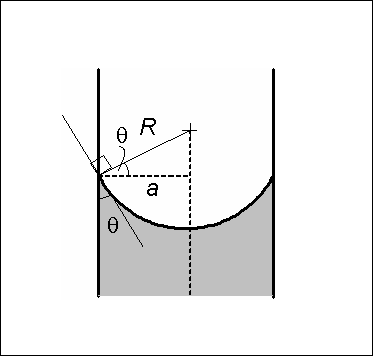 Konkavni ukrepi meniskusa. Vir: Wikimedia Commons
Konkavni ukrepi meniskusa. Vir: Wikimedia Commons Konkavni meniskus je značilen v tem, da kontaktni kot θ, ki tvori steno kozarca s tangentno črto do meniskusa, ki je vnesena v krog tekočine, ima vrednost manjša od 90 °.
Če je na kozarcu nameščena količina tekočine, se nagiba na stekleni površini.
Prisotnost konkavnega meniska.
Zato se tekočina kopa ali zbira stekleno steno, ki obdrži količino tekočine in daje meniskusu konkavno. Voda je primer tekočine, ki tvori konkavno meniskus.
Konveksni meniskus
V primeru konveksnega meniskusa ima kontaktni kot θ vrednost, večjo od 90 °. Živo srebro je primer tekočine, ki tvori konveksni meniskus. Ko je kapljica živega srebra nameščena na stekleni površini, ima kontaktni kot θ vrednost 140 °.
Opazovanje konveksnega meniska. Govori se, da tekočina ne zmoti kozarca.
Površne sile kohezije (tekočina-tekočina) in adhezije (tekoče trdne) so odgovorne za številne pojave biološkega interesa, kot sta primer površinske napetosti in kapilarne.
Površinska napetost
Površinska napetost je neto privlačna sila, ki se izvaja na molekulah tekočine, ki jih najdemo na površini, in jih ponavadi vnese v tekočino.
Vam lahko služi: diatomični elementiZato se površinska napetost ponavadi obnese tekočina in daje več konkavnega meniskusa. Z drugimi besedami, ta sila ponavadi odstrani površino steklene stenske tekočine.
Površinska napetost se ponavadi zmanjšuje, ko se temperatura poveča, na primer: napetost površinske vode je enaka 0,076 N/M A 0 ° C in 0,059 N/M A 100 ° C.
Medtem ko je površinska napetost živega srebra pri 20 ° C 0,465 N/m. To bi razložilo, zakaj živo srebro oblikuje konveksni meniskus.
Kapilarnost
Če je kontaktni kot θ manjši od 90 °, tekočina pa moči stekleno steno, se lahko tekočina v steklenih kapilarah vzpenja, dokler ne doseže stanja ravnotežja.
Teža tekočega stolpca je kompenzirana z navpično komponento kohezijske sile zaradi površinske napetosti. Adhezijska sila ne posreduje, ker je pravokotna na površino cevi.
Ta zakon ne pojasnjuje, kako se lahko voda dvigne iz korenin do listov skozi žile Xylem.
Pravzaprav so v zvezi s tem vključeni tudi drugi dejavniki: Ko voda izhlapi v listih, omogoča, da se molekule vode sesajo v zgornjem delu kapilar.
To omogoča, da se druge molekule na dnu kapilar vzpenjajo, da bi zasedle mesto izhlapenih molekul vode.
Reference
- Whitten, Davis, Peck & Stanley. Kemija. Cengage učenje.
- Čelada, Anne Marie, ph.D. Kako brati meniskus v kemiji. Opomogel od Thoughtco.com

