Boyle zakon
- 4103
- 335
- Roman Schamberger
Kaj je Boylejev zakon?
The zakon Boyle ali Boyle-Maleotte zakon To je tisto, ki izraža razmerje med pritiskom, ki ga ima plin ali na njem, in prostornino, ki ga to zaseda; Nenehno ohranja tako temperaturo plina kot tudi njegovo količino (število molov).
Ta zakon skupaj z zakonom Charlesa, Gay-Lussac, Charlesa in Avogadro opisuje vedenje idealnega plina; Konkretno v zaprti posodi, ki so podvrženi sprememb volumna, ki jo izvaja mehanska sila.
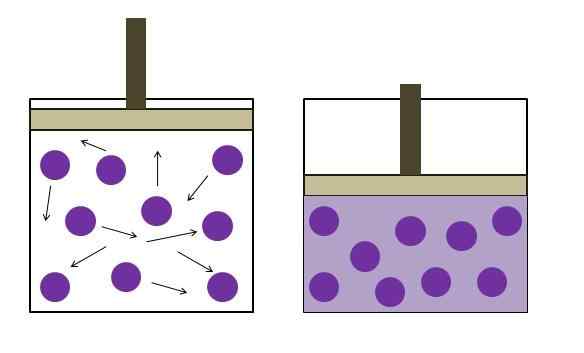
 Povečan tlak znižanja tlaka. Vir: Gabriel Bolívar
Povečan tlak znižanja tlaka. Vir: Gabriel Bolívar Zgornja slika na kratko povzema Boylejev zakon. Vijolične točke predstavljajo molekule ali plinske atome, ki trčijo v notranje stene posode (levo). Z zmanjšanjem razpoložljivega prostora ali volumna vsebnika, ki ga zaseda ta plin, se povečajo trki, kar pomeni povečanje tlaka (desno).
To kaže, da sta tlak P in volumna V plina obratno sorazmerna, če je posoda tesno zaprta; v nasprotnem primeru bi bil večji tlak enak večji dilataciji posode.
Če bi opazili graf V proti P, s podatki V in P na osi oziroma X, bi opazili asimptotsko krivuljo. Spodnji V, večji je povečanje p; To pomeni, da se bo krivulja razširila na visoke vrednosti p na osi x.
Seveda temperatura ostane konstantna; Če pa bi bil isti poskus izveden pri različnih temperaturah, bi se relativni položaji teh krivulj v Vs P spremenili na kartezijanski osi. Sprememba bi bila še bolj očitna, če bi bili grafi na tridimenzionalni osi, s konstantno t na osi z.
Zgodovina Boylejevega zakona
Ozadje
Ker je znanstvenik Galileo Galilei izrazil svoje prepričanje v obstoj praznine (1638), so znanstveniki začeli preučevati lastnosti zraka in delnih vrzeli.
Angloirlandični kemik Robert Boyle je leta 1638 začel študij o zračnih nepremičninah, ko je izvedel, da je Otto Von Guericke, nemški inženir in fizični inženir, zgradil zračno bombo.
Vam lahko služi: bromova: zgodovina, struktura, elektronska konfiguracija, lastnosti, uporabeEksperiment živega srebra
Da bi izvedel študije zračnega tlaka, je Boyle uporabil cev "J", katere konstrukcijo je bil pripisan Robertu Hookeu, asistentu Boyle. Konec kratke roke je bil zapečaten, medtem ko je bil dolg ročni konec cevi odprt, da bi postavil živo srebro.
Od začetka je Boyle želel preučiti elastičnost zraka, kakovostno in kvantitativno. Ko se je živo srebro vlilo skozi odprti konec cevi v obliki "J", je Boyle ugotovil, da je bil zrak v kratki roki cevi pod pritiskom živega srebra.
Rezultati
Večja kot je količina živega srebra, dodana cevi, večji je tlak v zraku in nižji je njen prostornina. Boyle je dobil negativno eksponentno tabelo volumna zraka, odvisno od tlaka.
Medtem, če je narisana prostornina zraka proti inverznemu tlaku, obstaja ravna črta pozitivnega naklona.
Leta 1662 je Boyle objavil prvi fizični zakon, ki je bil podan v obliki enačbe, ki je pokazala funkcionalno odvisnost dveh spremenljivk. V tem primeru tlak in prostornina.
Boyle je dejal, da obstaja obratno razmerje med pritiskom na plin in prostornino, ki je zaseden ta plin, kar je relativno resnično razmerje za resnične pline. Večina plinov se obnaša kot idealni plini za zmerne tlake in temperature.
Ko se pojavijo višji pritiski in nižje temperature, so odstopanja od obnašanja resničnih plinov idealov postala bolj opazna.
Edme Mariotte
Francoski fizik Edme Mariotte (1620-1684) je leta 1679 neodvisno odkril isti zakon. Vendar je imel zasluge, da je pokazal, da se prostornina razlikuje glede na temperaturo. Zato se imenuje Mariottejev zakon ali zakon Boyle in Mariotte.
Krepitev zakona
Daniel Bernoulli (1737) je okrepil Boylov zakon tako.
Lahko vam služi: nukleofil: nukleofilni napad, tipi, primeri, nukleofilnostLeta 1845 je John Waterston objavil znanstveni članek, ki se osredotoča na glavna načela kinetične teorije plinov.
Nato so Rudolf Clausius, James Maxwell in Ludqwig Boltzmann konsolidirali kinetično teorijo plinov, ki navaja tlak, ki ga ima plin s hitrostjo plinskih delcev v gibanju v gibanju v gibanju.
Nižja kot je prostornina posode, ki vsebuje plin, večja je pogostost udarcev delcev, ki ga tvorijo ob stenah vsebnika; In zato je večji tlak, ki ga ima plin.
Kaj je ta zakon?
Poskusi, ki jih je izvedel Boyle. Vendar že omenjeno razmerje ni popolnoma linearno, kot kaže graf variacije glasnosti glede na tlak, pripisan Boyleu.
V Boylejevem zakonu je navedeno, da je prostornina, ki jo zaseda plin, obratno sorazmerna s pritiskom. Prav tako je navedeno, da je produkt tlaka plina z njegovo prostornino konstanten.
Matematični izraz
Če želite priti do matematičnega izraza Boylejevega zakona, se začne iz:
V ∝ 1/p
Kjer kaže, da je prostornina, ki jo zaseda plin, obratno sorazmerna s pritiskom. Vendar obstaja konstanta, ki narekuje, kako obratno sorazmerna je ta odnos.
V = k/p
Kjer je k konstanta sorazmernosti. Čiščenje k imate:
Vp = k
Produkt tlaka plina po njegovi prostornini je konstanten. Tako:
V1Str1 = K in V2Str2 = k
In to je mogoče sklepati:
V1Str1 = V2Str2
Slednji je izraz ali končna enačba za Boylejev zakon.
Za kaj je? Kakšne težave rešuje Boyleov zakon?
Parni motorji
Zakon Boyle-Maleotte se uporablja pri delovanju parni stroji. To je zunanji zgorevalni motor, ki uporablja transformacijo toplotne energije količine vode v mehansko energijo.
Voda se segreva v tesno zaprtem kotlu, proizvedena para pa ima tlak v skladu z zakonom Boyle, ki povzroči širitev volumna cilindra s potiskanjem bata.
Vam lahko služi: faktor redčenjaLinearno gibanje bata se pretvori v rotacijsko gibanje z uporabo ročic in ročičnega sistema, ki lahko poganja kolesa lokomotive ali rotorja električnega generatorja.
Srkajo pijače
Dejanje, ki si prizadeva za sodo ali sok steklenice skozi plastično cev, je povezano z Boylejevim zakonom. Ko se z usti predlaga zrak cevi, pride do zmanjšanja tlaka znotraj cevi.
Ta padec tlaka olajša naraščajoče gibanje tekočine v cevi, kar omogoča zaužitje. To isto načelo deluje pri pridobivanju krvi z uporabo brizge.
Dihalni sistem
Boylejev zakon je tesno povezan z delovanjem dihalnega sistema. V fazi navdiha pride do krčenja diafragme in drugih mišic; Na primer, zunanji interkostali, ki proizvajajo širitev rebraste kletke.
To povzroči znižanje intrapleuralnega tlaka, kar povzroči pljučno širitev, ki povzroči povečanje volumna pljuč. Zato se intrapulmonalni tlak zmanjšuje glede na to, kar se vzgaja v Boylejevem zakonu.
Z intrapulmonalnim pritiskom s subatozo se v pljuča teče atmosferski zrak, kar povzroči povečanje tlaka v pljučih; Tako ujemajo njen pritisk z atmosferskim pritiskom in zaključi fazo navdiha.
Kasneje se navdihujoče mišice sprostijo in ekspiratorne mišice se krčijo. Poleg tega se nastaja elastični pljučni odvzem, pojav, ki povzroči zmanjšanje volumna pljuč, s posledičnim povečanjem intrapulmonalnega pritiska.
S povečanjem intrapulmonalnega tlaka in večjim od atmosferskega tlaka zrak teče znotraj pljuč do atmosfere. To se zgodi, dokler pritiski niso enaki, kar zaključi fazo poteka.
Reference
- Boylejev zakon. Encyclopædia Britannica. Okrevano od: Britannica.com
- Formula za Boylejev zakon. Okreval od: Thoughtco.com

