Hidroksiapatit

- 2788
- 93
- Ricky Dach
Pojasnjujemo, kaj je hidroksilapatit, njena struktura, kako je sintetizirana, njegova uporaba in fizikalne in kemijske lastnosti
 Hidroksiapatit. Vir: Rob Lavinsky, Irocks.com-cc-by-sa-3.0, cc by-sa 3.0, prek Wikimedia Commons
Hidroksiapatit. Vir: Rob Lavinsky, Irocks.com-cc-by-sa-3.0, cc by-sa 3.0, prek Wikimedia Commons Kaj je hidroksiapatit?
The Hidroksiapatit Gre za mineral kalcijevega fosfata, katerega kemična formula je CA10(Po4)6(OH)2. Skupaj z drugimi minerali in organsko in stisnjeno organsko snovjo tvori surovino, znano kot fosforna skala. Izraz Hydroxi se nanaša na Anion Oh-.
Če bi bil namesto tega aniona fluorid, bi mineral imenovali fluoroapatita (CA10(Po4)6(F)2; In tako z drugimi anioni (Cl-, Br-, Co32-, itd.). Prav tako je hidroksiapatit glavna anorganska sestavina kosti in zobne sklenine, pretežno prisotna v kristalni.
Torej, to je bistveni element v kostnih tkivih živih bitij. Njegova velika stabilnost proti drugim kalcijevim fosfatom mu omogoča, da podpira fiziološke razmere, kar daje kosti njihovo značilno trdoto. Hidroksiapatit ni sam: izpolnjuje svojo funkcijo, ki jo spremlja kolagen, vlaknasti protein konjunktivnih tkiv.
Hidroksiapatit (ali hidroksilapatit) vsebuje CA ione2+, Toda tudi v drugi kationi lahko nastanejo v svoji strukturi (MG2+, Na+), nečistoče, vključene v druge biokemijske procese kosti (na primer njihovo preoblikovanje).
Struktura hidroksiapatita
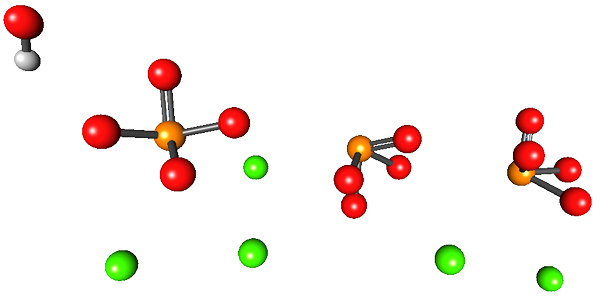
Vrhunska slika ponazarja strukturo kalcijevega hidroksiapatita. Vse sfere zasedajo glasnost polovice šesterokotnega "predala", kjer je druga polovica enaka prvemu.
V tej strukturi zelene sfere ustrezajo kationom2+, Medtem ko rdeče krogle do kisikovih atomov, oranžne do fosforjeve atome in bela do OH vodikovega atoma-.
Fosfatni ioni na tej sliki imajo napako, da ne prikazujejo tetraedrske geometrije; Namesto tega se zdijo kot kvadratne bazne piramide.
Vam lahko služi: steklovinoOh- daje vtis, da se nahaja daleč od ca2+. Vendar se lahko kristalna enota ponovi na strehi prvega in tako kaže bližino obeh ionov. Tudi te ione lahko nadomestijo drugi (NA+ in f-, Na primer).
Sinteza hidroksilapatita
Hidroksilapatit lahko sintetiziramo z reakcijo kalcijevega hidroksida s fosforno kislino:
10 CA (OH)2 + 6 h3Po4 => Ca10(Po4)6(OH)2 + 18 h2Tudi
Hidroksiapatita (ca10(Po4)6(OH)2) se izraža z dvema enotama formuli CA5(Po4)3Oh.
Prav tako lahko hidroksiapatit sintetiziramo z naslednjo reakcijo:
10 CA (št3)2.4H2O + 6 NH4H2Po4 => Ca10(Po4)6(OH)2 + 20 nh4Ne3 + 52 h2Tudi
Nadzor hitrosti padavin omogoča, da ta reakcija ustvari hidroksiapatitne nanodelce.
Kristali hidroksiapatita

Ioni so stisnjeni in rastejo, da tvorijo togo in odporno biokritno. To se uporablja kot biomaterial mineralizacije kosti.
Vendar potrebuje kolagen, organsko podporo, ki služi kot kalup njegove rasti. Ti kristali in njihovi zapleteni procesi tvorbe bodo odvisni od kosti (ali zob).
Ti kristali rastejo impregnirani z organsko snovjo, uporaba elektronskih mikroskopijskih tehnik.
Uporaba hidroksilapatita
Medicinska in zobozdravstvena uporaba
Nanohidroksiapatit je zaradi svoje podobnosti, kristalografije in sestave s trdim človeškim tkivom privlačen za uporabo v protezah. Tudi nanohidroksiapatit je biokompatibilen, bioaktiven in naraven, poleg tega, da ni strupen ali vneten.
Posledično ima nanohidroksiapatitna keramika različne aplikacije, ki vključujejo:
- Pri operaciji kosti tejido se uporablja pri polnjenju votlin v ortopedskih, travmatoloških, maksilofacialnih in zobnih operacijah.
- Uporablja se kot ortopedski in zobni vsadki. Je desenzibilizirajoč sredstvo, ki se uporablja za beljenje zob. Uporablja se tudi kot remineralizacijsko sredstvo v zobnih pastah in zgodnjem zdravljenju kariesa.
- Implantati iz nerjavečega jekla in titana so pogosto prekrita s hidroksiapatitom, da zmanjšajo hitrost zavrnitve.
- Je alternativa alogenim in ksenogenim presadkom kosti. Čas celjenja je krajši v prisotnosti hidroksiapatita kot v odsotnosti.
- Nanohidroksiapatit Sintetični mimetiza do hidroksiapatita, ki je naravno prisoten v dentinu in apatitskem enaltiku, zato je njegova uporaba pri popravilu sklenine in vključitvi v zobne paste ugodna, pa tudi v izpiranju ust.
Druge uporabe hidroksiapatita
- Hidroksiapatit se uporablja v zračnih filtrih motornih vozil, da se poveča njihova učinkovitost pri absorpciji in razgradnji ogljikovega monoksida (CO). To zmanjšuje onesnaževanje z okoljem.
- Alginat-hidroksiapatitni kompleks je bil sintetiziran, da so poljski testi nakazali, da lahko absorbira fluorid z mehanizmom za izmenjavo ionov.
- Hidroksiatpatit se uporablja kot kromatografski medij za beljakovine. To ima pozitivne stroške (CA++) in negativno (PO4-3), tako da lahko komunicira z električno napolnjenimi beljakovinami in omogoči njegovo ločitev z ionsko izmenjavo.
- Kot podporo za elektrofotične nukleinske kisline je bil uporabljen tudi hidroksiapatit. DNK je mogoče ločiti od RNA, pa tudi DNK preprostega sklopa obeh pramenov DNK.
Fizikalne in kemijske lastnosti
Hydroxyapatit je bela trdna snov, ki lahko pridobi sive, rumene in zelenke. Kot je kristalna trdna, predstavlja visoke fuzijske točke, ki kažejo na močne elektrostatične interakcije; Za hidroksiapatit je to 1100 ° C.
Je gostejša od vode, z gostoto 3,05 - 3,15 g/cm3. Poleg tega je praktično netopna v vodi (0,3 mg/ml), kar je posledica fosfatnih ionov.
Vendar je v kislih medijih (kot v HCl) topno. Ta topnost je posledica tvorbe CACL2, Zelo topna vodna sol. Prav tako so fosfati proton (HPO42- in h2Po4-) in v boljšo stopnjo interakcijo z vodo.
Topnost kislega hidroksiapatita je pomembna pri patofiziologiji kariesa. Bakterije v oralni votlini izločajo mlečno kislino, produkt glukozne fermentacije, kar zmanjšuje pH zobne površine na manj kot 5, zato se hidroksiapatit začne raztapljati.
Vam lahko služi: sublimacija: koncept, proces in primeriFluorid (f-) OH lahko zamenjate- V kristalni strukturi. Ko se to zgodi, zagotavlja odpornost na hidroksiapatit zobne sklenine pred kislinami.
Mogoče je ta odpor lahko posledica netopnosti CAF2 oblikoval, noče "zapustiti" kozarec.
Reference
- Shiver & Atkins. (2008). Anorganska kemija. (Četrti izd., str. 349, 627). MC Graw Hill.
- Fluidinova. (2017). Hidroksilapatit. Pridobljeno iz Fluidinova.com
- Gaiabulbanix. (5. november 2015). Hidroksiapatit. [Slika]. Okrevano iz Commons.Wikimedia.org
- Martin.Neitsov. (25. november 2015). Hüdroksüapatiidi Kristallid. [Slika]. Okrevano iz Commons.Wikimedia.org
- Wikipedija. (2018). Hidroksilapatit. Pridobljeno iz.Wikipedija.org
- Fiona Petchey. Kost. C14Dating je bil obnovljen.com

