Lastnosti aromatičnih ogljikovodikov, primeri, aplikacije
- 2634
- 494
- Cary Goyette
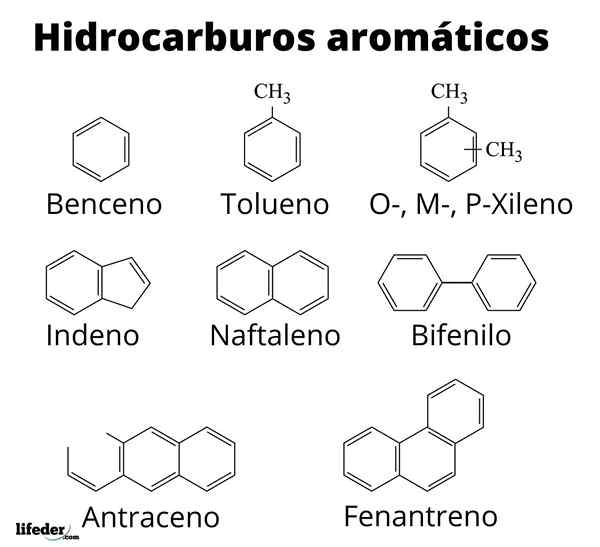
The Aromatični ali peščeni ogljikovodiki So nabor organskih spojin, ki so sestavljene samo iz ogljikov in vodikov, za katere so značilne, da imajo enote benzenskih obročev v svojih molekularnih strukturah.
Nekateri, kot poudarja njegovo ime, sprožijo sladke in prijetne vonjave; razlog, zakaj jih prve organske kemikalije imenujejo aromatične. Na primer metan plin je toaletni ogljikovodik; Medtem ko toluena, hlapna tekočina, predstavlja dokaj poseben in močan vonj.
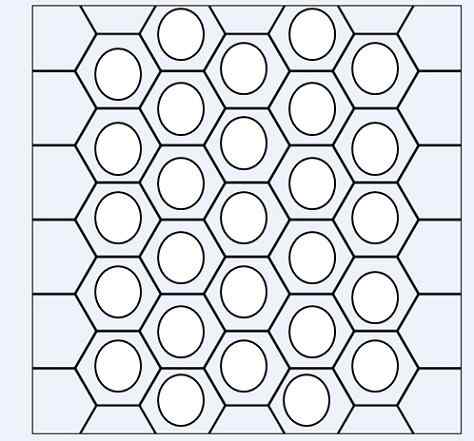 Aromatične ogljikovodike prepoznajo z enotami benncteničnih obročev
Aromatične ogljikovodike prepoznajo z enotami benncteničnih obročev Na zgornji sliki imamo nekakšno omrežje ali mrežo, sestavljeno iz benzenskih obročev. Upoštevajte svoje šesterokotne geometrije in krog v notranjosti. Ta krog predstavlja tisto, kar je znano kot aromatičnost, ki je povsem kemična in nefizična lastnost, neodvisno od vonjav teh ogljikovodikov.
Aromatični ogljikovodiki so med najpomembnejšimi, ekstrahiranimi ali proizvedenimi minerali nafte in ogljika. Benzen je temelj teh ogljikovodikov in njihovih aplikacij, saj iz njega izhaja simfine spojin, ki se uporabljajo kot surovine za proizvodnjo gnojil, plastike, lepil, detergentov, parfumov, zdravil itd.
[TOC]
Kako se imenujejo aromatični ogljikovodiki?
En sam benzenski prstan
Za aromatične ogljikovodike imamo posebnost, da njihova tradicionalna ali običajna imena običajno prevladujejo nad tistimi, ki jih ureja nomenklatura IUPAC.
Vsi vsebujejo benzenski obroč ali obroč, ki ustreza lastnost aromatičnosti. Najpreprostejši lahko imenujemo po benzenu in relativni položaji njihovih substituentov.
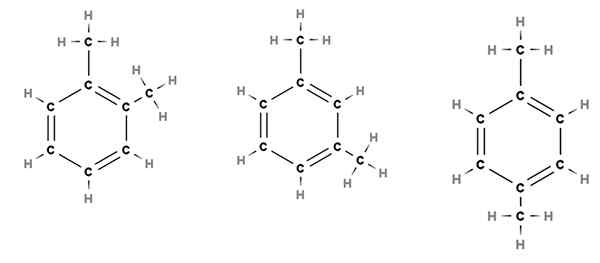 Relativni položaji substituentov v benzenskem obroču za molekulo dimetilbenzena. Vir: Gabriel Bolívar prek Molview.
Relativni položaji substituentov v benzenskem obroču za molekulo dimetilbenzena. Vir: Gabriel Bolívar prek Molview. Na primer razmislite o zgornji sliki. V treh strukturah vidimo šesterokotni obroč benzena, ki ima dva metilna substituenta, Cho3. Tako se ta spojina imenuje dimetilbenzen, ker je sestavljen iz benzena z dvema metilosoma.
Vam lahko služi: kalijev sulfat (K2SO4): struktura, lastnosti, uporabe, sintezaOd leve proti desni vidimo, da ločitev med obema3 Postane večja, kar ne vpliva samo na fizične lastnosti molekule, ampak tudi spreminja njihova imena. Da bi jih razlikovali, saj se vsi imenujejo dimetilbenzen, se uporabljajo Ortho predpone (O-), cilj (m-) in za (p-) (p-).
Zato in spet od leve proti desni imamo: orto-dimetilbenzen, meta-dimetilbenzen in parameterbenzen. Vendar je tradicionalno ime te spojine ksilen, zato postanejo imena: orto-ksilen, meta-ksilen in para-ksilen.
Če obstajata več kot dva različna substituenta, se uporablja za naštevanje ogljikov po enakih pravilih nomenklature kot za vse ogljikovodike.
Več obročev
Za aromatične ogljikovodike z več kot enim benzenskim obročem postanejo tradicionalna imena še pomembnejša. To je zato, ker so sistematična imena, ki opisujejo njihove strukture, okorna in jih je težko zapomniti. Razmislite o primeru naftalena:
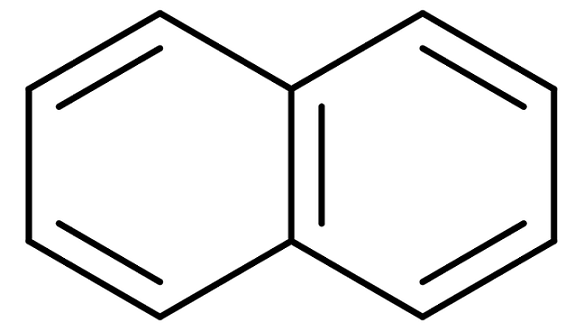 Naftalenska struktura
Naftalenska struktura Naftalen je komercialno znan tudi kot naftalin ali beli kamfor. Vendar je njegovo sistematično ime: biciclo [4,4,0] dec-1,3,5,7,9 Pentana. In to samo za spojino z dvema združenimi benzenskimi obroči; Nomenklatura postane veliko bolj zapletena za spojine s tremi ali več obroči.
Lastnosti aromatičnih ogljikovodikov
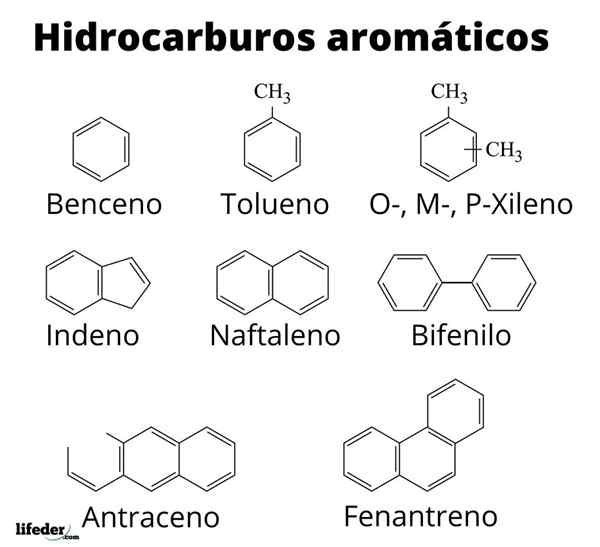 Struktura nekaterih aromatičnih ogljikovodikov
Struktura nekaterih aromatičnih ogljikovodikov Aromatičnost
Aromatični ogljikovodiki vsebujejo obroče, ki upoštevajo Huckle -pravila. To pomeni, da morajo imeti njihovi obroči atome s hibridizacijami SP2, Bodite čim bolj ravni in imajo številne elocced π elektrone, enake 4n + 2. Na primer, benzen je aromatičen, ker ima 6 demociranih elektronov za n= 1 (4 · 1 + 2 = 6).
Visoki odnosi C/H
C/h odnosi za aromatične ogljikovodike so visoki ali večji od 1. Na primer za benzen, c6H6, Vaš c/h je enak 6/6 ali 1. Medtem za naftalen, c10H8, Vaš c/h je enak 10/8 ali 1.25. Kaj to pomeni? Da so ti ogljikovodiki zelo "gazirani" v primerjavi z drugimi spojinami.
Vam lahko služi: sulfonska kislina: struktura, nomenklatura, lastnosti, uporabeRumeni plameni
Prav zaradi svojih visokih c/h odnosov, ko se aromatični ogljikovodiki požgajo ogenj rumeni plameni, produkt nastalih delcev premoga (saje).
Nadomestne reakcije
Aromatični ogljikovodiki lahko svoje vodikove atome nadomestijo s katerim koli drugim substituentom. To dosežemo z dvema vrstama organskih reakcij: aromatična elektrofilna substitucija (SEAR) ali aromatična nukleofilna substitucija (SNAR).
Dišave
Za aromatične ogljikovodike, kot že ime pove, je značilno, da imajo sladki ali močni vonji. Ta lastnost jim je omogočila, da jih načeloma razlikujejo od plinastih ogljikovodikov in nekaterih parafinov hroščev.
Primeri aromatičnih ogljikovodikov
Aromatični ogljikovodiki, strogo gledano, zadevajo le tiste, ki so sestavljeni iz ogljika in vodika. Heteroátomos (ali, p, n, s itd.). Zato bodo omenjeni naslednji primeri, ki jih bomo izpustili spojinam, kot so piridin, furano ali fenol.
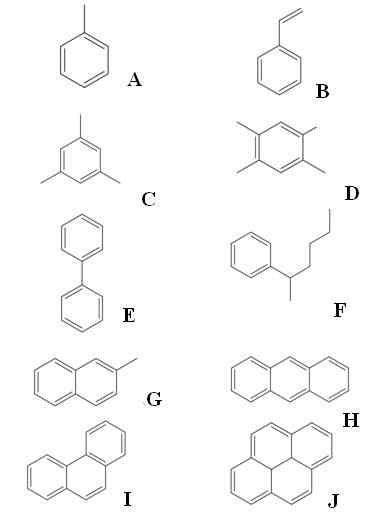 Primeri aromatičnih ogljikovodikov. Vir: Gabriel Bolívar prek Molview.
Primeri aromatičnih ogljikovodikov. Vir: Gabriel Bolívar prek Molview. Zgoraj imamo deset primerov aromatičnih ogljikovodikov. Upoštevajte, da ima vsak vsaj en benzenski obroč. Njihova imena so:
O: Toluen
B: raztezanje
C: Mesitileno
D: pozno
E: bifenil
F: 2-fenilheksan
G: 2-metilnaftalen
H: Antracen
I: Fenantreno
J: Pireno
Od vseh je toluene tisti z največjo industrijsko vrednostjo.
Aplikacije/uporabe
Večina aplikacij aromatičnih ogljikovodikov je sestavljena iz služenja kot surovine za sintezo ali proizvodnje, izdelkov z visoko komercialno vrednostjo. Skoraj vsi se začnejo iz benzena, ki je podvržen več organskim reakcijam, da dobimo funkcionalne derivate.
Vlakna in plastika
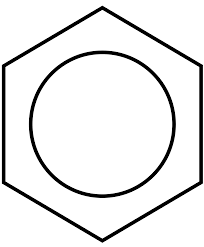 Benzen
Benzen Iz benzena je cikloheksan, ki se pozneje pretvori v druge spojine za sintezo najlona 6 ali najlona 66. Po drugi strani pa lahko raztezanje dobimo tudi iz benzena, ki ga sestavlja polistirenski monomer. Tako imamo polimere, potrebne za proizvodnjo vlaken in plastike.
Vam lahko služi: aktivacijska energijaEpoksi smole
Tudi od benzena je mogoče sintetizirati bisfenol A, s katerim se po različnih sintezi, epoksi smolah, lepilu, lepila in celo slikah pojavijo po različnih poteh sinteze.
Detergenti
Alkibente z dolgimi stranskimi verigami služijo za proizvodnjo detergentov; Med njimi Alkybenzeosulfonates.
TNT
Iz toluena lahko proizvedete TNT: Trinitrotoluene, enega najbolj znanih eksploziva.
Benzojska kislina
Iz toluena dobimo benzojsko kislino kot izpeljano, bistveno spojino za formulacije številnih parfumov, zdravil in hrane.
Topila
Benzen, toluen in Xileno (BTX) so najbolj uporabljena organska topila v raziskavah olja.
Bencin
Aromatični ogljikovodiki so tudi del sestave bencina, z glavno vlogo dviga svojega oktanskega ali oktanskega indeksa.
Reference
- Graham Solomons t.W., Craig b. Fryhle. (2011). Organska kemija. (10th Izdaja.). Wiley Plus.
- Carey f. (2008). Organska kemija. (Šesta izdaja). MC Graw Hill.
- Morrison in Boyd. (1987). Organska kemija. (Peta izdaja). Addison-Wesley Iberoamericana.
- Wikipedija. (2020). Aromatična spojina. Pridobljeno iz: v.Wikipedija.org
- Ed Vitz in sod. (8. septembra 2020). Aromatični ogljikovodiki. Kemija librettexts. Okrevano od: kem.Librettexts.org
- Wyman Elizabeth. (2020). Aromatični ogljikovodiki: definicija, primer in uporaba. Študij. Okrevano od: študij.com
- Boluda, c. J., Macías, m., & González Marrero, J. (2019). Kemična zapletenost avtomobilskega bencina. Znanost, inženiring in aplikacije,2(2), 51–79. Doi: doi.org/10.22206/Cyap.2019.V2i2.PP51-79

