Živo srebro fulminate strukture, lastnosti, pridobivanje, uporabe
- 2208
- 654
- Ignacio Barrows
On Živo srebro To je anorganska spojina, ki jo tvorijo živo srebro (HG), ogljik (C), dušik (N) in elemente kisika (O) (O). Njegova kemična formula je HG (CNO)2. Ne bi smeli zamenjati z živosrebro cianato, ker čeprav imata obe spojini enake elemente, se v slednjih atomi vežejo drugače.
Odkril ga je angleški kemik Edward Howard leta 1800. Vendar pa je skoraj 200 let, preden ga je po nesreči sintetiziral nemški alkimist Johannes Kunckel, ki ga je zaradi eksplozije ni izoliral, vendar je zapustil pisne zapise o uporabljenih sestavinah.
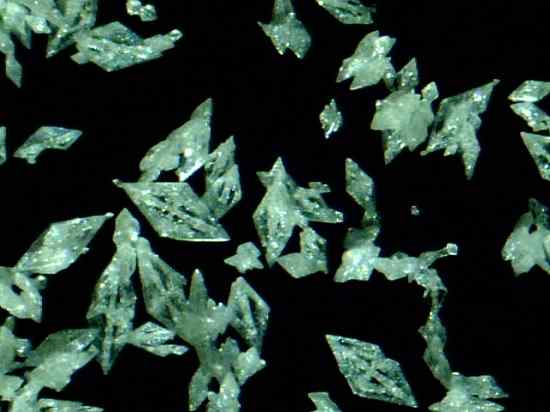
 Mercury Fulminat Crystals HG (CNO)2. Daniel Grohmann/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons.
Mercury Fulminat Crystals HG (CNO)2. Daniel Grohmann/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons. Je primarni eksploziv, zato se uporablja pri tolkalih ali kapsulah za spodbujanje eksplozije drugih snovi. Čeprav je njegova priprava in ohranjanje izjemno nevarna, se je v devetnajstem stoletju široko uporabljala kot detonator v vojni in lovskem orožju.
Trenutno se uporablja za eksplozijo močnih dinamitnih obremenitev pri gradnji predorov in cest ter rudarjenju.
To je očitno izjemno nevarna spojina, ki jo lahko manipulirajo le ljudje z globokim znanjem o tem, kako ravnati z eksplozivi.
[TOC]
Struktura
HG (CNO)2 Je hcno fulminska kislina sol. Vsebuje živo srebro v oksidaciji +2 in dve fulminatni enoti CNO-.
Glede na rentgensko študijo, izvedeno leta 2007 v Nemčiji (poročali v angleščini leta 2008), imajo živo srebro fulminate molekule strukturo ONC-HG-CNO, kjer opazimo, da je živo srebro neposredno povezano z ogljikovimi atomi.
Zveza C-HG-C je linearna; tvori kot 180 °, skupina Fulminat (CNO).
Dolžina povezave C-N je 1,14-1,17 Å (angstromi), kar ustreza trojni šibki povezavi. Povezava N-O je 1,20-1,25 Å, kar kaže na šibko dvojno vez. Angstrom (Å) je dolžinski ukrep in je deset -melonski del metra.
Lahko vam služi: metode ločevanja homogenih mešanic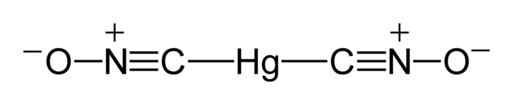 Lewisova struktura živega srebra Fulminata. Benjah-bmm27 / javna domena. Vir: Wikimedia Commons.
Lewisova struktura živega srebra Fulminata. Benjah-bmm27 / javna domena. Vir: Wikimedia Commons. V trdnem stanju, čeprav je zveza C-HG-C linearna, skupina CNO.
 HG molekula (CNO)2 V trdnem stanju. Sivo = živo srebro; Črna = ogljik; modra = dušik; Rdeča = kisik. Benjah-bmm27 / javna domena. Vir: Wikimedia Commons.
HG molekula (CNO)2 V trdnem stanju. Sivo = živo srebro; Črna = ogljik; modra = dušik; Rdeča = kisik. Benjah-bmm27 / javna domena. Vir: Wikimedia Commons. Vendar je po že omenjeni študiji v plinastih stanju celotna molekula popolnoma linearna.
Nomenklatura
- Živo srebro
- Merkurski fulminat
- Živo srebro difullminate
- Živo srebro bisfullminate
- Fulmininska kislina živo srebro sol
- Fulminantno živo srebro
- Eksplozivno živo srebro
Lastnosti
Fizično stanje
Belo do oranžno trdno trdno.
 HG (CNO)2 navlažena trdna. Daniel Grohmann/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons.
HG (CNO)2 navlažena trdna. Daniel Grohmann/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons. Molekularna teža
284,63 g/mol
Tališče
Ne topi se. Segreva pri več kot 100 ° C.
Gostota
4.42 g/cm3
Topnost
Rahlo topno v vodi. Topno v etanolu (c2H5OH) in amonijev hidroksid (NH4OH).
Kemične lastnosti
Je zelo eksplozivna spojina in zelo občutljiva na udarce, udarce ali trenje. Z lahkoto lahko eksplodirate s iskri in plameni. Ko se razpade za živosrebne pline (HG), ogljikov monoksid (CO) in dušik (n2).
Z žveplovo kislino (h2SW4) Koncentracija se pojavi tudi nasilna eksplozija. Klorovodikova kislina jo delno raztopi in pojavi merkurični klorid.
Glede na študijo, izvedeno leta 1981, če je pod nadzorom in zelo počasi segrevanje, pod inertno atmosfero argona, ko doseže 120 ° C, se pojavi neekplozivna razgradnja in nastanejo trdni živosreni.
To je spojina, ki so jo redki časi preučevali zaradi svoje nevarnosti in takšne priložnosti za študij so bile pravočasno zelo oddaljene drug od drugega. Morate delati v temi, da se izognete eksplozijam. Njegove vzorce je treba ohraniti pod vodo in brez svetlobe.
 Hg trdno (CNO)2 Ohranite pod vodo. Daniel Grohmann/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons.
Hg trdno (CNO)2 Ohranite pod vodo. Daniel Grohmann/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons. Pridobivanje
Po njegovem odkritju je bilo komercialno skozi reakcije med etanolom (CHO3Pogl2OH), živo srebro (HG) in dušikova kislina (HNO3).
Lahko vam služi: Clausius-Clapeyronova enačba: za kaj je, primeri, vajeV eni najpomembnejših raziskav o strukturi te spojine raziskovalci predlagajo, da je treba za večjo uspešnost med pripravo, prvo polovico celotne količine etanola je treba dodati mešanici HG in HNO3 preden rjavi plini izginejo.
Z drugimi besedami, pomembno je, da so prisotni dušikovi oksidi, tako da se reakcija nadaljuje.
Najprej se zgodi pretvorba etanola v acetaldehid. Po določenih študijah sledi več oksidacije, nitracije, dekarboksilacije in izločanja dušikove kisline, tako da se tvori fulminat.
Uporabljam kot detonirajoči agent drugih eksploziva
Vojne prijave
Prvi poskusi uporabe živega srebra kot eksplozivnega prahu za strelno orožje so bili frustrirani zaradi izjemne hitrosti in nasilja njihove eksplozije.
Puške in puške so uničili majhne obremenitve te spojine. Zgodilo se je tudi s koščki topništva in granat v vojaških testih.
Vendar ga je leta 1822 angleški Wright prvič uporabil kot gasilca v svojih športnih lovskih puškah. Nato je bila v Britani uvedena njegova uporaba v pehotnih musketah in nato po vsej Evropi.
 V devetnajstem stoletju je bil Fulminat Merkur uporabljen kot detonator številnih vrst vojnih orožij. Avtor: Vetsikas Dimitris. Vir: Pixabay.
V devetnajstem stoletju je bil Fulminat Merkur uporabljen kot detonator številnih vrst vojnih orožij. Avtor: Vetsikas Dimitris. Vir: Pixabay. Do zgodnjih 1900 -ih je bil edini detonator, ki se uporablja za snemanje kakršnih.
Mirne aplikacije
Ta spojina je igrala pomembno vlogo pri razvoju eksploziva v mirne namene.
Njegova vloga v izumu dinamita s strani Alfreda Nobel je bila zelo pomembna. Ta znanstvenik je kombiniral nitroglicerin, močan eksploziv, z poroznim materialom, zemljo diatomov. Toda detonacija te mešanice je težko z iskri ali stenj.
Nobel je presegel to težavo z uporabo živega srebra, ki ga Fulminat Fulminat, ki so bile zanesljive pri njihovi uporabi. Ta kombinacija trenutno omogoča njegovo uporabo pri rudarjenju, izkoriščanju kamnolomov, gradnje tunelov in gradbeništva za gradnjo cest, železnic, pristanišč itd.
Lahko vam služi: buteno Široko se uporablja kot detonator eksplozij pri rudarstvu in gradnji cest. Avtor: Nyamdorj. Vir: Pixabay.
Široko se uporablja kot detonator eksplozij pri rudarstvu in gradnji cest. Avtor: Nyamdorj. Vir: Pixabay. Sam Alfred Nobel je poudaril temeljni pomen živega srebra v razvoju gradbeništva, ki je spodbujal dinamit.
Tveganja
Je zelo nestabilna in izjemno eksplozivna spojina.
 Avtor: Clker-brez vektorjev. Vir: Pixabay.
Avtor: Clker-brez vektorjev. Vir: Pixabay. Proizvaja akutno strupenost. Je strupen, če ga zaužijemo, vdihava ali če pride v stik s kožo. Enostavno proizvede kontaktni dermatitis. Povzroči škodo na notranjih organih, če je oseba izpostavljena ponavljajoči se.
Zelo strupeno za vodno in kopensko življenje z neprekinjeno dolgoročno nevarnostjo.
Reference
- Svinec, d.R. (Urednik) (2003). Priročnik za kemijo in fiziko CRC. 85th CRC Press.
- Ali.S. Nacionalna knjižnica medicine. (2019). Živo srebro se razpravlja. Okrevano od PubChema.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Munroe, c.In. (1912). Opomba o proizvodnji živega srebra. Journal of Industrial & Engineering Chemistry 1912, 4, 2, 152-153. Okrevani iz lokalov.Acs.org.
- Kurzer, f. (2000). Fulminska kislina v zgodovini organske kemije. J Chem. Educa. 2000, 77, 7, 851. Okrevani iz lokalov.Acs.org.
- Beck, w. in klapötke, t.M. (2008). Živo srebro Fulminate: ONC-HG-CNO ali CNO-HG-ENC-A DFT Študija. Časopis za molekularno strukturo: Theochem 848 (2008) 94–97. Okrevano od Scientirect.com.
- Wilson, e. (2007). Živo srebro Fulminate je revirano. Arhiv za kemične in inženirske novice 2007, 85, 36, 10. Okrevani iz lokalov.Acs.org.
- Rjava, m.In. in lastovke, g.M. (1981). Toplotna razgradnja srebra (I) in živega srebra (ii) soli 5-nitrotetrazole in živega srebra (ii). Thermochimica Acta, 49 (1981) 333–349. Okrevano od Scientirect.com.
- Alderson, h.In. (1910). Do nove poklicanosti dermatoze. Dermatitis zaradi suhega fulminata živega srebra. Cal State J Med 1910 AP; 8 (4): 114. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Fundacija Wikimedia (2020). Živo srebro (ii). Pridobljeno iz.Wikipedija.org.
- « Živosrebrni klorid (ii) struktura, lastnosti, pridobivanje, uporabe
- Značilnosti in prispevki kmetijskih civilizacij »

