Amonijeva fosfatna struktura, lastnosti, pridobivanje, uporabe
- 645
- 112
- Ms. Pablo Lebsack
On Amonijev fosfat To je družina fizioloških spojin, ki izhajajo iz reakcije med fosforno kislino in amonijakom. Po anorganski nomenklaturi bi to ime ustrezalo soli, katere kemijska formula je (NH4)3Po4, Sestavljen iz amonijevih kationov, NH4+, in fosfatne anione, po43-.
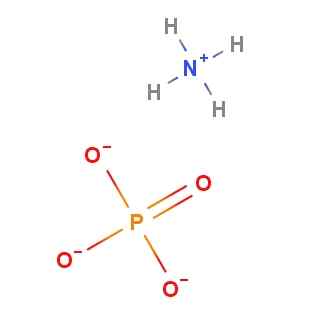
Na spodnji sliki je prikazana predstavitev teh ionov. (NH4)3Po4 Znan je tudi kot tribasični fosfat amonijevega ali triamoničnega fosfata. Ta imena so posledica dejstva, da je, kot je bilo opaženo43- Na voljo ima tri negativne kisike, ki lahko sprejme protone, h+, okoliške kisline.
 Amonijevi fosfatni ioni. Vir: Gabriel Bolívar prek Molview.
Amonijevi fosfatni ioni. Vir: Gabriel Bolívar prek Molview. In ravno to se zgodi z NH4+ lastne strukture. Zato je amonijev fosfat nestabilen, razpadajoči v NH4H2Po4 in nh3. Zato ta sol odpušča močan vonj amoniaka.
Druge soli amonijevih fosfatov so bolj stabilne in uporabne. Na primer, v kmetijstvu se uporabljajo kot materiali za gnojila, kristali nekaterih pa imajo celo optično in fizično uporabo.
Ta družina soli je preprosta, a raznolika, ko se kislost medija spremeni tam, kjer se nahaja.
[TOC]
Struktura
Amonijev fosfat je sestavljen iz NH ionov4+ in po43-, obe tetraedrski geometriji. Elektroni PO43- Razdeljeni so med tremi atomi kisika P-O vezi-, katere negativna obremenitev močno pritegne NH4+. Zato bi lahko mislili, da je kristalna struktura (NH4)3Po4 je močan.
V njem, NH ioni4+ in po43- Najdemo jih v razmerju 3: 1, kar pomeni, da v njihovih kristalih obstajajo trojni NH ioni4+ Kaj pa ions po43-. Tako njene elektrostatične interakcije na koncu določijo tetragonalni kristal.
Vam lahko služi: radio: struktura, lastnosti, uporabe, pridobivanjeEnako se delno dogaja z drugimi soli tega fosfata: (NH4)2HPO4 in nh4H2Po4, v katerem Po43- je osvojil eno ali dva h+, oziroma. V svojih predvsem tetragonalnih kristalih so elektrostatične interakcije šibkejše zaradi svojih manjših ionskih obremenitev.
Vendar so energijsko bolj stabilni, zlasti NH4H2Po4, No, predstavlja največjo tališče.
Po drugi strani lahko amonijeve fosfatne soli tvorijo tudi hidrate, ki v svoje kristalne strukture vključujejo molekule vode.
Lastnosti aminonijevega fosfata
Imena
(NH4)3Po4
Ta formula, strogo po anorganski nomenklaturi, ustreza soli fosfatni soli. Druga sprejeta imena so:
-Tribazični amonijev fosfat
-Triammonium ali triamonični fosfat
(NH4)2HPO4
Ta sol predstavlja več imen v skladu z nomenklaturo Preference. Najpogostejši, razen diamoničnega fosfata, so:
-Fosfat amonijeve kisline
-Dibasični amonijev fosfat
Za razliko od (nh4)3Po4, Sestavljen je iz NH ionov4+ in HPO42- V deležu 2: 1.
Nh4H2Po4
Ta sol ustreza "najbolj kisli različici" amonijevega fosfata. V njem, po43- je osvojil dva h+, s tem zmanjšanje svoje ionske obremenitve na h2Po4-. Zato so njihova najpogostejša imena:
-Monobasični amonijev fosfat (ker komaj ima kisik, ki lahko sprejme protone)
-Amonium diácido fosfat
Nekatera prejšnja imena lahko spremenite tudi z:
-Dihidrogen amonijev fosfat
-Monoamonijev fosfat
Kot je razvidno, je veliko možnih imen. Pomembno je vedeti, kako jih neposredno povezati s formulami katere koli od treh soli, ki ustrezajo družini amonijevih fosfatov.
Molarne mase
(NH4)3Po4: 149.09 g/mol
(NH4)2HPO4: 132.06 g/mol
Nh4H2Po4: 115.025 g/mol
Fizični videz
Amonijeve fosfatne soli imajo skupno, da so vse bele. Z izjemo triamoničnega ali tribaznega fosfata amonijasta ostale soli ne zavrnejo vonja amonijaka v normalnih pogojih.
Vam lahko služi: aromatična nukleofilna substitucija: učinki, primeriFuzijske točke
(NH4)3Po4 Se pokvari, preden se lahko stopi. Medtem (NH4)2HPO4 stopi pri 155 ° C in NH4H2Po4 pri 190 ° C. Največja fuzijska točka NH4H2Po4 kaže na večjo stabilnost in močnejšo ionsko vez.
Vrelišča
Datoteko, ko se razbijejo pri topinju.
Topnost
Amonijeve fosfatne soli so v vodi zelo topne, saj so (NH4)3Po4 Higroskopska trdna snov. Vendar so netopni v etanolu, acetonu in tekočem amonijaku.
Razgradnja
Vse amonijeve fosfatne soli lahko sprostijo amoniak pri razpadu. Tudi glede na toplotno intenzivnost se razgradi na fosforno kislino, da končno sprostijo škodljive pline iz dušika in fosforjevih oksidov.
Pridobivanje
Amonijeve fosfatne soli dobimo z reakcijo nevtralizacije, ki se je pojavila med fosforno kislino in amoniakom:
H3Po4 + 3 nh3 → (nh4)3Po4
Kot je razvidno, če je želeno. Na splošno se uporablja fosforni oksid, str2Tudi5, kot vir fosforja za svojo kislino.
Bolj h3Po4 biti tam, največja bo proizvodnja NH4H2Po4 ali (nh4)2HPO4 (več kislin) kot (NH4)3Po4 (bolj osnovno).
Pravzaprav so NH4H2Po4 (Zemljevid za svojo kratico v angleščini: Monoamonijev fosfat) in (NH4)2HPO4 (DAP) Amonijeve fosfatne soli, ki imajo večjo komercialno vrednost. Medtem (NH4)3Po4 To je manj prodano, ravno zato, ker je najbolj nestabilen in, morda najdražji za pripravo.
Lahko vam služi: Avogadro Številka: Zgodovina, enote, kako se izračuna, uporabljaPrijave
Ena neposrednih posledic prejšnjega odstavka je, da je večina uporabe amonijevih fosfatnih soli posledica NH4H2Po4 in (nh4)2HPO4. (NH4)3Po4, Po drugi strani pa skoraj nima koristi, ker hitro razpade.
Gnojila
 Kot gnojilo se uporablja amonijev fosfat. Vir: pxhere.
Kot gnojilo se uporablja amonijev fosfat. Vir: pxhere. Amonijeve fosfatne soli so dobra gnojila, saj zagotavljajo dve bistveni hranili za razvoj rastlin: dušik in fosfor. Poleg tega so topni v vodi, zato hitro postanejo na voljo na tleh za ustrezno absorpcijo skozi korenine.
Shranjeni so brez kakršnih koli težav in če ni požara, ne odpravljajo amoniaka, plina, ki lahko poškoduje rastlinska tkiva.
Zaostali za plamen
 Amonijev fosfat je del nekaterih zaviralcev plamena. Vir: Coconino National Forest/CC by-S (https: // createCommons.Org/licence/by-sa/2.0
Amonijev fosfat je del nekaterih zaviralcev plamena. Vir: Coconino National Forest/CC by-S (https: // createCommons.Org/licence/by-sa/2.0 Amonijeve fosfatne soli ob razpadu sproščajo več plinov, ki sicer škodljivi, kisik iz zraka izpodrinejo v polnem ognju. Zato se uporabljajo kot zaostali požar. Na ta način se napredek plamena upočasni ali zavleče.
Optika in fizična
NH4H2Po4 Uporablja se v optičnih aplikacijah, ker njihovi kristali kažejo bizo, torej imajo dvojno lomanje. Imajo tudi piezoelektrične lastnosti, zato se uporabljajo pri pretvornikih.
Reference
- Shiver & Atkins. (2008). Anorganska kemija. (Četrta izdaja). MC Graw Hill.
- Wikipedija. (2020). Amonijev fosfat. Pridobljeno iz: v.Wikipedija.org
- Elsevier b.V. (2020). Amonijev fosfat. Znanstveno. Pridobljeno iz: SCINCEDIRECT.com
- Diane Milner. (4. februar 2019). Številne uporabe amonijevega fosfata. Noah Technologies. Okrevano od: informacije.Noahtech.com
- Nacionalni center za informacije o biotehnologiji. (2020). Tribazični amonijev fosfat. Baza podatkov Pubchem., Cid = 57517680. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Milek j.T., Neuberger m. (1972) Amonijev dihidrogen fosfat (ADP). V: linearni elektrooptični modularni materiali. Springer, Boston, MA.
- Mozaično podjetje. (2020). Monoamonijev fosfat (MAP). Okrevano od: posek.com
- « Značilnosti ustnega jezika, funkcije, primeri
- Značilnosti literarnega pregleda, deli, funkcija, primeri »

