Razpršena faza
- 2900
- 584
- Ms. Pablo Lebsack
 Vir: Gabriel Bolívar
Vir: Gabriel Bolívar Kaj je razpršena faza?
The razpršena faza To je tisti, ki je manjši delež v disperziji in je sestavljen iz zelo majhnih delcev agregatov. Medtem se najpogostejša in neprekinjena faza, kjer se delci lažejo. Primer je voda s sladkorjem, kjer bi bila razpršena faza sladkor in razpršena voda.
Disperzije so razvrščene glede na velikost delcev, ki tvorijo razpršeno fazo, ki lahko ločijo tri vrste disperzij: nesramne disperzije, koloidne rešitve in resnične rešitve.
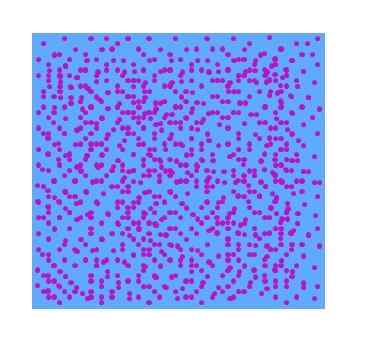
Na vrhunski sliki je mogoče opaziti hipotetično razpršeno fazo vijoličnih delcev v vodi. Kot rezultat, kozarec, poln te razpršenosti, ne bo pokazal preglednosti vidne svetlobe; to pomeni, da bo videti kot vijolični tekoči jogurt. Vrsta disperzij se razlikuje glede na velikost teh delcev.
Ko so "odlični" (10-7 m) govori o nesramnih disperzijah in lahko usedli z delovanjem gravitacije; koloidne rešitve, če se njihove velikosti gibljejo med 10-9 M in 10-6 M, zaradi česar so vidni le z ultramikoskopom ali elektronskim mikroskopom; in resnične rešitve, če so njihove velikosti manjše od 10-9 M, ki lahko prečka membrane.
Prave rešitve so torej vse, ki so popularno znani, na primer kis ali sladka voda.
Značilnosti razpršene faze
Rešitve predstavljajo poseben primer disperzij, ki so zelo zanimive za poznavanje fiziokvizije živih bitij. Večina bioloških snovi, tako znotrajceličnih kot zunajceličnih, najdemo v obliki disperzij klicev.
Brownovo gibanje in Tyndall učinek
Delci razpršene faze koloidnih raztopin imajo majhno velikost, ki ovira njihovo sedimentacijo. Poleg tega se delci nenehno premikajo v naključnem gibanju in trkajo drug na drugega, kar tudi otežuje usedline. Ta vrsta gibanja je znana kot Browan.
Vam lahko postreže: vijolično stekloZaradi relativno velike velikosti razpršenih faznih delcev imajo koloidne raztopine mračen ali celo neprozoren videz. To je zato, ker je svetloba razpršena, ko se koloid prečka, pojav, znan kot Tyndall Effect.
Heterogenost
Koloidni sistemi so nehomogeni sistemi, saj je razpršena faza sestavljena iz delcev s premerom med 10-9 M in 10-6 m. Medtem ko so delci raztopine manjše velikosti, običajno manj kot 10-9 m.
Delci razpršene faze koloidnih raztopin lahko križajo filtrirni papir in glineni filter. Vendar ne morejo prečkati dializnih membran, kot so celofan, kapilarni endotel in kolodion.
V nekaterih primerih so delci, ki tvorijo razpršeno fazo. Ko so v vodni fazi, se beljakovine zložijo, tako da hidrofilni del zunaj ostanejo zunaj za večjo interakcijo z vodo, skozi ionske sile ali s tvorbo vodikovih mostov.
Beljakovine tvorijo retikularni sistem znotraj celic, ki lahko prevzamejo del razpršilnika. Poleg tega površina beljakovin služi za povezovanje majhnih molekul, ki daje površinski električni naboj, kar omejuje interakcijo med molekulami beljakovin in jim preprečuje sestavljanje strdkov, ki povzročajo usedljivost.
Stabilnost
Koloidi so razvrščeni glede na privlačnost med razpršeno fazo in fazo razprševanja. Če je faza razprševanja tekoča, so koloidni sistemi razvrščeni kot sonci. Ti so razdeljeni na delifilos in liofobe.
Lahko vam postreže: kalijev klorat (KCLO3)Liofilni koloidi lahko tvorijo resnične rešitve in so termodinamično stabilni. Po drugi strani pa lahko liofobi koloidi tvorijo dve fazi, saj sta nestabilna, čeprav stabilna s kinetičnega vidika. To jim omogoča, da dolgo ostanejo v razpršenem stanju.
Razpršeni fazni primeri
V treh fizičnih stanjih zadeve se lahko pojavita tako faza razprševanja kot razpršena faza, to je: trdna, tekoča ali plinasta.
Običajno je faza neprekinjene ali razprševanja v tekočem stanju, vendar je mogoče najti koloide, katerih sestavne dele najdemo v drugih stanjih združevanja snovi.
Možnosti kombinacije faze razprševanja in razpršene faze v teh fizičnih stanjih je devet.
Vsaka bo razložena z nekaterimi primeri.
- Trdne rešitve: Ko je faza razprševanja trdna, jo lahko kombinirate s razpršeno fazo v trdnem stanju in tvori tako imenovane trdne rešitve.
To so primeri teh interakcij: veliko jeklenih zlitin z drugimi kovinami, nekaj barvitih draguljev, ojačane gume, porcelana in pigmentirane plastike.
- Trdne emulzije: Faza razprševanja trdnega stanja lahko kombiniramo s tekočo razpršeno fazo, ki tvori tako imenovane trdne emulzije. So primeri teh interakcij: sir, maslo in žele.
- Trdne pene: Faza razprševanja kot trdne snovi je mogoče kombinirati z razpršeno fazo v plinastem stanju, ki predstavlja tako imenovane trdne pene. Primeri teh interakcij so goba, guma, kamnita in gumijasta pena.
- Podplati in geli: Faza razprševanja v tekočem stanju se kombinira z razpršeno fazo v trdnem stanju, ki tvori sonce in gele. Primeri teh interakcij so magnezijsko mleko, slike, blato in pudin.
Vam lahko služi: rešitve za amortiber- Emulzije: Faza razprševanja v tekočem stanju se kombinira z razpršeno fazo tudi v tekočem stanju, ki proizvaja tako imenovane emulzije. Primeri teh interakcij so mleko, smetana za obraz, solatni prelivi in majoneza.
- Pene: Faza razprševanja v tekočem stanju se kombinira z razpršeno fazo v plinastem stanju, ki tvori peno. Primeri teh interakcij so krema za britje, stepena smetana in pivska pena.
- Trdni aerosoli: Faza razprševanja v plinastem stanju je kombinirana s razpršeno fazo v trdnem stanju, kar povzroči tako imenovane trdne aerosole. Primeri teh interakcij so dim, virusi, korpuskularni materiali v zraku, materiali, ki jih oddajajo izpušne cevi avtomobilov.
- Tekoči aerosoli: Faza razprševanja v plinastim stanju je mogoče kombinirati z razpršeno fazo v tekočem stanju, kar predstavlja tako imenovana tekoča razpršila. Primeri teh interakcij so megla, megla in rosa.
- Resnične rešitve: Faza razprševanja v plinastim stanju je mogoče kombinirati z plinasto fazo v plinastem stanju, ki tvori plinaste mešanice, ki so resnične rešitve in ne koloidne sisteme. Primeri teh interakcij so zrak in plin osvetlitve.
Reference
- Whitten, Davis, Peck & Stanley. Kemija (8.ª Ed.). Cengage učenje.
- Toppr (s.F.). Klasifikacija koloidov. Okrevano od: toppr.com
- Jiménez Vargas, J in Macarulla. J. M. (1984). Fiziološka fizikalnakemija, šesta izdaja. Interameriški uvodnik.
- Madhusha. Razlika med fazo razpršenosti in disperzijsko medum. Okreval od: pediaa.com

