Dimetilanilaninska struktura, lastnosti, sinteza, uporablja
- 1949
- 365
- Ricky Dach
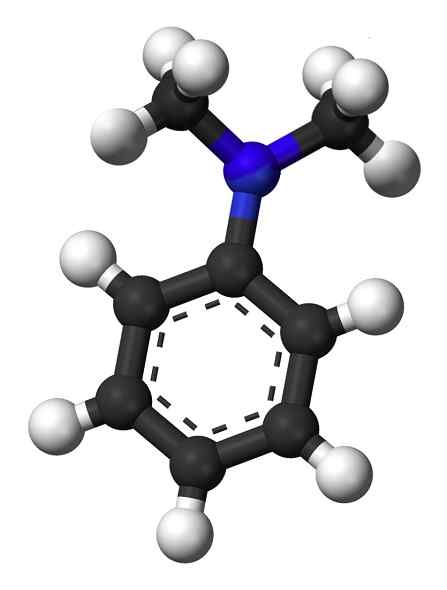
The dimetilanilin o Dimetilfenillamin je organska spojina, ki jo tvori benzenski obroč z amino skupino, nadomeščeno z dvema metilnima skupinama. Njegova kemična formula je c8HenajstN.
Znan je tudi kot N, N-dimetilanil, saj je derivat katerega koli, v katerem se vodika amino skupin nadomesti z dvema metilnima skupinama. Zaradi tega je terciarni amin.
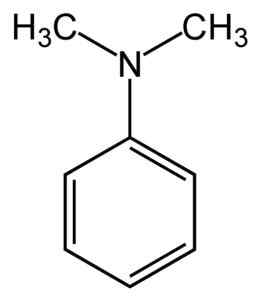 Struktura N, N-dimetilanilanilina. Noben strojno berljiv avtor ni zagotovil. Mysid predpostavlja (na podlagi zahtevkov za avtorske pravice). [CC BY-SA 3.0 (http: // creativeCommons.Org/licence/by-sa/3.0/]]. Vir: Wikipedia Commons.
Struktura N, N-dimetilanilanilina. Noben strojno berljiv avtor ni zagotovil. Mysid predpostavlja (na podlagi zahtevkov za avtorske pravice). [CC BY-SA 3.0 (http: // creativeCommons.Org/licence/by-sa/3.0/]]. Vir: Wikipedia Commons. N, N-dimetilanil je bledo rumena do rjava mastna tekočina z značilnim vonjem po aminih. Je osnovna spojina in reagira z dušikovo kislino, ki tvori nitrosokompoziran. Ko je izpostavljen zraku, postane rjava.
Uporablja se pri proizvodnji barvil za slike. Uporablja se tudi kot aktivator polimerizacijskih katalizatorjev in v mešanicah, ki se uporabljajo za snemanje slik. Po drugi strani je bila uporabljena pri sintezi antibakterijskih spojin ali antibiotikov kot nekaterih cefalosporinov, pridobljenih s penicilinom. N, N-dimetilanilin je tudi osnova za pridobivanje drugih kemičnih spojin.
Je vnetljiva tekočina in ko se segreva, dokler razgradnja ne oddaja strupenih hlapov. Akutna izpostavljenost človeka N, N-dimetilanilin lahko med drugimi simptomi privede do negativnih učinkov, kot so glavoboli, omotica, zmanjšanje kisika v krvi in modrikasto obarvanost kože.
[TOC]
Struktura
Naslednja slika prikazuje prostorsko strukturo N, N-dimetilanila:
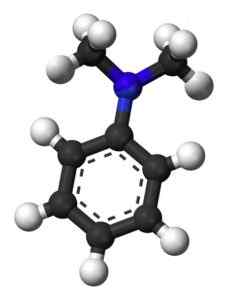 Prostorska struktura N, N-dimetilanila. Esquilo [javna domena]. Vir: Wikipedia Commons.
Prostorska struktura N, N-dimetilanila. Esquilo [javna domena]. Vir: Wikipedia Commons. Nomenklatura
- N, N-dimetilanilin
- Dimetilanilin
- Dimetilfenillamin
- N, N-dimetil bencenamin
N je nameščena v imenu, ki kaže, da dve metilni skupini (-CH3) so pritrjeni na dušik (n) in ne na obroč Benncénico.
Lastnosti
Fizično stanje
Bleda do rjave tekočine.
Molekularna teža
121.18 g/mol.
Lahko vam služi: Anion: Trening, značilnosti in vrsteTališče
3 ° C.
Vrelišče
194 ° C.
Plamenišče
63 ° C (metoda zaprte skodelice). To je najmanjša temperatura, pri kateri lahko vklopite hlape, če se na njem prenese plamen.
Parni tlak
0,70 mm Hg pri 25 ° C.
Temperatura samostojnosti
371 ° C. To je najmanjša temperatura pri spontano gorečem atmosferskem tlaku, brez zunanjega vira toplote ali plamena.
Gostota
0,9537 g/cm3 pri 20 ° C.
Lomni količnik
1.5582 do 20 ° C.
Topnost
V vodi je zelo malo topno: 1.454 mg/l A 25 ° C.
Prosto topno v alkoholu, kloroformu in etru. Topno v acetonu, benzenu in oksigeniranem ter kloriranem topilu.
Osnovna konstanta
Kb 11.7, kar kaže na lahkoto, s katero ta spojina sprejema vodikov ion vode.
Kemične lastnosti
N, N-dimetilanil je osnovna spojina. Reagira z ocetno kislino, da dobi acetat N, N-dimetilanilinio.
Skupina -n (izberite3)2 N je N-dimetilanila močnega aromatičnega substitucijskega aktivatorja v položaju za benzenskega obroča.
Reagira z natrijevim nitritom (nano2) V prisotnosti klorovodikove kisline (HCl), ki tvori p-nitroso-n, n-dimetilanilt. Tudi z dušikovo kislino ustvari isti sestavljeni nitrosado v položaju za.
Ko reagirate N, N-dimetilanilin z benzezonijevim kloridom, v nežno kislem mediju, je azokompoziran AR-N = N-AR ', kjer je AR aromatična skupina. Molekule z azo skupinami so močno obarvane spojine.
Tveganja
Ko se ogreje na njegovo razgradnjo, oddaja zelo strupene hlape dušikovih oksidov štx.
Je gorljiva tekočina.
Počasi se razpada v vodi, ki je izpostavljena sončni svetlobi. Ni biorazgraden.
Je hlapna od mokrih tal in vodnih površin. Ne izhlapete suhe zemlje in se premikajte skozi to. Se ne kopiči v ribah.
Vam lahko služi: železni sulfid (ii): lastnosti, tveganja in uporabeLahko absorbira koža. Tudi vdihavanje ga hitro absorbira. Izpostavljenost človeka je N, N-dimetilanilin lahko zmanjša vsebnost kisika v krvi, kar ima za posledico modrikasto barvo kože.
Akutno vdihavanje te spojine lahko privede do negativnih učinkov za centralni živčni sistem in krvni sistem z glavoboli, cianozo in omotico.
Sinteza
Se lahko zgodi na več načinov:
- Od anilina in metanola pod pritiskom v prisotnosti kislinskih katalizatorjev, kot je H2SW4. Dobimo sulfat, ki postane osnova z dodajanjem natrijevega hidroksida.
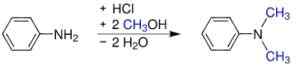 S sinteza, n-dimetilanil. Werderkli - lastno delo. Javna domena. Vir: Wikipedia Commons.
S sinteza, n-dimetilanil. Werderkli - lastno delo. Javna domena. Vir: Wikipedia Commons. - Prehod anilinske pare in dimetil etra na aktiviranem aluminijevem oksidu.
- Segrevanje mešanice anilina, anilinijevega klorida in metanola pod pritiskom in nato destiliranja.
Prijave
V barvni industriji
Za lastnost reakcije z bencenodiazonijevim kloridom, ki tvori azokompistos, se N-dimetilanil uporablja kot posrednik pri proizvodnji barvil.
To je surovina v sintezi barvil družine metil vijolice.
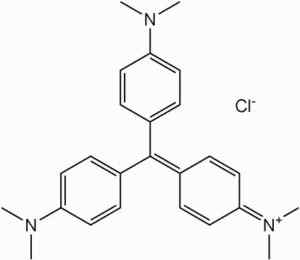 Metilno vijolično barvanje. Noben strojno berljiv avtor ni zagotovil. Shaddack je domneval (na podlagi zahtevkov za avtorske pravice). [Javna domena]. Vir: Wikipedia Commons
Metilno vijolično barvanje. Noben strojno berljiv avtor ni zagotovil. Shaddack je domneval (na podlagi zahtevkov za avtorske pravice). [Javna domena]. Vir: Wikipedia Commons Pri izdelavi fotokaktivnih mešanic
N, N-dimetilanila je del fotookrebilne mešanice, ki doživlja reakcijo ozdravitve kot posledica visoke občutljivosti na vidno svetlobo ali tesno infrardeče.
N, N-dimetilanilin je ena izmed komponent mešanice, ki povzročajo ozaveščenost o valovnih dolžinah, tako da je sestava ozdravljena z nizkoenergijsko svetlobo valovne dolžine.
Lahko vam služi: derivati benzenaOcenjuje se, da mora funkcija N, N-dimetilanila verjetno zatreti reakcijo končne reakcije radikalne polimerizacije, ki jo povzroča kisik.
V proizvodnji vlaken
N, N-dimetilanilin se uporablja kot katalitični tesnik v določenih smolah iz steklenih vlaken.
V sintezi antibiotikov
N, N-dimetilanilin sodeluje pri sintezi cefalosporinov, ki temeljijo na penicilinih.
Penicilin sulfoksidi se pretvorijo v cefeme, kadar se segrejejo v prisotnosti osnovnih katalizatorjev, kot so N, N-dimetilaniln.
Ti cefalosporini imajo antibakterijsko delovanje proti gram-pozitivnim in gram-negativnim organizmom, pa tudi proti stafilokokom, odpornim proti penicilinu.
 Antibiotiki. Alina Kupsova. Vir: Pixabay.
Antibiotiki. Alina Kupsova. Vir: Pixabay. Vendar je treba opozoriti, da N, N-dimetilanilina ostane v teh antibiotikih kot nečistoča.
O kemičnih reakcijah
N, N-dimetilanilin se uporablja pri aktivaciji katalizatorjev polimerizacije olefina.
Uporablja se skupaj s pentafluorofenolom (c6F5Oh) s katero tvori ionsko spojino [hnphme2]+[H (OC6F5)2]-. Ta ionska spojina ima en ali dva aktivna protona, ki aktivirata katalizator na podlagi prehodne kovine.
Poleg tega je bil v proizvodnji smol uporabljen N-dimetilanilin kot pospeševalnik polimerizacije ali promotor za poliestrske smole. Njegovo delovanje ustvarja hitro strjevanje smole.
V več aplikacijah
Uporablja se v sintezi drugih kemičnih spojin, na primer vanilin in kot posrednik za farmacevtska zdravila.
Uporablja se tudi kot topilo kot alkilirajoče sredstvo, kot stabilizator in za izdelavo slik in premazov.
Reference
- S. Nacionalna knjižnica medicine. (2019). N, N-dimetilanilin. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Morrison, r.T. in Boyd, r.N. (2002). Organska kemija. 6. izdaja. Prentice-Hall.
- (2000). N, N-dimetilanilin. Povzetek. Pridobljeno iz EPA.Gov
- Zanaboni, str. (1966). Nenasičena poliestrska solna sestava HAVH stabilnost in hitro ozdravitev pri nizkih temperaturah z mešanico dimetilanila, trenhanolamina in difenilamina. Ali.S. Patent št. 3.236.915. 22. februar 1966.
- Nudelman, a. in McCaully, r.J. (1977). Postopek za preureditev penicilinov v cefalosporine in vmesne komponene. Ali.S. Patent št. 4.010,156. 1. marec 1977.
- Kouji inaishi (2001). Fotocirano sestavo. Ali.S. Patent št. 6.171.759 B1. 9. januar 2001.
- Luo, l. et al. (2012). Ionska Bransted kislina. Ali.S. Patent št. 8.088.952 B2. 3. januar 2012.

