Tartarična kislina
- 3696
- 828
- Dexter Koch
Pojasnjujemo, kaj je tartarična kislina, njegove fizikalne in kemijske lastnosti, njene strukture in njene uporabe
Kaj je vinarna kislina?
On tartarična kislina To je organska spojina, katere molekularna formula je COOH (CHOH)2COOH. Ima dve karboksilni skupini; To pomeni, da lahko izpustite dva protona (h+). Z drugimi besedami, gre za diprotično kislino. Lahko ga uvrstimo tudi med aldarsko kislino (kisli sladkor) in derivat za sukcinsko kislino.
Njegova sol je znana že od nekdaj in je eden od sekundarnih izdelkov vinske izdelave. Kristaliziran je kot bela usedlina, krščena kot "vinski diamanti", ki se kopiči v plutovini ali na dnu sodov in steklenic. Ta sol je kalijev biitartrat (ali kalijeva kislina tartrato).
Soli iz tartarične kisline imajo skupno prisotnost enega ali dveh kationov (NA+, K+. Nh4+, AC2+, itd.) Ker s sproščanjem svojih dveh protonov ostane negativno nabit z obremenitvijo -1 (kot pri Biterrato Salts) ali -2.
Ta spojina je bila predmet preučevanja in poučevanja organskih teorij, povezanih z optično dejavnostjo, natančneje s stereokemijo.
Kje je tartarna kislina?
Tartarska kislina je sestavni del številnih rastlin in hrane, kot so marelica, avokado, jabolka, tamarindo, sončnična semena in grozdje.
V procesu staranja vin je ta kislina - do hladnih temperatur - kombinirana s kalijem, da se kristalizira kot tartrato. V rdečih vinih je koncentracija teh tartatov manjša, v belih vinih.
Tartrate so soli belih kristalov, ko pa oklujijo nečistoče alkoholnega okolja, pridobijo rdečkaste ali vijolične tone.
Vam lahko služi: reakcija premikaStruktura tartarne kisline
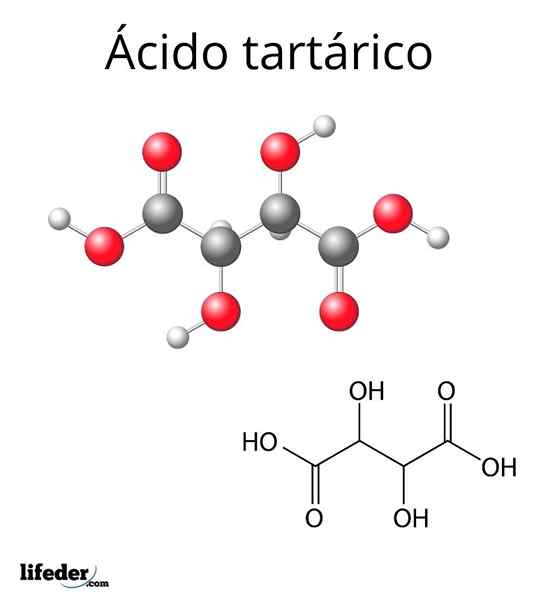
 Molekularna struktura vintarične kisline
Molekularna struktura vintarične kisline Molekularna struktura vinalne kisline je predstavljena na zgornji sliki. Karboksilne skupine (-Cooh) so nameščene na stranskih koncih in so ločene s kratko dvema ogljikovo verigo (c2 in c3).
Vsak od teh ogljikov je povezan z H (belo krogla) in skupino OH. Ta struktura lahko zasuka povezavo C2-C3, Tako ustvari več skladb, ki stabilizirajo molekulo.
To pomeni, da je osrednja povezava zlomljene molekule kot vrtečega se valj, zaporedno izmenično izmenično prostorsko razpolaganje skupin -Cooh, H in OH (Newmanove projekcije).
Na primer na sliki dve OH skupini kažeta v nasprotne smeri, kar pomeni, da sta v protipomnilnih položajih drug z drugim. Enako velja za skupine -Cooh.
Druga možna konformacija je nekaj zasenčenih skupin, v katerih sta obe skupini usmerjeni v isto smer. Te konformacije ne bi imele pomembne vloge v strukturi spojine, če bi vse skupine ogljika c2 in c3 Bili so enaki.
Kot v tej sestavi so tudi štiri skupine različne (-cooh, OH, H in druga stran molekule), so ogljikovi asimetrični (ali kirali) in kažejo znamenito optično aktivnost.
Način, kako so skupine razporejene v ogljikih2 in c3 tartarne kisline določa nekatere različne strukture in lastnosti za isto spojino; to pomeni, da omogoča obstoj stereoizomerov.
Uporaba tartarne kisline
V živilski industriji
Uporablja se kot stabilizator Eulsion v pekarnah. Uporablja se tudi kot sestavina za kvas, marmelado, želatino in brezalkoholne pijače. Prav tako izpolnjuje funkcije kot zakisljivega, knjižnice in ponudnika iona.
Lahko vam služi: natrijev bromid (NABR)Tartarična kislina najdemo v teh živilih: sladki piškotki, bomboni, čokolade, plinske tekočine, pekarne in vina.
V izdelavi vin se uporablja za bolj uravnoteženo z gnusnega vidika z zmanjšanjem pH le -teh teh.
V farmacevtski industriji
Uporablja se pri ustvarjanju tablet, antibiotikov in šumečih tablet, pa tudi pri zdravilih, ki se uporabljajo pri zdravljenju srčnih bolezni.
V kemični industriji
Uporablja se tudi pri fotografiji, pa tudi v galvanotehniki in je idealen antioksidant za industrijske maščobe.
Uporablja se tudi kot ugrabitelj kovinskih ionov. Kot? Njihove povezave vrnejo tako, da lahko okoli teh pozitivno obremenjenih vrst najdete atome kisika karbonilne skupine, bogate z elektroni.
V gradbeništvu
Odlašajte postopek utrjevanja ometa, cementa in omet, s čimer je manipulacija teh materialov učinkovitejša.
Lastnosti tartarne kisline

Najpogostejše aplikacije iz tartarne kisline so:
- Tartarična kislina se trži v obliki kristalnega prahu ali rahlo neprozornih belih kristalov. Ima prijeten okus in ta lastnost kaže na kakovostno vino.
- Stopi pri 206 ° C in gori pri 210 ° C. Je zelo topen v vodi, alkoholih, osnovnih rešitvah in boraksu.
- Njegova gostota je 1,79 g/ml pri 18 ° C in predstavlja dve konstanti kislosti: PKA1 in PKA2. To pomeni, da ima vsak od obeh kislinskih protonov svojo nagnjenost, da se osvobodi v vodnem okolju.
- Kot imata skupine za stroje in OH, jo lahko analiziramo z infrardečo spektroskopijo (IR) za njihovo kvalitativno in kvantitativno določitev.
- Druge tehnike, kot so masna spektroskopija in jedrska magnetna resonanca, omogočajo prejšnjo analizo te spojine.
Stereokemija

Tartarska kislina je bila prva organska spojina, na katero je bila razvita enantiomerna ločljivost. Kaj to pomeni? To pomeni, da bi lahko njene stereoizomere ročno ločili zahvaljujoč raziskovalnemu delu biokemista Louisa Pasterja leta 1848.
In kakšni so stereoizomeri iz tartarne kisline? To so: (r, r), (s, s) in (r, s). R in S sta prostorske konfiguracije ogljika C2 in c3.
Tartarična kislina (R, R), najbolj "naravna", vrti polarizirano svetlobo v desno; Tartarne kisline (S, S) je pokvarjeno na levi strani, v nasprotju z iglami. In končno, tartarska kislina (R, S) ne zlomi polarizirane svetlobe, saj je optično neaktivna.
Louis Pasteur je s pomočjo mikroskopa in pincete našel in ločeval kristale iz tartarne kisline, ki so pokazali "desno" in "levo" vzorce, na primer na vrhunski sliki.
Na ta način so kristali z desnimi desnimi tistimi, ki jih tvori enantiomer (R, R), medtem ko so kristali "levi -sprejeti" enantiomer (S, S).
Vendar pa se kristali višine tartarične kisline (R, S) ne razlikujejo od drugih, saj imajo hkrati usposobljene in leve značilnosti; Zato jih ni bilo mogoče "rešiti".
Reference
- Wikipedija. (2018). Tartarična kislina. Pridobljeno iz.Wikipedija.org
- Pubchem. (2018). Tartarična kislina. Okrevano od PubChema.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Razumevanje vinskih tartatov. Okreval od Jordanwinery.com
- Aktivno. Tartarična kislina. Okrevano od Actipedije.org
- Pochteca. Tartarična kislina. Pochteca si je opomogla.com.mx
- Dhaneshwar Singh et al. (2012). O izvoru optične neaktivnosti mezo-tortarne kisline. Oddelek za kemijo, Univerza Manipur, Canchipur, Imphal, Indija. J. Kem. Očestva. Govedina., 4 (2): 1123-1129.

