Anomerični ogljik, kar je, značilnosti, primeri
- 3220
- 699
- Mr. Shane Larkin
On Anomerni ogljik To je stereocentro prisoten v cikličnih strukturah ogljikovih hidratov (mono ali polisaharidi)). Ker je stereocentro, natančneje epimerus, izhaja iz njega dva diastereoizomera, označena z α in β črkami; To so anomeri in so del obsežne nomenklature v svetu sladkorjev.
Vsak anomer, α ali β, se razlikuje v položaju OH skupine ANómerico Carbon glede na obroč; Toda v obeh je anomerni ogljik enak in se nahaja na istem mestu molekule. Anomeri so ciklični hemiacetali, produkt intramolekularne reakcije v odprti verigi sladkorjev; biti aldose (aldehidos) ali ketosas (ketoni).
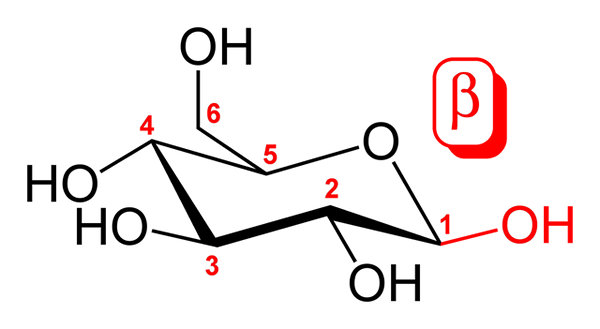
 Konformacija stola za β-D-glukopiranozo. Vir: Commons Wikimedia.
Konformacija stola za β-D-glukopiranozo. Vir: Commons Wikimedia. Zgornja slika prikazuje konformacijo stola za β-D-glukopiranozo. Kot je razvidno, je sestavljen iz šesterodnega obroča, vključno z atomom kisika med ogljikovimi 5 in 1; Slednji ali bolje rečeno prvi, je Anómerico Carbon, ki tvori dve preprosti vezi z dvema atoma kisika.
Če ga podrobno opazimo, je OH Carbon 1 skupina 1 usmerjena nad šestkotnim obročem, pa tudi CH Group2Oh (ogljik 6). To je β anomer. Α anomer bi se na drugi strani razlikoval le v tej skupini OH, ki bi bila nameščena po obroču, kot da bi bila Transtereoisomer.
Hemiacetals
V konceptu hemiacetal je treba še malo poglobiti, da bi bolje razumeli in razlikovali anomerni ogljik. Hemiacetali so produkt kemijske reakcije med alkoholom in aldehidom (aldose) ali ketonom (ketosas).
Ta reakcija je lahko predstavljena z naslednjo splošno kemijsko enačbo:
Vam lahko služi: polivinilpirrolidon: struktura, lastnosti, uporabe, neželeni učinkiRoh + r'cho => roch (oh) r '
Kot je razvidno, alkohol reagira z aldehidom, da tvori hemiacetal. Kaj bi se zgodilo, če bi tako R kot R 'pripadata isti verigi? V tem primeru bi obstajala ciklična hemiacetal in edini možen način, da ga je mogoče oblikovati.
Poleg tega mora biti struktura sestavljena iz prožne verige in s sposobnimi povezavami, da olajšajo nukleofilni napad OH proti karbonilnemu ogljiku skupine Cho. Ko se to zgodi, se struktura zapre v pet ali šest članov.
Ciklični hemiacetal
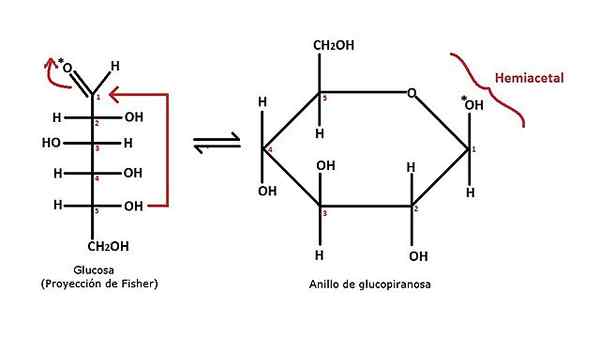 Ciklična tvorba hemiacetala. Vir: Alejandro Porto [CC BY-SA 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)]
Ciklična tvorba hemiacetala. Vir: Alejandro Porto [CC BY-SA 3.0 (https: // creativeCommons.Org/licence/by-sa/3.0)] Na zgornji sliki je prikazan primer tvorbe cikličnega hemiacetala za glukozni monosaharid. To je mogoče videti iz aldoze s skupino Aldehid Cho (Carbon 1). To napade OH skupina ogljika 5, kot kaže rdeča puščica.
Struktura sega od odprte verige (glukoze), do piranskega obroča (glukopofarous). Sprva med to reakcijo in novo razloženo za hemiacetal ni povezave; Če pa je obroč skrbno opažen, zlasti v oddelku C5-O-c1(OH) -C2, Cenimo, da to ustreza pričakovanemu okostja za hemiacetal.
Carbons 5 in 2 predstavljata r in r 'splošne enačbe. Ker so to del iste strukture, je potem ciklični hemiacetal (in obroč je dovolj, da je razviden).
Značilnosti anomernega ogljika in kako ga prepoznati
Kje je anomerni ogljik? V glukozi je to skupina CHO, ki lahko trpi nukleofilni napad OH bodisi spodaj ali zgoraj. Glede na orientacijo napada se oblikujeta dva različna anomera: α in β, kot že omenjeno.
Lahko vam služi: kemični pojavi: značilnosti in primeriZato je prva značilnost, ki jo ima ta ogljik, ta, da je v odprti verigi sladkorja tisti, ki trpi nukleofilni napad; Se pravi, da je skupina CHO za Aldos ali R skupino2C = O, za ketuse. Ko pa se nastaja ciklični hemiacetal ali obroč, lahko ta ogljik daje vtis, da je izginil.
Tu je, kjer obstajajo še druge posebne lastnosti, ki jih lahko najdete v katerem koli piranoso ali furanusnem obroču vsakega ogljikovega hidrata:
-Anomerni ogljik je vedno v desni ali levi od atoma kisika, ki tvori obroč.
-Še pomembneje je, da je to povezano ne samo s tem atomom kisika, ampak tudi s skupino OH, iz Cho ali R2C = O.
-Je asimetričen, torej ima štiri različne substituente.
S temi štirimi značilnostmi je enostavno prepoznati anomerni ogljik, ki opazuje katero koli "sladko strukturo".
Primeri
Primer 1
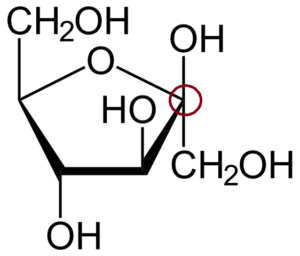 β-d-fructofuranosa. Vir: Neurotoger (pogovor • prispevki) [javna domena]
β-d-fructofuranosa. Vir: Neurotoger (pogovor • prispevki) [javna domena] Gor.
Če želite prepoznati anomerni ogljik, morate najprej opazovati ogljikove ogljike na levi in desni strani atoma kisika, ki tvori obroč. Potem je tisti, ki je povezan s skupino OH, anomerni ogljik; da je v tem primeru že zaklenjen v rdečem krogu.
To je β anomer, ker je OH anomernega ogljika nad obročem, tako kot čip2Oh.
Primer 2
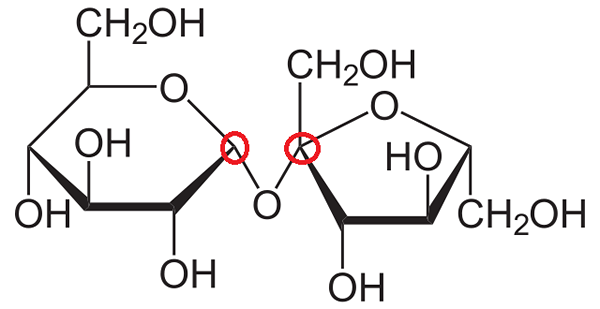 Saharoza. Vir: Neurotoger prek Wikipedije.
Saharoza. Vir: Neurotoger prek Wikipedije. Zdaj je poskušen razložiti, kaj so anomerni ogljikovi v strukturi saharoze. Kot je razvidno, ga sestavljata dva monosaharida, ki sta kovalentno povezana z glikozidno vez, -o-.
Vam lahko služi: natrijev permanganat (NAMNO4): Lastnosti, tveganjaDesni obroč je popolnoma enak na novo komentirano: β-d-fructofuranosa, le da je "obrnjen" na levo. Anomerni ogljik ostaja enak za prejšnji primer in izpolnjuje vse značilnosti, ki bi jih od njega pričakovali.
Po drugi strani je obroč na levi strani α-D-glukopiranoza.
Ponavljanje istega postopka prepoznavanja anomernega ogljika, ki gledata dva ogljika na levi in desni strani kisika, ugotovimo, da je desni ogljik povezan s skupino OH; ki sodeluje v glukozidni vezi.
Zato sta oba anomerna ogljika povezana z -O-, zato sta zaklenjena v rdeče kroge.
Primer 3
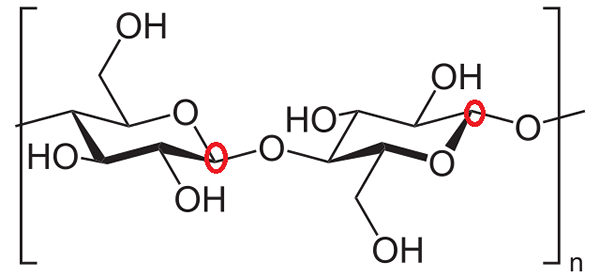 Celuloza. Vir: Neurotoger [javna domena]
Celuloza. Vir: Neurotoger [javna domena] Končno je predlagano prepoznati anomerne ogljikove enote dveh glukoznih enot v celulozi. Ponovno opazimo karbone okoli kisika znotraj obroča in ugotovimo, da v glukoznem obroču na levi strani anomerni ogljik sodeluje v glukozidni vezi (zaklenjen v rdeči krog).
V obroču glukoze na desni strani pa je anomični ogljik desno od kisika in ga je enostavno prepoznati, ker je povezan s kisikom glukozidne vezi. Tako sta oba anomerna ogljika v celoti prepoznana.
Reference
- Morrison, r. T. in Boyd, r, n. (1987). Organska kemija. 5ta Izdaja. Uredništvo Addison-Wesley Interamerican.
- Carey f. (2008). Organska kemija. (Šesta izdaja). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Organska kemija. Amine. (10th Izdaja.). Wiley Plus.
- Rendina g. (1974). Uporabne biokemijske tehnike. Interamerican, Mehika.
- Chang s. (s.F.). Vodnik po anomernem ogljiku: kaj je anomerni ogljik? [PDF]. Okrevano od: kem.UCLA.Edu
- Gunawardena G. (13. marec 2018). Anomerika premoga. Kemija librettexts. Okrevano od: kem.Librettexts.org
- Foist l. (2019). Anomerni ogljik: definicija in pregled. Študij. Okrevano od: študij.com

