Butanonska struktura, lastnosti in uporabe
- 3156
- 733
- Ricky Dach
The Butanon Gre za organsko spojino, zlasti keton, katerega kemijska formula je CHO3Pogl2Coch3. Njegov videz je brezbarvna tekočina, ki se v bistvu uporablja kot topilo. Ima podobno lastnosti acetona, vendar zavre pri višji temperaturi in počasneje izhlapi.
Proizvaja ga katalitična dehidrogenacija 2-butanola (kiralna spojina). Vendar je v naravnem stanju v sestavi nekaterih sadov. Je del izpušnih cevi vozil in je sestavni del dima tobaka.
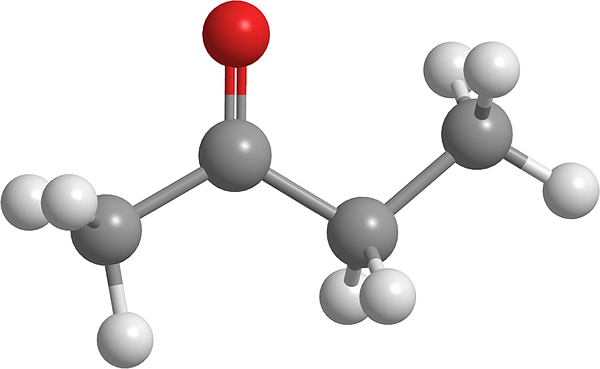
 Butanonska molekula. Vir: Pixabay.
Butanonska molekula. Vir: Pixabay. Po acetonu je najpreprostejši od te družine organskih spojin. Butnonone povzroča draženje v očeh in nosu. V nenavadno visokem odmerku lahko povzroči draženje pljučne sluznice. Po drugi strani se ta tekočina šteje za predhodnika narkotikov.
Butanone ima veliko topnost v vodi; Je pa tudi zelo topen v organskih topilih, kot so etanol, eter, aceton, benzen in kloroform. To je mogoče razložiti, ker je njegova vrednost p log (0,29) za koeficient predelne particije oktana/vode nizka.
[TOC]
Butanonska struktura
Na zgornji sliki je molekula butanona prikazana z modelom sfer in palic. Atom kisika karbonilne skupine (rdeča krogla) je mogoče videti v drugem ogljiku. Ta skupina, C = O, je odgovorna za podelitev trajnega dipolnega trenutka za molekulo.
Butanon, strukturno pogled, ni nič drugega kot aceton, ki mu je bila dodana metilenska skupina, ch2. Če ima več ogljikov, je dipolski trenutek manjši v primerjavi z acetonom; Toda njegova največja molekularna masa povzroči, da zavre pri višji temperaturi.
Ta molekula, tako kot drugi ketoni, nima možnosti oblikovanja vodikovih mostov; In zato njihove interakcije dipol-dipolo niso tako močne.
Vam lahko služi: emulzifikator: postopek emulzije, molekularni vidiki, aplikacijeZato je nestanovitna tekočina. Ko temperatura pade (-86,6 ° C), so njeni šibki dipoli tisti, ki vodijo njihove molekule, da tvorijo kristal. Poleg tega je mogoče komentirati tudi, da je butanon strukturno asimetričen.
Lastnosti
Molekularna formula
C4H8Ali pogl3Coch2Pogl3
Imena
- Butanon.
- 2-butanon.
- Butan -2 -na.
- Metil etil Cetona.
Molarna masa
72,107 g/mol.
Fizični opis
Brezbarvna tekočina.
Vonj
Dišeče do mete, zmerno močan.
Vrelišče
79,59 ° C pri 760 mmHg.
Tališče
-86.6 ° C.
točka vžiga
-9 ° C (zaprta skodelica).
Topnost vode
29 g /100 ml pri 20 ° C. Medtem ko je njegov dipolni trenutek manjši od trenutka acetona, lahko še vedno v odlični meri deluje z molekulami vode. Od njih prejme vodikove mostove: (ch3) (Pogl2Pogl3) C = o-hah. Zaradi tega je v vodi zelo topno.
Topnost v organskih topilih
Topno v benzenu, alkoholu in etru; Metano z olji, etanolom, etrom, acetonom, benzenom in kloroformom. Upoštevajte, da je butanon topen v najrazličnejših topilih.
Gostota
0,7997 g/cm3 pri 25 ° C.
Gostota hlapov
2,41 (glede na vodo = 1).
Parni tlak
90,6 mmHg pri 25 ° C.
Koeficient oktanola/vode
Dnevnik p = 0,29
Temperatura samoificiranja
505 ° C.
Razgradnja
Razpade s fotokemičnimi procesi z oksidacijo z brezplačnim hidroksilnim radikalom. Ko se ogreva na razgradnjo, oddaja akrov.
Goo
0,40 cpoise pri 25 ° C.
Toplota zgorevanja
2.444,1 kJ/mol pri 25 ° C.
Toplota za uparjanje
31.30 kJ/mol na vrelišču; in 34,79 kJ/mol pri 25 ° C.
Vam lahko služi: splošni zakon o plinuPovršinska napetost
23,97 mn/m a 25 ° C.
Ionizacijski potencial
0,54 eV.
Prag vonja
Nizek vonj: 0,735 mg/m3.
Visok vonj: 147,5 mg/m3.
Lomni količnik
1.788 do 20 ° C.
Konstanta disociacije
PKA = 14,70.
Stabilnost
Stabilen, a zelo vnetljiv. Nezdružljivo z oksidacijskimi sredstvi, bazami in močnimi zmanjšanimi sredstvi. Izogibati se je treba vlagi.
Prijave
Topilo
Butanon se uporablja kot topilo pri izdelavi površinskih premazov, izdelave brezdiumnega prahu, obarvane obarvane smole in pri odpravljanju kopičenja maščob, ki jih proizvajajo maziva.
Poleg tega se uporablja pri izdelavi:
- Umetno usnje.
- Gomas.
- Lacas.
- Laki.
- Lepilo.
- Topila.
- Barvne vložke.
- Lepila.
- Plastični cementi.
- Tesnila.
- Magnetni trakovi.
- Prozoren papir.
- Tiskana črnila.
- Kozmetika in farmacevtski izdelki.
Uporablja se tudi kot topilo za odmrzovanje kovinskih površin, čistil za elektronsko opremo in ekstrakcijo maščob. Služi za pridobivanje trdega lesa in rastlinsko olje.
Je inertna sestavina pri izdelavi pesticidov in pri izdelavi acetata in celuloznega nitrata.
Uporablja se kot ekstrakcijsko topilo pri predelavi hrane in sestavinah hrane; Na primer pri frakcioniranju maščob in olj, pa tudi v postopku kave iz kofeina. Uporablja se tudi kot topilo v markerjih, ki se uporabljajo v belih deskah.
Reagent
- Butanone se uporablja kot fotoiniciator v vodi topni.
- Kondenzira se s formaldehidom, da proizvaja izopropenil keton.
- Izkušnje z avtokodenzacijo za proizvodnjo etil amilo cetona.
- Reagira s citralom, da dobimo parfumske komponente, kot je metilpseudoon.
Vam lahko služi: reakcijska toplota- Vmešava kot katalizator pri proizvodnji hidraccina.
- Poleg tega je predhodnik metil etil cetonskega peroksida, ki je katalizator za nekatere reakcije polimerizacije.
Plastični cement
Butanone ima kot plastično varilno sredstvo, z uporabo pri sklopu modelov polistirena. Butnonone raztopi polistiren, kar omogoča, da se robovi pridružijo, ko se pojavi nova polimerizacija. To vedenje je cement in ne lepila.
Druge uporabe
Butanon se uporablja kot sterilizator bakterijskih spor v kirurških instrumentih, iglah, hipodermalnih injektorjih in zobnih instrumentih.
Uporablja se kot aromatično sredstvo hrane v zelo nizkih koncentracijah; Na primer, pri alkoholnih pijačah je koncentracija 20 ppm; v pečenih izdelkih, 12,7 ppm; Meso ima približno 26,5 ppm; žvečilna guma, 0,63 ppm; in v maščobah in oljih 1,0 ppm.
In končno se butanon uporablja pri ločitvi apoproteina hemoproteina v hemoproteinih.
Reference
- Morrison, r. T. in Boyd, r, n. (1987). Organska kemija. 5ta Izdaja. Uredništvo Addison-Wesley Interamerican.
- Carey f. (2008). Organska kemija. (Šesta izdaja). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Organska kemija. Amine. (10thIzdaja.). Wiley Plus.
- Nacionalni center za informacije o biotehnologiji. (2019). Baza podatkov metil etil ketona pubchem. Cid = 6569. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Wikipedija. (2019). Butanon. Pridobljeno iz: v.Wikipedija.org
- Royal Society of Chemistry. (2015). Butanon. Chemspider. Okreval od: chemspider.com
- Arlem Cheprasov. (2019). Kaj je butanon? Formula in uporaba. Študij. Okrevano od: študij.com
- Ben Verve. (17. maj 2017). Butanon. Kemijski svet. Okrevano od: ChemistryWorld.com

