Zgodovina Bromo, struktura, elektronska konfiguracija, lastnosti, uporabe

- 2223
- 551
- Ignacio Barrows
On Bromin Gre za nemetalni element, ki spada v skupino halogenov, skupina 17 (VIIA) periodične tabele. Njen kemični simbol je BR. Predstavljena je kot diatomska molekula, katere atome združuje kovalentna vez, zato je dodeljena molekularna formula2.
Za razliko od fluorida in klora, broma v kopenskih pogojih ni plin, ampak rdečkasto rjava tekočina (spodnja slika). Kadi in skupaj z živo srebrom, edinimi tekočimi elementi. Pod njim se jod, čeprav se njegova barva stopnjeva in postane vijolična, lahko kristalizira v hlapni snovi.
 Viala s čistim tekočim bromom. Vir: Hi-res slike kemičnih elementov [cc do 3.0 (https: // creativeCommons.Org/licence/by/3.0)]
Viala s čistim tekočim bromom. Vir: Hi-res slike kemičnih elementov [cc do 3.0 (https: // creativeCommons.Org/licence/by/3.0)] Bromo je leta 1825 odkril Carl Löwig, ki je študiral pod vodstvom nemškega kemika Leopolda Gmelina; In leta 1826 francoski kemik Antoine-Jerome Ballard. Vendar je bila objava eksperimentalnih rezultatov Balarda pred izdajo Löwiga.
Bromo je 62. najpogostejši element na Zemlji, ki ga v nizkih koncentracijah porazdeli zemeljska skorja. V morju je povprečna koncentracija 65 ppm. Človeško telo vsebuje 0,0004 % broma in ne dokončno pozna njegovo funkcijo.
Ta element se komercialno izkorišča v salmuelasu ali krajih, ki so po posebnih pogojih visoke soli; Na primer, Mrtvo morje, na katerega se zbližajo vode sosednjih ozemelj.
To je jedki element, ki lahko napada kovine, kot sta platina in paladij. Raztopljen v vodi, brom lahko tudi korozivno deluje na človeška tkiva, kar poslabša situacijo, ker je mogoče ustvariti bromhirično kislino. Glede svoje strupenosti lahko povzroči pomembno škodo organom, kot so jetra, ledvice, pljuča in želodec.
Brom je v atmosferi zelo škodljiv, saj je 40-100-krat bolj uničujoč za ozonsko plast kot klor. Polovica izgube ozonske plasti na Antarktiki nastane z reakcijami, povezanimi z bromometilom, spojino, ki se uporablja kot fumigant.
Ima številne uporabe, kot so: zaostalilnik za požar, belilno sredstvo, površinsko razkužilo, dodatek za gorivo, posrednik v sedativni proizvodnji, pri proizvodnji organskih kemikalij itd.
[TOC]
Zgodovina
Carl Löwig Work
Bromo je leta 1825, nemški kemik, odkril samostojno in skoraj istočasno, leta 1825 in Antoine Balard, francoski kemik leta 1826.
Carl Löwig, učenec nemškega kemika Leopold Gmelin, je zbral vodo iz vzmeti Bad Kreuznacha in dodal klor; Po dodajanju etra je mešal mešanico tekočin.
Nato je eter ločil z destilacijo in ga koncentriral z izhlapevanjem. Kot rezultat tega je dobil rdečkasto rjavo snov, ki je bila bromin.
Antoine Balard deluje
Balard je na drugi strani uporabljal pepel rjave alge. Tako se je Bromo sprostil, klor je šel skozi vodni material, ki je bil podvržen ekstrakciji, v katerem je bil prisoten magnezijev bromid, MGBR2.
Nato smo material destilirali v prisotnosti manganovega dioksida in žveplove kisline, kar je povzročilo rdeče hlape, ki so se kondenzirale v temno tekočino. Balard je menil, da gre za nov element in ga je imenoval Muride, izhaja iz latinske besede muria, s katero je bila imenovana slanica.
Lahko vam služi: živa snov: koncept, značilnosti in primeriPoudarjeno je, da je Balard s predlogom Angglade ali Gay-Lussac spremenil ime Muride v Brôme, ki temelji na dejstvu, da Brôme pomeni pestilent, ki definira vonj odkritega elementa.
Rezultate je objavil Belard v Annales of Chemie in Physique, preden je Löwig objavil svoje.
Šele od leta 1858 je bil bromin proizveden v pomembnih količinah; leto, v katerem so bile odkrite in izkoriščanje nahajališč soli, pri čemer pridobivanje broma.
Elektronska struktura in konfiguracija Bromo
Molekula
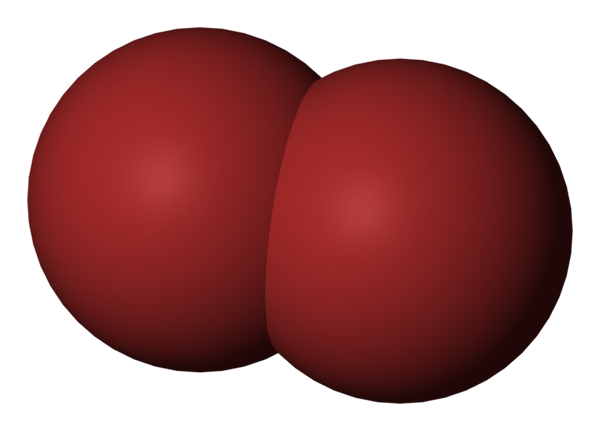 BR2 molekula. Vir: Benjah-BMM27 [javna domena].
BR2 molekula. Vir: Benjah-BMM27 [javna domena]. Na zgornji sliki je prikazana molekula broma, BR2, S kompaktnim modelom polnjenja. Pravzaprav obstaja preprosta kovalentna vez med dvema atomima broma, BR-BR.
Ker je diatomična in homogena molekula, primanjkuje stalnega dipolnega trenutka in lahko prek londonskih disperzijskih sil komunicira le z drugimi istega tipa.
To je razlog, zakaj vaša rdečkasto tekočino kadi; V BR molekulah2, Medtem ko so razmeroma težke, jih njihove medmolekularne sile šibko povežejo.
Bromo je manj elektronegativen kot klor, zato vpliva na nižji učinek privlačnosti na elektrone plasti Valencije. Kot rezultat tega je potrebno manj energije za prehod z višjo raven energije, absorbirajo zelene fotone in odražajo rdečkasto barvo.
Kristali
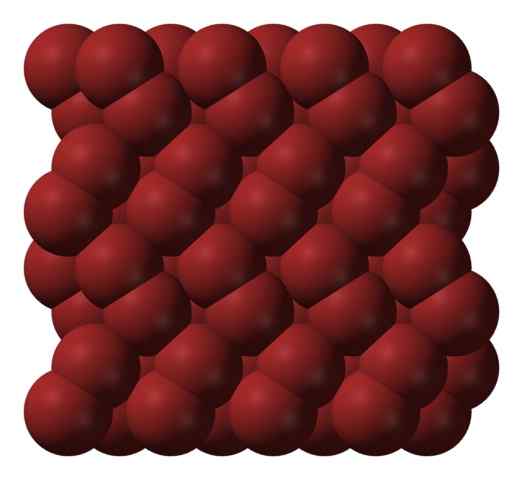 Kristalna struktura Bromo. Vir: Ben Mills [javna domena].
Kristalna struktura Bromo. Vir: Ben Mills [javna domena]. V plinski fazi so molekule BR2 Se precej ločijo, dokler med njimi obstajajo učinkovite interakcije. Vendar pa lahko pod svojim talilnim točkam zamrznete v rdečkasto ortorambičnih kristalih (nadrejena slika).
Upoštevajte, kako BR molekule2 Postavljeni so urejeni tako, da se zdijo "brominski črvi". Tukaj in pri teh temperaturah (t < -7,2°C), las fuerzas de dispersión son suficientes para que las vibraciones de las moléculas no desmoronen el cristal en el acto; pero aún así, varias de ellas sublimarán constantemente.
Stanja plasti in oksidacije Valencia
Konfiguracija elektronske broma je:
[AR] 3D104s2 4p5
Biti 3D104s2 4p5 njegova valenčna plast (čeprav 3D orbital10 Nimajo pomembnosti v svojih kemičnih reakcijah). Elektroni orbitalov 4S in 4P so najbolj zunanji in dodajo skupno 7, le en elektron za dokončanje okteta Valencije.
Iz te konfiguracije lahko možno oksidacijsko stanja sklepamo za bromin: -1, če je dobiček elektronov izolektronski do Kriptona; +1, biti kot 3D104s2 4p4; +3, +4 in +5, izguba vseh elektronov 4P orbitala ([AR] 3D104s24p0); in +7, ki teče brez elektronov v orbitalu 4S ([AR] 3D104s04p0).
Lastnosti
Fizični videz
Majhna temno rjava rdečkasta tekočina. V naravi ga najdemo kot diatomska molekula, atomi pa jih združujejo kovalentna vez. Bromo je gostejša tekočina kot voda in se potopi vanj.
Vam lahko služi: radio: struktura, lastnosti, uporabe, pridobivanjeAtomska teža
79.904 g/mol.
Atomska številka
35.
Vonj
Acre dim, zadušljiv in draži.
Tališče
-7.2 ° C.
Vrelišče
58,8 ° C.
Gostota (Br2) tekočina
3.1028 g/cm3
Topnost vode
33,6 g/l a 25 ° C. Topnost broma v vodi je nizka in se ponavadi povečuje z zniževanjem temperature; vedenje, podobno drugim plinom.
Topnost
Prosto topno v alkoholu, etru, kloroformu, ogljikovem tetrakloridu, ogljikovem disulfidu in koncentrirani klorovodiki. Topno v ne -polarnih topilih in nekaterih polarnih, kot so alkohol, žveplova kislina in v mnogih halogeniranih topilih.
Trojna točka
265,9 K pri 5,8 kPa.
Kritična točka
588 K pri 10,34 MPA.
Fusion Heat (Br2)
10,571 kJ/mol.
Toplota za uparjanje (Br2)
29,96 kJ/mol.
Molarna kalorična sposobnost (Br2)
75,69 kJ/mol.
Parni tlak
Pri temperaturi 270 K, 10 kPa.
Temperatura samoificiranja
Ni vnetljivo.
točka vžiga
113 ° C.
Temperatura skladišča
2 do 8 ° C.
Površinska napetost
40,9 mn/m a 25 ° C.
Prag vonja
0,05 - 3,5 ppm. 0,39 mg/m3
Indeks loma (ηD)
1.6083 do 20 ° C in 1.6478 do 25 ° C.
Elektronegativnost
2.96 na lestvici Pauling.
Ionizacijska energija
- Prva stopnja: 1.139,9 kJ/mol.
- Druga stopnja: 2.103 kJ/mol.
- Tretja stopnja: 3.470 kJ/mol.
Atomski radio
120 popoldne.
Radijski kovalent
120.3 PM.
Van der Waals radio
185 popoldne.
Reaktivnost
Je manj reaktiven kot klor, vendar bolj reaktiven kot jod. Je oksidant, ki je manj močan od klora in močnejši od joda. Je tudi šibkejši redukcijski sredstvo kot jod, vendar močnejši od klora.
Klorska para je zelo jedska za številne materiale in človeška tkiva. Napada številne kovinske elemente, vključno s platino in paladijem; Vendar ne napada svinca, niklja, magnezija, železa, cinka in manj kot na natrij.
Bromo v vodi doživi spremembo in se spremeni v bromid. Obstaja lahko tudi kot bromat (bratec3-), Odvisno od tekočega pH.
Brom lahko zaradi svojega oksidacijskega delovanja sproži sproščanje radikalov brez kisika. To so močni oksidanti in lahko povzročijo poškodbe tkiv. Prav tako lahko bromin povzroči spontano vžig v kombinaciji s kalijem, fosforjem ali kositrom.
Prijave
Aditiv bencina
Etilen dibromid smo uporabili za odpravo možnih nahajališč svinca v motorjih avtomobilov. Po zgorevanju bencina, ki je svinca uporabljal kot aditiv, se je brom v kombinaciji s svincem, da tvori svinčev bromid, hlapni plin, ki ga je izpustila izpušna cev.
Medtem ko je bromin odpravil vodstvo iz bencina, je bilo njegovo destruktivno delovanje na ozonski plasti zelo močno, zato je bilo za to aplikacijo zavrženo.
Pesticidi
Metilen ali bromometil bromid smo uporabili kot pesticid za čiščenje tal, zlasti za odpravo parazitskih ogorčic, kot je AnyLostome.
Vendar je bila uporaba večine spojin, ki vsebujejo bromin.
Nadzor nad izdajo živega srebra
BROMO se uporablja v nekaterih rastlinah za zmanjšanje emisij živega srebra, zelo strupene kovine.
Vam lahko služi: gravimetrija: gravimetrična analiza, metode, uporabe in primeriFotografija
Srebrni bromid se poleg srebrnega joduroja in srebrnega klorida uporablja kot svetlobna spojina v fotografskih emulzijah.
Terapevtska dejanja
Kalijev bromid, pa tudi litijev bromid, so bili v 19. stoletju in začetku dvajsetega stoletja uporabljeni kot splošni sedativi. Preproste soli se še vedno uporabljajo v nekaterih državah, kot so antikonvulzije.
Vendar pa FDA ZDA ne odobri uporabe broma za zdravljenje katere koli bolezni.
Ogenj zaostalega
Brom se plameni preoblikujejo v bromhorovo kislino, kar moti reakcijo oksidacije, ki se pojavi med požarom, in ustvari njegovo izumrtje. Polimeri vsebujejo bromin za izdelavo zaostalih smol za zaostale.
Aditiv za hrano
Za izboljšanje kuhanja so dodane sledi kalijevega bromata do moke.
Kemični reagenti in posrednik
Vodikov bromid se uporablja kot reducirajoče sredstvo in katalizator za organske reakcije. Bromo se uporablja kot kemični posrednik pri proizvodnji zdravil, hidravličnih tekočin, hladilnih sredstev, dehumidifikatorjev in pripravkov za valovito las.
Ugotavlja tudi uporabo pri izdelavi vrtilnih tekočin, izdelkov za razkužitev vode, belkastih sredstev, površinskih razkuživ, barvil, dodatkov za gorivo itd.
Biološko delovanje
Študija, izvedena leta 2014. Vendar pa ni podatkov o posledicah primanjkljaja elementa.
Kje je
Bromo se komercialno izvleče iz solinskih min in globokih vrtin Salmuelas, ki jih najdemo v zvezni državi Arkansas, in v Velikem slanem Utahu, oba v ZDA. Ta zadnja slanica ima 0,5 -odstotno koncentracijo broma.
Za ekstrakcijo broma.
Mrtvo morje, na meji med Jordanijo in Izraelom, je zaprto morje, ki je pod morsko gladino, zaradi česar je zelo visoka koncentracija soli.
Bromo in Potassa se tam komercialno pridobijo z izhlapevanjem vode z visoko soljo Mrtvega morja. V tem morju lahko koncentracija broma doseže 5 g/l.
Najdemo ga tudi v visokih koncentracijah v nekaterih vročih vzmeti. Na primer, bominita je srebrni mineral Bromida, ki ga najdemo v Boliviji in Mehiki.
Tveganja
Brom v tekočem stanju je jedko za človeška tkiva. Toda največja nevarnost za človeka prihaja iz bromonskih hlapov in vdihavanja.
Vdihnite okolje s koncentracijo broma 11-23 mg/m3 Proizvaja hude šoke. Koncentracija 30-60 mg/m3 Je izjemno škodljivo. Medtem je koncentracija 200 mg lahko usodna.
Reference
- Shiver & Atkins. (2008). Anorganska kemija. (Četrta izdaja). MC Graw Hill.
- Nacionalni center za informacije o biotehnologiji. (2019). Bromin. Baza podatkov Pubchem. Cid = 23968. Okrevano od: pubchem.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov
- Ross Rachel. (8. februar 2017). Dejstva o bromu. Okrevano od: Livescience.com
- Wikipedija. (2019). Boraks. Pridobljeno iz: v.Wikipedija.org
- Lentech b. V. (2019). Bromin. Okrevano od: Lentech.com
- « Značilnosti miozina, struktura, vrste in delovanje
- Nuklearne značilnosti, struktura, vrste in funkcije »

