Struktura kalijevega benzoata, lastnosti, pridobivanje, uporabe
- 3737
- 535
- Cary Goyette
On Kalijev benzoat Gre za organsko spojino, ki jo tvori ionski kalij k+ in benzoato c ion6H5COO-. Njegova kemična formula je c6H5Kuhajte ali kondenzirano formulo c7H5Ko2. Je kristalno bela trdna snov. Je higroskopska, kar pomeni, da absorbira zrak iz zraka.
Vodne raztopine kalijevega benzoata so rahlo alkalne. V kislem mediju benzoat ion (c6H5COO-) ponavadi vzame proton in postane benzojska kislina (c6H5COOH).
 Kalijev benzoat6H5Trden kuhar. W. Oelen [cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0)]. Vir: Wikimedia Commons.
Kalijev benzoat6H5Trden kuhar. W. Oelen [cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0)]. Vir: Wikimedia Commons. Kalijev benzoat se uporablja kot konzervans za hrano, še posebej, če so zaželeni, da so brez natrija (NA). Preprečuje, da bi se hrana poslabšala zaradi mikroorganizmov.
Uporablja se v klobasah, predelanih brezalkoholnih pijačah in pekovskih izdelkih, med drugim. Verjetno je njegovo konzervirno delovanje posledica benzojske kisline (c6H5COOH), ki nastane pri nizkem pH, kar preprečuje razmnoževanje gliv in bakterij.
Čeprav zdravstvene organizacije odobrijo kalijev benzoat, je priročno, da ne zlorabljajo njihove uporabe, saj je bilo ugotovljeno, da plodovi miši vplivajo.
[TOC]
Struktura
Kalijev benzoat je organska sol, to je sol karboksilne kisline, saj je kalijeva sol benzojske kisline. Nastane ga K+ kalijev kation in benzoatni anion c6H5COO-.
Benzoato c anion6H5COO- Tvori ga benzenski obroč c6H5- in skupina karboksilata -Coo-.
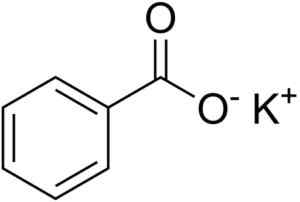 Kemična struktura kalijevega benzoata. Edgar181 [javna domena]. Vir: Wikimedia Commons.
Kemična struktura kalijevega benzoata. Edgar181 [javna domena]. Vir: Wikimedia Commons. Zveza med tema dvema ionoma je močna elektrostatična zveza, ki jih ohranja v kristalni mreži.
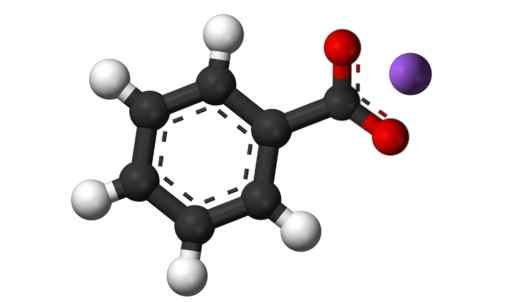
 3D struktura kalijevega benzoata. Črna = ogljik; Bela = vodik; rdeča = kisik; Violet = kalij. Claudio pistilli [cc by-sa (https: // creativeCommons.Org/licence/by-sa/4.0)]. Vir: Wikimedia Commons.
3D struktura kalijevega benzoata. Črna = ogljik; Bela = vodik; rdeča = kisik; Violet = kalij. Claudio pistilli [cc by-sa (https: // creativeCommons.Org/licence/by-sa/4.0)]. Vir: Wikimedia Commons. Nomenklatura
- Kalijev benzoat
- Potona benzojska kislina sol
Lastnosti
Fizično stanje
Kristalno bela trdna trdna snov.
Molekularna teža
160,212 g/mol
Topnost
Topno v vodi.
ph
Vodne raztopine kalijevega benzoata so nekoliko osnovne.
Kemične lastnosti
Je higroskopska, to je trdna snov, ki zlahka absorbira vodo iz okolja.
Zveza med kalijevim k ionom+ in benzoato c ion6H5COO- Kot v večini ionskih spojin ga lahko premaga le z visoko temperaturo ali zelo polarno topilo kot voda.
Vam lahko služi: učinkovita jedrska obremenitevBenzoato c anion6H5COO- Je zmerno osnovna, z občutno težnjo po kombinaciji s protoni. Reagirati z vodo, ki jemlje proton h+ Oblikovati benzojsko kislino (c6H5COOH) in to vodi do povečanja koncentracije OH ionov-.
C6H5COO- + H2Ali ⇔ c6H5COOH + OH-
Zaradi tega so vodne raztopine kalijevega benzoata rahlo alkalne.
Pridobivanje
Za pripravo kalijevega benzoata se benzojska kislina nevtralizira (c6H5Cooh) s kalijevim karbonatom (k2Co3) V minimalni prostornini vode, da dobite prozorno raztopino, iz katere sol kristalizira.
2 c6H5COOH + K2Co3 → 2 c6H5COO-K+ + H2Ali + co2↑
Nato kristalizirano kalijevo benzoatno sol večkrat opramo z etrom in suši.
Prijave
V predelani prehrambeni industriji
Kalijev benzoat se pogosto uporablja kot protimikrobno sredstvo za ohranjanje pijač, derivati sadja, pekarne in druge obroke.
 Nekateri pekarski izdelki lahko vsebujejo kalijev benzoat. Avtor: Andrew Martin. Vir: Pixabay.
Nekateri pekarski izdelki lahko vsebujejo kalijev benzoat. Avtor: Andrew Martin. Vir: Pixabay. Je konzervans za hrano, ki lahko zavira, odloži ali ustavi postopek fermentacije, zakisanja ali poslabšanja hrane zaradi nekaterih gliv in bakterij.
Po podatkih varstva okolja ali agencije EPA (kratica za angleščino Agencija za varstvo okolja) Kalijev benzoat je bil preverjen kot spojina, ki malo skrbi za zdravje ljudi.
Proti glivam
To je antimikotično sredstvo, saj jih lahko uniči tako, da zavira njihovo sposobnost rasti ali razmnoževanja. To ni fungicid za tkiva organizma živali ali ljudi, ampak zaviralec, ki zaostaja ali zavira napredovanje gliv v hrani ali pijači.
Nekatere vrste plesni proizvajajo snovi, imenovane aflatoksini, ki grozijo tako ljudem kot živalim, ker so strupene, lahko proizvajajo raka in mutacije.
Večina kalupov zavira v koncentracijah 0,05-0,10% kalijevega benzoata. Učinkovitost tega je odvisna od pH, saj je manjši pH učinkovitejši kot Antihongos.
Vam lahko služi: kalcijev hidroksid (Ca (OH) 2): struktura, lastnosti, pridobivanje, uporabe Predelane brezalkoholne pijače lahko vsebujejo kalijev benzoat. Avtor: Lisakara. Vir: Pixabay.
Predelane brezalkoholne pijače lahko vsebujejo kalijev benzoat. Avtor: Lisakara. Vir: Pixabay. To je zato, ker je v resnici antimikotično delovanje v benzojski kislini c6H5COOH, ki je konjugirana kislina kalijevega benzoata. Ta kislina se tvori pod pH, torej v prisotnosti velikega števila vodikovih ionov H+:
Kalijev benzoat + vodikovi ioni → benzojska kislina + kalijevi ioni
C6H5Kuhar + h+ → c6H5COOH + K+
Po mnenju nekaterih raziskovalcev je njihova učinkovitost delno posledica topnosti benzojske kisline v celični membrani mikroorganizma. Ta vrsta kisline poveča pretok protonov skozi omenjeno membrano.
To povzroči prekinitev ali neorganizacijo nekaterih funkcij glivične celice.
Proti bakterijam
To je sredstvo, ki deluje proti nekaterim bakterijam. Dodamo ga hrani, kot so predelane klobase, predelane šunke (pripravljene za jesti) in nekaj pijač.
Je bil testiran proti Listeria monocytogenes, bakterija, ki lahko povzroči smrt ljudi, ki zaužije hrano, onesnaženo s tem. Med drugimi simptomi proizvaja vročino, bruhanje in drisko.
Ugotovljeno je bilo, da je hrana, obdelana s kalijevim benzoatom in je bila onesnažena Listeria Vzdrževati jih je treba pri temperaturah pod -2,2 ° C, tako da se takšne bakterije ne reproducirajo.
 Klobase in drugo meso klobas lahko vsebujejo kalijev benzoat. Avtor: Prodaja mojih fotografij z zalog ni dovoljena. Vir: Pixabay.
Klobase in drugo meso klobas lahko vsebujejo kalijev benzoat. Avtor: Prodaja mojih fotografij z zalog ni dovoljena. Vir: Pixabay. Po drugi strani je bila uporaba elektronskega sevanja preizkušena za okrepitev učinka kalijevega benzoata proti bakterijam, vendar je bilo ugotovljeno, da je benzen C proizvajal6H6 ki je strupena spojina.
Torej, tudi če hrana vsebuje kalijev benzoat.
V več aplikacijah
Po mnenju virov, ki so se posvetovali, se kalijev benzoat uporablja tudi pri lepilih in vezavnih sredstvih za različne namene. Doda se cigaretam in tobaku ali je povezan s proizvodnjo le -teh.
Vam lahko služi: Neon: Zgodovina, lastnosti, struktura, tveganja, uporabeUporablja se v izdelkih za osebno nego, kot so kozmetika, šampon, parfumi, mila, losjoni itd. Je tudi del slik in premazov.
Negativni učinki na zaužitje hrane s kalijevim benzoatom
Nekateri raziskovalci so ugotovili, da kalijev benzoat povzroča škodljive učinke na mišice.
Čeprav ni bilo učinkov na odrasle miši, ki so bile izpostavljene kalijevemu benzoatu.
 Po laboratorijskih izkušnjah lahko na mišice vpliva kalijev benzoat, ki ga zaužije mati. Avtor: Tibor Janosi Mozes. Vir: Pixabay.
Po laboratorijskih izkušnjah lahko na mišice vpliva kalijev benzoat, ki ga zaužije mati. Avtor: Tibor Janosi Mozes. Vir: Pixabay. To pomeni, da so plodovi bolj občutljivi na kalijev benzoat kot odrasle miši.
Reference
- Mandal, str.K. et al. (1978). Obnašanje viskoznosti benzojske kisline in benzoatnega iona v vodni raztopini. Journal of Solution Chemistry, Vol. 7, ne. 1, 1978. Povezava je bila obnovljena.Springer.com.
- Rusul, g. in Marth in.H. (1987). Rast in proizvodnja aflatoksina Aspergillus paraziticus NRRL 2999 V pododdelku kalijevega bnezata ali kalijevega sorbata in pri začetnih pH vrednostih. J Hrana pr. 1987; 50 (10): 820–825. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Svetloba. et al. (2005). Inhibitorne učinke soli organske kisline za nadzor Listeria monocytogenes Na Frankfurters. J Hrana pr. 2005; 68 (3): 499-506. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Zhu, m.J. et al. (2005). Vpliv protimikrobnih sestavin in obsevanja na preživetje Listeria monocytogenes in kakovost pripravljene turške šunke. POULT SCI. 2005; 84 (4): 613–20. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Ali.S. Nacionalna knjižnica medicine. (2019). Kalijev benzoat. Okrevano od PubChema.NCBI.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Afshar, m. et al. (2013). Teratogeni učinki Lont izraza poraba kalijevega benzoata na razvoj oči pri miših BALB/C. Iran J Basic Med Sci. 2013; 16 (4): 584–589. NCBI si je opomogel.NLM.ameriški nacionalni inštitut za zdravje.Gov.
- Svinec, d.R. (Urednik) (2003). Priročnik za kemijo in fiziko CRC. 85th CRC Press.
- Morrison, r.T. in Boyd, r.N. (2002). Organska kemija. 6. izdaja. Prentice-Hall.
- « Institucionalne vrednote uprave, za kar so, pomembne
- Magnetni udarni enote, formule, izračun, primeri »

