Koncept najemnine, pogostejši radikali, struktura
- 3441
- 688
- Don Nitzsche
A Najamem To je skupina ali substituent, ki izhaja iz alkana z odpravo enega od njegovih vodikov. Zato je sestavljen iz ogljika in vodika, njegova splošna formula pa je cnH2N+1, namesto cnH2N+2 Za vse neciklične alkane, torej linearne ali razvejane verige.
Najemnina kot skupina simbolizira s črko r. Tako lahko molekularno strukturo številnih organskih spojin posplošimo z uvedbo r. V njih je R le del molekule, povezan s svojim okostjem ali reaktivno funkcionalno skupino.
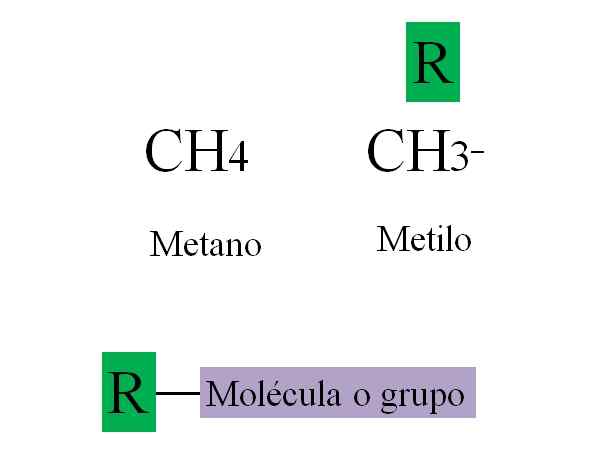 Najemnina. Vir: Gabriel Bolívar.
Najemnina. Vir: Gabriel Bolívar. Vrhunska slika prikazuje zgoraj navedeno. Metano, pogl4, Je alkan, in ko izgubi enega od svojih vodikov, ki se povezuje z molekulo ali skupino, se pretvori v metil, ch3-. Metil ni spojina: ne obstaja kot prosta molekula; Razen če gre za metil radikal, CHO3·, Kar je zelo reaktivno.
Najemnina, simbolizirana z r, tvori kovalentno vez s preostalo molekulo. Tako so alkilične spojine predstavljene kot RG, kjer je G skupina, ki zajema celotno molekulo. Na primer, alkoholi imajo formulo ROH, zato so alkilne spojine.
[TOC]
Nomenklatura
Nomenklatura najemnine nima nobene zveze z dohodkom nepremičnine. To izvira iz iste nomenklature alkana, iz katere izhaja. Na zgornji sliki se na primer metan spremeni v metilno skupino. Tako je dovolj, da zamenjate zaključek -leto, imena alkana, s prekinitvijo -ilo.
Drug primer je iz Etana, Cho3Pogl3. Ko izgubi enega od vodika in je povezana z molekulo ali skupino, se pretvori v etilno skupino, ch3Pogl2-.
Vam lahko služi: Vrsta povezave CO2Na enak način se pojavi pri vseh drugih alkanih, tudi tistih, ki so sestavljeni iz cikličnih verig, kot je cikloheksan.
Radikali pogostejši
Alkind radikali so tisti "ohlapni in reaktivni kosi", ki jih dobimo, ko je r ločen od molekule. Njihove številčnosti so sorazmerne z najetami skupinami, iz katerih izhajajo. Na primer, skupina Metilo, CHO3- In radikalni metil, cho3· So relativno enaki kot običajni.
Na splošno so najpogostejši radikali ali najemne skupine, ki prihajajo iz alkanov, ki vsebujejo manj kot pet ogljikovih atomov. To je nad Pentanom in vsemi njegovimi izomeri.
Ker? Obstajata dva razloga. Prva je, da molekule ogljikovodikov v visokih energetskih razmerah ponavadi trpijo rupture vezi, zato se njihove molekulske velikosti in mase zmanjšajo.
In drugo je, da v naravi obstajajo "izomerne juhe", ki jih je zelo težko očistiti z destilacijo zaradi majhne razlike med njihovimi vrelišči.
Tako je, da so najpogostejši alkijev in njihovi radikali tisti iz kratkih verig, s številnimi atomi ogljika, manjši od šest. Primeri teh alkov so: ch3-, Pogl3Pogl2-, Pogl3Pogl2Pogl2-, Pogl3Pogl2Pogl2Pogl2-, in njegovi možni izomeri.
Struktura
Do zdaj so naslovljeni Alks imeli linearne verižne strukture. Njene strukture, kot je bilo pričakovano, so enake strukturi alkanov tistih, ki nadaljujejo.
Linearne leve bodo povzročile linearne alkimalne skupine. Po drugi strani bodo razvejani vrhovi ustvarili razvejane alkale. Enako se zgodi s cikličnimi alkani.
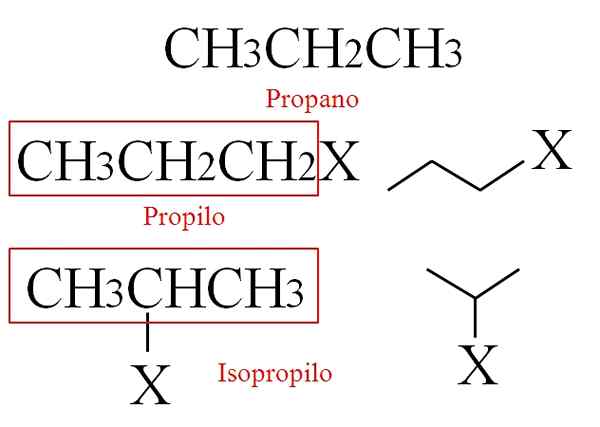
Vam lahko služi: jodometrija: temelje, reakcije, splošni postopek, uporabeVendar lahko linearni alkani povzročijo tudi na videz razvejane alkale, odvisno od tega, kateri od njegovih ogljikovih atomov izgubi vodik. Razmislite o primeru propana:
 Struktura propana in njegove izpeljane alkle skupine. Vir: Gabriel Bolívar.
Struktura propana in njegove izpeljane alkle skupine. Vir: Gabriel Bolívar. Če izgubite vodik iz katerega koli od njegovih primarnih ogljikov, to pomeni, da se tista konca dobijo propilna skupina, ch3Pogl2Pogl2-.
Medtem, če ga vodik izgubi iz svojega sekundarnega ali osrednjega ogljika, dobimo izopropilno skupino (ch3)2Pogl-. Na sliki sta prikazani dve RX spojini, pri čemer sta r propil ali izopropil.
Lastnosti
Najemne skupine običajno ne reagirajo, ker njihovih povezav C-C ali C-H ni enostavno prekiniti. Ne glede na njihovo molekularno strukturo imajo vsi skupno lastnost: hidrofobnost. To pomeni, da ne kažejo naklonjenosti do vode ali kakršnega koli polarnega topila. Vendar to počnejo za maščobe.
Ko je skupina Renta R zelo velika ali ko jih je veliko v molekuli, se njegova hidrofobnost poveča. To je isto, če pravimo, da se njegova lipofilnost povečuje (ljubezen do maščob). Torej, bolj ko je "najeta" molekula, bolj afiniteta bo imela za maščobo, in težje ga bo odstraniti z vodo.
Primeri alkilnih spojin
Izraz "alkilne spojine" je izjemno dvoumni v smislu organske kemije. Skupina ali molekula, ki ji je skupina Rento r vedno dana prednost. In te skupine ali molekule opredeljujejo družine organskih spojin.
Ko pa so te skupine pogostejše pri anorganski kemiji, tako kot pri halogeni in sulfati, je nekaj pomembnosti dati komponenti alkil. Za razjasnitev te točke bomo omenjeni nekaj primerov.
Vam lahko služi: vodik: zgodovina, struktura, lastnosti in uporabeNajemnine
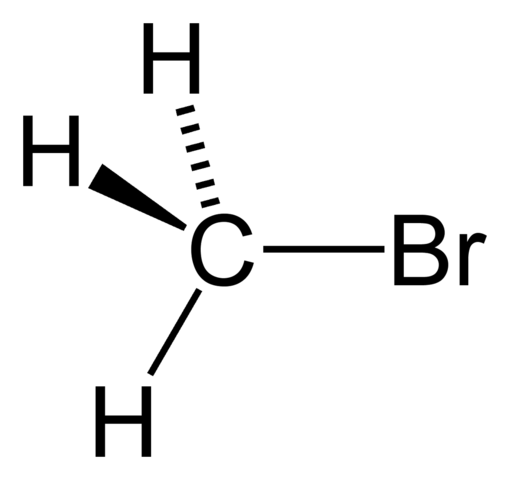 Metil bromid
Metil bromid Rent Haluros ima splošno formulo RX, kjer je X halogenski atom (F, CL, BR in I), in R katero koli skupino ali alkilno zamenjavo. Na primer CHO3Br je metil bromid.
Najem sulfatov
 Dimetil sulfat
Dimetil sulfat Najemni sulfati imajo splošno formulo Roso3R ', kjer sta r in r' dve alkalni skupini, ki sta lahko enaka ali drugačna. Tako imamo dimetil sulfat, cho3Medved3Pogl3 ali jaz2SW4.
Najemnina
Najemni borati imajo splošno formulo (ro3) B. Na primer (CHO3Pogl2Da)3B o (eto)3B se imenuje etil borat.
Triaquilboros
Podobno imamo triaquilboros, katerega splošna formula je r3B. Na primer (CHO3)3B O jaz3B se imenuje Trimethylborano (TMB).
Alkoholi
Alkoholi so tudi alkilične spojine, njihova splošna formula pa je ROH. Vendar ena sama prisotnost skupine OH izgubi pomen za najemne skupine. Alkoholi se ne imenujejo "alkil hidroksidi", ker najemnina kot take niso najbolj temeljni deli njihovih molekul, ampak OH.
Po drugi strani je v prejšnjih primerih poudarek na prisotnosti najetih skupin R; Ker so na računu halogeni, sulfati, boros in boratos zelo.
Reference
- Morrison, r. T. in Boyd, r, n. (1987). Organska kemija. 5. izdaja. Uredništvo Addison-Wesley Interamerican.
- Carey f. (2008). Organska kemija. (Šesta izdaja). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Organska kemija. (10. izdaja.). Wiley Plus.
- Wikipedija. (2020). Alkil. Pridobljeno iz: v.Wikipedija.org
- Danielle Reid. (2020). Alkilna skupina: definicija in pregled. Študij. Okrevano od: študij.com
- Kemija librettexts. (6. aprila 2020). Alkilne skupine. Okrevano od: kem.Librettexts.org
- « Standardi socialnega sobivanja, oblike, pomen, primeri
- Značilnosti voltmeter, delovanje, za kaj je, vrste »

