Alkoholi
- 2049
- 330
- Roman Schamberger
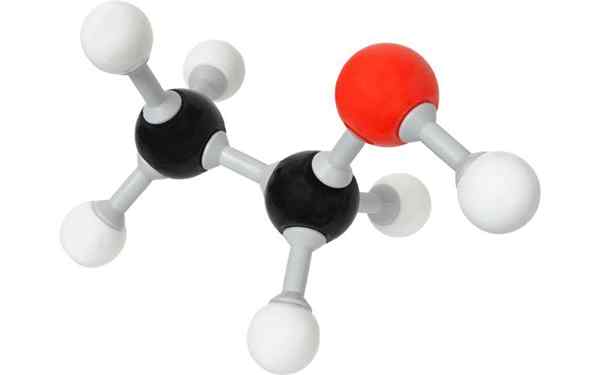
 Molekula etanola ali etilni alkohol. Z licenco
Molekula etanola ali etilni alkohol. Z licenco Kaj so alkoholi?
The Alkoholi So organske spojine, za katere je značilno, da ima hidroksilno skupino (-OH), povezano z nasičenim ogljikom, to je ogljik, ki je povezan s štirimi atomi s preprostimi vezmi (brez dvojnih ali trojnih povezav).
Splošna formula za to obsežno in vsestransko družino spojin je ROH. Če se v strogo kemičnem smislu šteje za alkohol, mora biti skupina OH najbolj reaktivna na molekularno strukturo. To je pomembno, da med več molekulami s skupinami OH potrdimo, katera od njih je alkohol.
Ena od odličnosti alkohola in najbolj znana v popularni kulturi je etilni alkohol ali etanol, CH3Pogl2Oh. Odvisno od njihovega naravnega izvora in s tem njihovega kemičnega okolja lahko njihove mešanice povzročijo neomejen spekter okusov, nekatere, ki celo kažejo pozitivne spremembe v nepcu s potekom let.
Struktura alkohola
Alkoholi imajo splošno formulo ROH. Skupina OH je povezana z R alkilično skupino, katere struktura se razlikuje od enega alkohola do drugega. Zveza med R in OH je preprosta kovalentna povezava, R-OH.
Naslednja slika prikazuje tri generične strukture za alkohole, če upoštevamo, da je atom ogljika nasičen, to je, da tvori štiri preproste povezave.
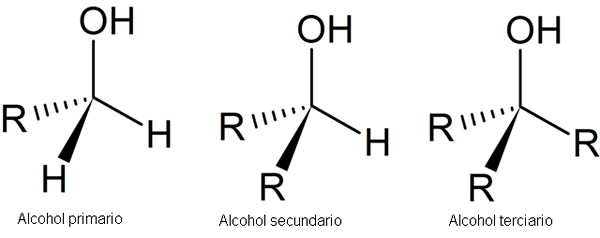 Struktura alkohola. Vir: Secalinum, Wikimedia Commons
Struktura alkohola. Vir: Secalinum, Wikimedia Commons Kot je razvidno, je R lahko katero koli gazirano strukturo, če nima več reaktivnih substituentov kot skupina OH.
V primeru primarnega alkohola je 1. skupina OH povezana s primarnim ogljikom. To je enostavno preveriti z opazovanjem, ali je atom v središču levega tetraedra povezan z R in dvema h.
Drugi sekundarni alkohol je preverjen z ogljikom tetraedra centra, ki je zdaj povezan z dvema R skupinama in h.
In končno imate terciarni alkohol, tretji, z ogljikom, povezanim s tremi skupinami R.
Amfifilski znak
Glede na vrsto ogljika, povezanega z OH, imate razvrstitev primarnih, sekundarnih in terciarnih alkoholov. V tetraedri so bile strukturne razlike med njimi že podrobne. Toda vsi alkoholi, ne glede na njihovo strukturo, delijo nekaj skupnega: lik amfifile.
Ni treba obravnavati strukture, da bi jo opazili, vendar je dovolj s svojo kemijsko formulo ROH. Najemna skupina je skoraj v celoti sestavljena.
Po drugi strani pa lahko skupina OH tvori vodikove mostove z molekulami vode, zato je hidrofilna, torej predstavlja afiniteto do vode. Nato imajo alkoholi hidrofobno okostje, skupaj s hidrofilno skupino. So apolarni in polarni hkrati, kar je isto, kot da gre za amfifile snovi.
Vam lahko služi: razlike med homogenimi mešanicami in heterogenimi mešanicamiR-oh
(Hidrofobna) - (hidrofilna)
Kot bo razloženo v naslednjem razdelku, Amfifilni značaj alkoholov določa nekatere njihove kemijske lastnosti.
Struktura r
Skupina Renta R ima lahko kakršno koli strukturo, vendar je pomembno, saj omogoča razvrščanje alkoholov.
Na primer, R je lahko odprta veriga, kot je to primer z etanolom ali propanolom, razvejano, na primer T-butil alkohol (ch3)2Chch2Oh, lahko je cikličen, kot v primeru cikloheksanola ali pa ima aromatičen obroč, kot pri benzilnem alkoholu (C6H5) Pogl2Oh, ali v 3-fenilpropanolu (c6H5) Pogl2Pogl2Pogl2Oh.
R veriga ima lahko celo substituente, kot so halogeni ali dvojne vezi, na primer za alkoholne 2-celice in 2-bunt-1-ol (ch3Pogl2= Chch2OH).
Glede na strukturo R postane klasifikacija alkoholov zapletena. Zato je razvrstitev na podlagi njegove strukture (1., 2. in 3. alkohola) lažja, vendar manj specifična, čeprav zadostuje za razlago reaktivnosti alkoholov.
Fizikalne in kemijske lastnosti
- Vrelišče: Ena glavnih lastnosti alkoholov je, da so povezani z vodikovimi mostovi. Zahvaljujoč temu so alkoholi običajno tekoči z visokimi vrelišči.
- Zmogljivost topila: V domovih se je zelo pogosto zateči k uporabi izopropilnega alkohola, da odstranite madež, ki ga je težko odstraniti na površini. Ta sposobnost topila, zelo uporabna za kemično sintezo, je posledica njegovega znaka amfropifila, ki je bila prej razložena. Za maščobe je značilno, da so hidrofobne: zato jih je težko odstraniti z vodo. Vendar imajo za razliko od vode alkoholi hidrofobni del v svoji strukturi. Tako njegova skupina Renta R sodeluje z maščobami, medtem ko skupina OH tvori vodikove mostove z vodo in jim pomaga premakniti.
- Anfoterizem: Alkoholi lahko reagirajo kot kisline in baze, torej so amftantne snovi. To je predstavljeno z naslednjima dvema kemijskima enačbama:
Roh + h+ => Roh2+
Roh + oh- => Ro-
Ro- Je splošna formula, ki je znana kot alcoksid.
Nomenklatura
Obstajata dva načina za imenovanje alkohola, katerih kompleksnost bo odvisna od njihove strukture.
Pogosto ime
Alkoholi lahko pokličete za njihova skupna imena. Če želite to narediti. Na primer CHO3Pogl2Pogl2Oh je propilico alkohol.
Vam lahko služi: heterogeni sistemDrugi primeri so:
- Pogl3OH: Metilni alkohol.
- (Pogl3)2Chch2OH: Isobutil alkohol.
- (Pogl3)3COH: TERT-BOUTYL ALLOH.
Sistem IUPAC
Kar zadeva skupna imena, morate začeti z identifikacijo r. Prednost tega sistema je, da je veliko natančnejši od drugega.
A, ker je ogljikov okostje, ima lahko posledice ali več verig. Najdaljša veriga, torej z več ogljikovimi atomi, je, na katero bo podeljeno ime alkohola.
Ime alkana je dodano ime najdaljše verige, doda se zaključek 'l'. Zato CHO3Pogl2Oh se imenuje etanol (cho3Pogl2- + OH).
Na splošno mora imeti najmanj možno naštevanje. Na primer BRCH2Pogl2Pogl2(OH) CHO3 Imenuje se 4-bromo-2-butanol in ne 1-bromo-3-butanol.
Sinteza
Hidracija alkenov
Postopek krčenja olja ustvari mešanico štirih ali petih ogljikovih atomov, ki se zlahka ločijo.
Ti alkeni lahko postanejo alkoholi z neposrednim dodajanjem vode ali z reakcijo alkena z žveplovo kislino, čemur sledi dodajanje vode, ki jo kislina razcepi, ki izvira iz alkohola.
OXO proces
V prisotnosti ustreznega katalizatorja alkeni reagirajo z ogljikovim in vodikovim monoksidom, da ustvarijo aldehide. Aldehido lahko zlahka zmanjšamo na alkohole s katalitično reakcijo hidrogenacije.
Pogosto obstaja takšna sinhronizacija procesa OXO, da je zmanjšanje aldehidosa skoraj istočasno z njihovo tvorbo.
Najbolj uporabljen katalizator je dekobalto oktokarbonil, ki ga dobimo z reakcijo med kobaltom in ogljikovim monoksidom.
Fermentacija ogljikovih hidratov
Fermentacija ogljikovih hidratov za kvas je še vedno zelo pomembna pri proizvodnji etanola in drugih alkoholov. Sladkorji prihajajo iz sladkornega trsa ali škroba, pridobljenega iz različnih zrn. Zaradi tega se etanol imenuje tudi "žitni alkohol"
Prijave
Pijača
- Čeprav to ni glavna funkcija alkoholov, je prisotnost etanola v nekaterih pijačah eno najbolj priljubljenih znanj. Tako je etanol, produkt fermentacije sladkornega trsa, grozdja, jabolka itd., Prisoten je v številnih pijačah za socialno porabo.
Kemična surovina
- Metanol se uporablja v proizvodnji formaldehida s svojo katalitično oksidacijo. Formaldehid se uporablja pri izdelavi plastike, slik, tekstila, eksploziva itd.
- Butanol se uporablja pri proizvodnji Butanoat Butana, estra, ki se uporablja kot aroma v živilski industriji in slaščičarni.
- Alilični alkohol se uporablja pri proizvodnji estrov, vključno z Dialilovim ftalatom in Dialilo isftalatom, ki služijo kot monomeri.
- Fenol se uporablja pri proizvodnji smol, proizvodnji najlona, deodorantov, kozmetiki itd.
- Linearni verižni alkoholi 11-16 ogljikovih atomov se uporabljajo kot posredniki za pridobivanje mehčalcev. Na primer polivinil klorid.
- Tako imenovani maščobni alkoholi se uporabljajo kot posredniki pri sintezi detergentov.
Topila
- Metanol se uporablja kot topilo za barvanje, pa tudi 1-butanol in izobutilni alkohol.
- Etilni alkohol se uporablja kot topilo številnih netopnih spojin v vodi, ki uporablja kot topilo v slikah, kozmetiki itd.
- Maščobni alkoholi se uporabljajo kot topila v tekstilni industriji, v barvilih, v detergentih in na slikah. Isobutanol se uporablja kot topilo v materialu za prevleke, slike in lepila.
Goriva
- Metanol se uporablja kot gorivo v notranjih in aditivnih bencinskih motorjih za izboljšanje zgorevanja.
- Etilni alkohol se uporablja v kombinaciji s fosilnimi gorivi v motornih vozilih. V ta namen so obsežne regije Brazilije namenjene gojenju sladkornega trsa za proizvodnjo etilnega alkohola. Ta alkohol ima prednost, da v svojem izgorevanju proizvaja samo ogljikov dioksid. Ko se kuri etilni alkohol, ustvari čist in brezdimen plamen, zato se uporablja kot gorivo v kuhinjah za kampanje.
- Gelificirani alkohol se proizvaja s kombinacijo metanola ali etanola s kalcijevim acetatom. Ta alkohol se uporablja kot toplotni vir v kampanjskih peči, in ko se razlije, je varnejši od tekočih alkoholov.
- Tako imenovani biobutanol se uporablja kot transportno gorivo, pa tudi izopropilni alkohol, čeprav njegova uporaba ni priporočljiva.
Antiseptiki
- 70% koncentracijski izopropilni alkohol se uporablja kot zunanji antiseptik za izločanje mikrobov in zaostalost njegove rasti, tako kot etilni alkohol.
Druge uporabe
- Cikloheksanol in metilcicloheksanol se uporabljata v tekstilnem zaključku, pohištvu predelanih in chitamanchas.
Primeri alkoholov in njihovih formul
- Metanol (pogl3OH).
- 1-propanol (c3H7OH).
- Etanol (c2H5OH).
- Isobutanol (c4H9OH).
- Izopropanol (c3H8Da).
- Allilični alkohol (c3H6Da).
- Benzilni alkohol (c7H8Da).
- Termična (c₄h₁₀o).
- Pentenol (c5HenajstOH).
- 2-butanol (pogl3-Pogl2-Choh-ch3).
- Fenol (c6H6Da).
- 2-propanol (pogl3-Choh-ch3).
- Izodekanol (c10H21OH).
- Cetilni alkohol (c16H3. 4Da).
- Propargilni alkohol (c3H4Da).
- Tetrahidrofuril alkohol (c5H10Tudi2).
- Cikloheksanol (c6H12Da).
- 2-klorotanol (c2H5Clo).
- Heptanol (c7H16Da).
- Heksanol (c₆h₁₄o).
Reference
- Organska kemija. MC Graw Hill.
- Alkoholi. Pridobljeno iz kolapreta.cm.Utexas.Edu.

