Ramificirani alkani
- 1241
- 91
- Raymond Moen
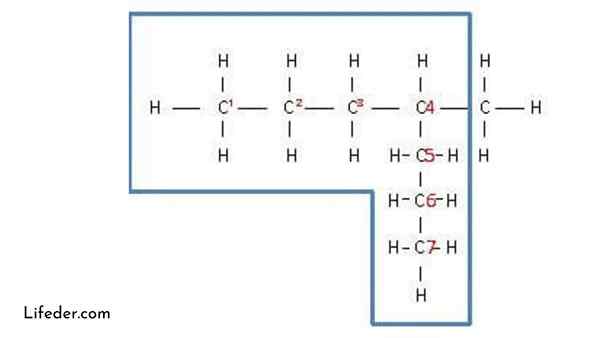 Ramificirani alkani so ogljikove in vodikove spojine, združene s preprostimi ogljikovimi ogljikovimi in ogljikovimi vodikovimi vezmi. Vir: Nilo Robles, javna domena, prek Wikimedia Commons
Ramificirani alkani so ogljikove in vodikove spojine, združene s preprostimi ogljikovimi ogljikovimi in ogljikovimi vodikovimi vezmi. Vir: Nilo Robles, javna domena, prek Wikimedia Commons Kaj so razvejani alkali?
The Ramificirani alkani So nasičeni ogljikovodiki, katerih strukture niso sestavljene iz linearne verige. So alkani z alkilnimi skupinami, združenimi z njegovo osrednjo ogljikovo verigo. Vsebujejo samo ogljikove in vodikove atome, združene s preprostimi ogljikovimi ogljikovimi ali ogljikovimi vodikovimi vezmi. Molekule imajo posledice in zato niso linearne.
Alkani linearnih verig se razlikujejo od njihovih razvejanih izomerov z dodajanjem pisma n pred imenom. Tako N-heksan pomeni, da struktura sestavlja šest ogljikovih atomov, poravnanih v verigi.
Veje osupljivega kozarca drevesa bi lahko primerjali z vejami razvejanih alkalcev; Vendar ima debelina njihovih verig, bodisi glavne, sekundarne ali terciarne, vse enake dimenzije. To je zato, ker so v vseh preprostih C-C povezavah prisotne.
Ko rastejo, se drevesa ponavadi podpirajo; Na enak način kot to počnejo alkani. Vzdrževanje konstantne verige z določenimi metilenskimi enotami (-CH2-) pomeni vrsto energetskih pogojev. Več energije imajo alkaoji, večja je nagnjenost k veji.
Tako linearni kot razvejani izomeri imajo enake kemijske lastnosti, vendar z majhnimi razlikami v njihovih vreliščih, fuziji in drugih fizikalnih lastnostih. Primer razvejanega alkana je 2-metil-profesionalna, najpreprostejša od vseh.
Kemične strukture razvejanih alkal
Ramificirani in linearni alkani imajo enako splošno kemijsko formulo: cnH2N+2. To je, da imata za določeno število ogljikovih atomov enako število vodikov. Zato sta dve vrsti spojin izomer: imata isto formulo, vendar različne kemijske strukture.
Vam lahko služi: berilij: zgodovina, struktura, lastnosti, uporabeKar je prvič opaziti v linearni verigi? Končno število metilenskih skupin, -ch2-. Tako, cho3Pogl2Pogl2Pogl2Pogl2Pogl2Pogl3 Gre za linearno verižno alkan, imenovan n-heptano.
Upoštevajte pet zaporednih metilenskih skupin. Prav tako je treba opozoriti, da te skupine sestavljajo vse verige, zato so iste debeline, vendar s spremenljivimi dolžinami. Kaj lahko še rečemo o njih? Ki so 2. ogljikovemu ogljiku, torej ogljikovi.
Tako da je ta n-heptano razbremenjen, je treba zadaj. Kot? Mehanizmi so lahko zelo zapleteni in pomenijo migracijo atomov in oblikovanje pozitivnih vrst, znanih kot karbokacije (-C+).
Vendar pa je na papirju dovolj, da strukturo naročite tako, da obstajajo 3. in 4. ogljikove ogljike; Z drugimi besedami, karboni so povezani s tremi ali štirimi. To novo naročilo je bolj stabilno kot dolge skupine skupin2 Ker sta 3. in 4. ogljik energijsko bolj stabilna.
Kemične in fizikalne lastnosti razvejanih alkal
Razvejani in linearni alkani, ki imajo enake atome, ohranjajo enake kemijske lastnosti. Njihove povezave ostajajo preproste, C-H in C-C in z malo razlike v elektronacijah, zato so njihove molekule apolarno. Razlika, omenjena zgoraj, leži v 3. in 4. ogljiku (CHR3 in cr4).
Ko pa je veriga razvejana v izomerih, spremeni način, kako molekule medsebojno delujejo.
Na primer, način, da dobite dve linearni veji drevesa. V prvi situaciji je veliko površnega stika, medtem ko v drugem prevladujejo "luknje" med vejami. Nekatere posledice bolj vplivajo na druge kot z glavno vejo.
Vam lahko služi: nepelometrijaVse to vodi do podobnih, vendar ne enakih vrednosti v mnogih fizikalnih lastnostih.
Vrele in fuzijske točke
Tekoče in trdne faze alkanov so podvržene medmolekularnim silam v določenih pogojih tlaka in temperature. Ker molekule razvejanih in linearnih alkanov ne delujejo na enak način, tudi njihove tekočine ali trdne snovi niso enake.
Fusion in vrelišča se povečajo s številom ogljika. Za linearne alkane so sorazmerne n. Toda za razvejane alkane je situacija odvisna od tega, kako razveja je glavna veriga in kakšne so nadomestne ali alkilične skupine (r).
Če se linearne verige štejejo za vrste cikcakov, se lahko popolnoma prilegajo drug drugemu; Toda pri vejah glavne verige skoraj ne delujejo, ker jih substituenti držijo drug od drugega.
Kot rezultat, imajo razvejani alkani nižjo molekulsko kontaktno površino, zato so njihove fuzijske in vrelišča ponavadi nekoliko manjše. Bolj ko bo struktura razvejana, mladoletniki bodo še vedno te vrednosti.
Na primer n-pentano (ch3Pogl2Pogl2Pogl2Pogl3) ima 36 PEB.1 ° C, medtem ko 2-metil-butan (izberite3Pogl2(Pogl3) Pogl2Pogl3) in 2,2-dimetil-profesionalni (C (CH (izberite3)4) od 27.8 in 9.5 ° C.
Gostota
Z istim sklepanjem so razvejani alkani nekoliko manj goste, saj zasedajo večji volumen, produkt spuščanja površinskega stika med glavnimi verigami.
Tako kot linearni alkani so tudi oni neizmerni z vodo in plavajo nad njo; to pomeni, da so manj goste.
Vam lahko služi: 7 najpomembnejših aplikacij za biokemijoNomenklatura in primeri
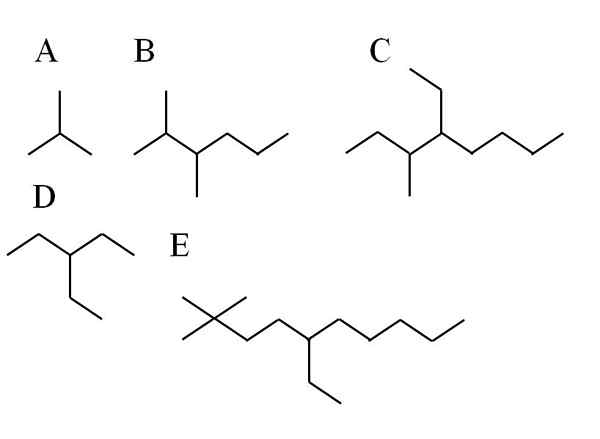
 Primeri razvejanih alkanov. Vir: Gabriel Bolívar
Primeri razvejanih alkanov. Vir: Gabriel Bolívar Na zgornji sliki je prikazanih pet primerov razvejanih alkal. Upoštevajte, da je za posledice značilno, da ima 3. ali 4. ogljikove ogljike. Kaj pa je glavna veriga? Da z največjim številom ogljikovih atomov.
- V A je ravnodušen, saj ne glede na to, katero verigo je izbrana, imata oba 3 c. Potem je njegovo ime 2-metil-profesionalno. Je butanski izomer, c4H10.
- Alcano B ima na prvi pogled dva substituenta in dolgo verigo. Skupinam -ch3 Navedeni so tako, da imajo najmanjše število; Zato se ogljikovemu ogljiku začnejo šteti z leve strani. Tako se B imenuje 2,3-dimetil-heksan.
- Za C velja enako kot v B. Glavna veriga ima 8 C in dva substituenta, CHO3 in pogl2Pogl3 So bolj na levi strani. Njegovo ime je torej: 4-etil-3-metiloktan. Upoštevajte, da je substituent -etil pred -metil omenjen po njegovem abecednem redu.
- V primeru D je ravnodušen, če se ogljikovi glavni verigi začnejo šteti. Njegovo ime je: 3-etil-propana.
- In končno za E, nekoliko bolj zapleteno razvejano alkano, glavna veriga je 10 C in začne iz katere koli od skupin CH3 z leve strani. Na ta način ji je ime: 5-etil-2,2-dimetil-decano.
Reference
- Carey, f. Do. (2006). Šesta izdaja organske kemije. MC Graw Hill uredništvo, strani 74–81.
- John t. Moore, Chris Hren, Peter J. Mikulecky. Kako poimenovati razvejane alkane v kemiji. Okrevano od: lutke.com
- Doktor. Ian Hunt. (2014). Preprosti razvejani alkani. Vzet od: kem.Ucalgary.AC
- Čelada, Anne Marie, ph.D. (8. januar 2018). Opredelitev alkane razvejane verige. Okreval od: Thoughtco.com
- Kemija librettexts. Alkani z razvejano verigo. Vzet od: kem.Librettexts.org
- Faceles: struktura in lastnosti. Vzeto od: UAM.je
- Nomenklatura: Alceans. [PDF]. Vzeto iz: Kemija.ti.Edu.co

