Acetonitril (C2H3N)
- 841
- 53
- Percy Feeney
Kaj je acetonitril?
On Acetonitril Je snov organskega izvora, sestavljenega samo iz ogljika, vodika in dušika. Ta kemična vrsta spada v skupino nitrilov, pri čemer je acetonitril najpreprostejša struktura med organskim tipom.
Nitriles so razred kemičnih spojin, katerih struktura sestavlja cianidna skupina (CN-) in radikalna veriga (-R). Ti elementi so predstavljeni z naslednjo splošno formulo: R-Cdajo.
Znano je, da ta snov izvira predvsem med proizvodnjo druge vrste, imenovane acrilonitrile (še en preprost nitril, molekularne formule C3H3N, ki se uporablja pri izdelavi izdelkov v tekstilni industriji) kot stranski produkt istega.
Poleg tega se acetonitril šteje za topilo s srednjimi lastnostmi polarnosti, zato se precej redno uporablja pri analizi RP-HPLC (kratica v angleščini za visoko učinkovito tekočo kromatografijo povratne faze).
Struktura
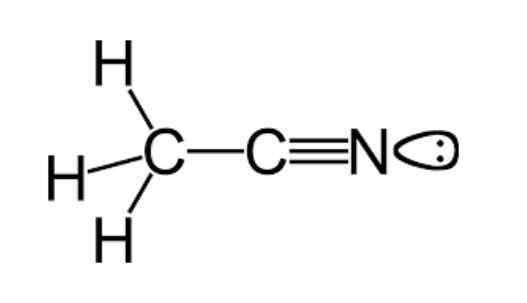
Kot smo že omenili, acetonitril spada v funkcionalno skupino nitrilov, pri čemer ima molekularno formulo, ki je običajno predstavljena kot C2H3N, ki jo lahko opazimo v strukturni formuli, ki je prikazana na zgornji sliki.
Ta slika prikazuje razred režnja, pritrjen na atom dušika, ki predstavlja par manjkajočih elektronov, ki jih ima ta atom, in ki mu daje velik del lastnosti reaktivnosti in stabilnosti, ki so značilne.
Na ta način ta vrsta kaže zelo posebno vedenje zaradi svoje strukturne ureditve, kar pomeni šibkost za prejemanje vodikovih vezi in malo sposobnosti darovanja elektronov.
Vam lahko služi: arzen: zgodovina, struktura, lastnosti, uporabePrav tako je ta snov prvič nastala v drugi polovici 1840-ih, ki jo je izdelal znanstvenik po imenu Jean-Baptiste Dumas, katerega državljanstvo je bilo francosko.
Strukturna konformacija te snovi omogoča to značilnost topila organske narave.
Ta lastnost omogoča, da se acetonitril meša z vodo, poleg niza drugih topil organskega izvora, razen ogljikovodikov ali nasičenih vrst ogljikovodikov.
Lastnosti Acetonitril
Ta spojina ima vrsto lastnosti, ki jo razlikujejo od drugih od istega razreda, ki so navedeni spodaj:
- Je v stanju združevanja tekočine v standardnih tlačnih in temperaturnih pogojih (1 atm in 25 ° C).
- Njegova molekularna konfiguracija ji daje molarno maso ali molekulsko maso približno 41 g/mol.
- Med organskimi vrstami velja za nitril, ki ima najpreprostejšo strukturo.
- Njegove optične lastnosti omogočajo brezbarvno v tej tekoči fazi in listo značilnosti, poleg tega, da imajo aromatičen vonj.
- Ima vnetno točko okoli 2 ° C, kar ustreza 35,6 ° F ali 275,1 K.
- Predstavlja vrelišče v območju od 81,3 do 82,1 ° C, gostota približno 0,786 g/cm3 in tališče med -46 do -44 ° C.
- Je manj gosta kot voda, vendar s tem in z različnimi organskimi topili.
- Manifestira dielektrično konstanto 38,8 poleg dipolnega momenta približno 3,92 d.
- Lahko raztopi najrazličnejše snovi ionskega izvora in ne -polarne narave.
- V analizi HPLC se precej uporablja kot mobilna faza, ki predstavlja visoke lastnosti vnetljivosti.
Uporaba/aplikacije
Med velikim številom aplikacij, ki jih ima acetonitril, je mogoče šteti naslednje:
- Podobno druge vrste nitrilov lahko to skozi proces presnove v mikrosomi (vezikularni elementi, ki so del jeter), zlasti v tem organu, za nastanek cianridne kisline.
- Uporablja se na zelo posplošeni način kot mobilna faza v vrsti analize, imenovane visoko učinkovita inverzna fazna tekoča kromatografija (RP-HPLC); to je kot eluentna snov, ki ima visoko stabilnost, veliko eluent in zmanjšano viskoznost.
- V primeru uporabe industrijske velikosti se ta kemična spojina uporablja v rafinerijah surove nafte kot topilo v določenih procesih, kot je čiščenje alkena, imenovanega Butadieno.
- Uporablja se tudi kot ligand (kemične vrste, ki se kombinira z atomom kovinskega elementa, ki se šteje za osrednje v dani molekuli, da tvori koordinacijsko spojino ali kompleksno) v velikem številu nitrilnih spojin s kovinami prehodne skupine.
- Podobno se uporablja v sintezi organskega tipa za veliko število kemikalij, ki so ugodne kot α-naftalenska kislina, tiamin ali acetamidin hidroklorid.
Tveganja
Tveganja, povezana z izpostavljenostjo acetonitrila, so raznolika. Med njimi je zmanjšana toksičnost, ko je izpostavljenost v manjšem obdobju in v nizkih količinah, presnavlja se za proizvodnjo cianhidrične kisline.
Prav tako obstajajo primeri ljudi, ki so se zastrupili s to kemijsko vrsto, zastrupljeni s cianidom, ki je prisoten v molekuli, potem ko so bili v različnih stopnjah stik z acetonitrilom (pri vdihavanju, zaužitju ali absorbiranju skozi kožo).
Vam lahko služi: oljni ali benzinski eter: formula, struktura, uporabaZaradi tega se posledice njegove toksičnosti zamujajo, ker telo te snovi ne zlahka presnavlja v cianidu, ker sta potrebna dva do dvanajst ur.
Vendar se acetonitril zlahka absorbira na območju pljuč in prebavil. Nato se njena porazdelitev zgodi po celotnem organizmu, dogaja se pri ljudeh in celo pri živalih ter doseže ledvice in vranico.
Po drugi strani je acetonitril poleg tveganj, ki jih predstavlja, predhodnik takšnih strupenih snovi, kot sta cianhidrika ali formaldehidna kislina. Celo njena uporaba v izdelkih, ki pripadajo kozmetičnemu območju v tako imenovanem evropskem gospodarskem območju leta 2000.

