Preobrazbe snovi
- 4981
- 966
- Mr. Shane Larkin
 Preobrazbe snovi so tiste transformacije, ki jih trpi, ne da bi spremenili njegovo sestavo. Na primer, voda v obliki tekočine, trdne (ledu) ali sode (parna) ostane voda
Preobrazbe snovi so tiste transformacije, ki jih trpi, ne da bi spremenili njegovo sestavo. Na primer, voda v obliki tekočine, trdne (ledu) ali sode (parna) ostane voda Kakšne so preobrazbe snovi?
Preobrazbe snovi so spremembe, ki jih to trpi, ne da bi se njegova sestava spremenila. Se pravi, da se snov spremeni, ko gre skozi fizične in kemične spremembe.
Primeri fizičnih sprememb so tvorba ledu, ko se temperatura spušča, rosa na listih, ki se pojavi zjutraj, dilatacija predmetov, ko se segreje, in magnetizacija telesa.
Oksidacija vijakov in nohtov je kemična sprememba, saj je oksid snov, ki se razlikuje od prvotnega železa. Vsekakor so spremembe v energiji potrebne, da se te preobrazbe zgodijo.
Preoblikovanje ledu je sprememba stanja, v katerem se voda strdi, vendar obstaja več možnosti. Snovi se pojavljajo v naravi in v laboratoriju v različnih državah, od katerih so plinski, tekoči in trdni trije najpogostejši, vsaj v zemeljskih razmerah.
Ker pa se zadeva spreminja, so znanstveniki naleteli na več stanj, nekoliko eksotične narave, na eksperimentalni in teoretični osnovi.
Trdimo lahko, da obstaja pet temeljnih stanj snovi:
- Trden
- Tekočina
- Plin
- Plazma
- Bose-Einstein kondenzat
Od tega so prvi trije stabilni v pogojih našega planeta, zadnji dve pa potrebujejo tehnološka sredstva, čeprav so v vesolju pogosti. Plazma je v resnici najpogostejše stanje snovi v kozmosu.
Temeljna stanja snovi
Pod tlačnim in temperaturnim pogojem Zemlje je snov običajno predstavljena v treh stanjih: trdna, tekočina in plin, medtem ko sta plazma in kondenzatna stanja Bose-einsteina v različnih pogojih, ki jih je mogoče doseči v laboratoriju.
Vam lahko služi: nekonvencionalni ukrepiDa bi razložili, zakaj, si je treba zapomniti, da je snov sestavljen iz delcev, povezanih s sili, tako privlačne kot odbojne. Sile privlačnosti, kot že ime pove, ponavadi sestavljajo delce, medtem ko imajo odbojni nasproten učinek.
Trdne snovi, tekočine in plini
Ko sile privlačnosti prevladujejo med delci, ostanejo blizu drug drugemu, skupaj v bolj ali manj fiksnih položajih, kar povzroča trdne snovi. Delci lahko vibrirajo, vendar ne opustijo svojega položaja znotraj trdne snovi, zato to ohranja določeno obliko in volumen.
V Tekočine, Sile privlačnosti omogočajo, da se delci nadaljujejo v bližini, vendar so manj intenzivni kot v trdnih snovi, saj jim omogočajo možnost, da se na določen način "zdrsnejo". Zaradi tega tekočine prilagodijo svojo obliko posodi, ki jih vsebuje, vendar ohranjajo fiksno glasnost.
Končno v Plini, Privlačne sile so še šibkejše, pretežno odbojne sile. Zaradi tega delci ostanejo dobro drug od drugega in z veliko večjo svobodo gibanja. Zaradi tega se plini širijo, dokler se na voljo količina popolnoma ne zavzema.
Bose-einstein kondenzat in kondenzat
Z dovolj ogrevalnim plinom se ioni in elektroni ločijo v postopku, ki se imenuje ionizacija, Na ta način a plazma v laboratoriju. Države plazme ni enostavno videti naravno v bližini Zemlje, vendar ga je mogoče videti v severni in južni luči.
Ta čudovit naravni pojav se pojavi, ko delci sončnega vetra, precej razpršena plazma, vplivajo na zemeljsko atmosfero in ionizirajo.
Na drugem koncu lestvice se veliko ohladi, tik nad absolutno ničlo se pojavi novo stanje snovi, v katerem je večina delcev v temeljnem stanju, ki je najnižja energija.
Lahko vam služi: najpomembnejši vidik majhne znanosti, velike znanosti in tehnoznanostiTo stanje se imenuje Bose-Einstein kondenzat, Fizikala Satyendra Bose in Albert Einstein, ki sta leta 1924 napovedala svoj obstoj.
Mnogo let pozneje, leta 1995, je več znanstvenikov uspelo prenesti zelo razredčene pline v to državo, kar je lahka naloga, če upoštevamo, da so temperature samo nano-Kelvina potrebne nad absolutno ničlo.
Državne spremembe v zadevi
V naravi je zelo pogosto, da se zadeva prenaša iz ene države v drugo. Običajno so te fizične spremembe posledica sprememb v tlaku in temperaturi, ki izhajajo iz povečanja ali zmanjšanja energije delcev.
Ko se materialu doda toplotna energija, se kinetična energija njegovih delcev poveča, kar zmanjša silo privlačnosti, ki jih ohranja v koheziji. Če je bil material v trdnem stanju, se lahko nato premakne v tekoče stanje ali celo gre neposredno v plinasto stanje.
Nasprotno, odstranjevanje dovolj toplotne energije je mogoče, da se plinasti material pretvori v tekočino ali da prehaja iz tekočine v trdno. Vsekakor se sestava snovi ne spremeni.
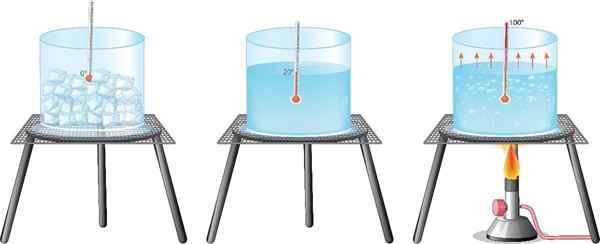
Najbolj znan primer za vse je voda: dobro je znano, da se porcija tekoče vode, ko ga zavre, pretvori v paro, medtem ko ga prehaja v ledeno hlajenje v zamrzovalnik.
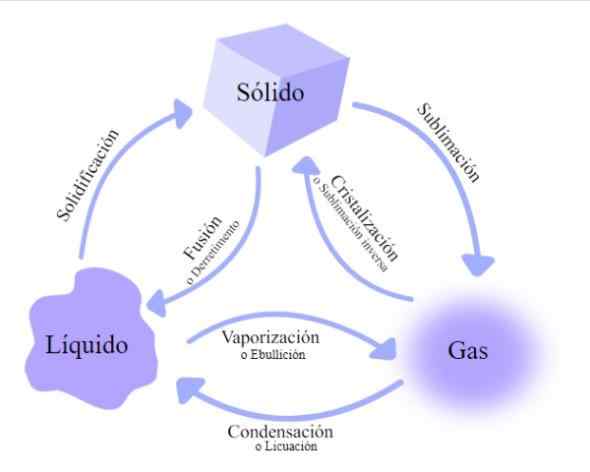 Spremembe v stanju snovi. Vir: Wikimedia Commons
Spremembe v stanju snovi. Vir: Wikimedia Commons Obstaja več menjalnih tečajev, skozi katere prenese zadevo, razvrščena glede na to, ali se toplotna energija povečuje ali zmanjšuje:
- Progresivno, Potekajo, ko material absorbira toplotno energijo.
- Regresivno, Oni so tisti, ki se pojavijo, ko material daje energijo.
Progresivne preobrazbe
Med različnimi progresivnimi preobrazbami, ki se v zadevi odvijajo z dodajanjem energije, so:
Fuzija
Sprememba, ki se pojavi, ko material prehaja iz svoje trdne faze v svojo tekočo fazo. Na primer s taljenjem ledenega bloka ali toplote ali voska v ponvi.
Uparjanje
V tem primeru zadevo pretvori tekoče stanje v plinasto stanje.
Vam lahko služi: metodologijaIzhlapevanje se pojavi na dva načina:
- Vreti, poteka, ko material doseže Temperatura vrenja, Na ta način je energija dovolj za premagovanje medmolekulskih sil, ki ohranjajo delce v njihovem tekočem stanju. Vsaka snov ima značilno temperaturo vrenja, ob določenem tlaku.
- Izhlapevanje, Samo površinski delci spreminjajo stanje, ker material ni pri temperaturi, ki je potrebna za vstop. Najbolj znan primer je izhlapevanje vode, ki je ostala v posodi, pri sobni temperaturi.
Hlapnost
Poklical tudi sublimacija, Poteka, ko se material pretvori neposredno iz plinske trdne snovi, ne da bi šel skozi tekočo fazo.
Na primer, suh led je ogljikov dioksid2 s hlapljivo pri sobni temperaturi. Naftalena, ki se uporablja za zaščito oblačil za žuželke, počasi preide od trdne do plinov.
Ionizacija
To je prehod plazemskega plina.
Regresivne transformacije
So transformacije, ki jih povzroča zmanjšanje toplotne energije delcev. Med njimi so:
Strjevanje
To je sprememba snovi iz tekočega stanja v trdno snov s hlajenjem, kot se zgodi pri namestitvi vode v zamrzovalnik. Postopek je zato, ker snov daje energijo v hladno okolje in tvori led.
Kondenzacija
Pojavi se pri prehodu iz plinastega stanja v tekočo fazo, kot z vodno paro v zraku, pri stiku s hladno površino avtomobilskega vetrobranskega stekla.
Utekočinjanje
To je preobrazba snovi pri prehodu iz plina v tekočino, kot se zgodi, hlajenje amoniaka ali visokotlačnega ogljikovega dioksida.
Inverzna sublimacija
To je prehod snovi v plinastemu do trdnem stanju, kot pri plinastem jodu, ki se spopada s hladno površino, kar ima za posledico nastanek trdnih kristalov. Znan je tudi kot kristalizacija.
Desionizacija
Sprememba stanja v plazmi v plinasto stanje.
Reference
- Chang, R. (2013). Kemija. 11VA. Izdaja. McGraw Hill Education.
- Giancoli, d. (2006 =. Fizika: načela z aplikacijami. 6. Ed Prentice Hall.
- Zadeva in njegove lastnosti. Okreval od: elbibliote.com.
- OpenTAX. Kemija. Pridobljeno iz: OpenStax.org.
- Shipman, j. (2009). Uvod v fizikalno znanost. Dvanajsta izdaja. Brooks/Cole, Cengage Editions.

