Teorija morja o temeljih in nepremičninah elektronov
- 1294
- 361
- Barry Ernser
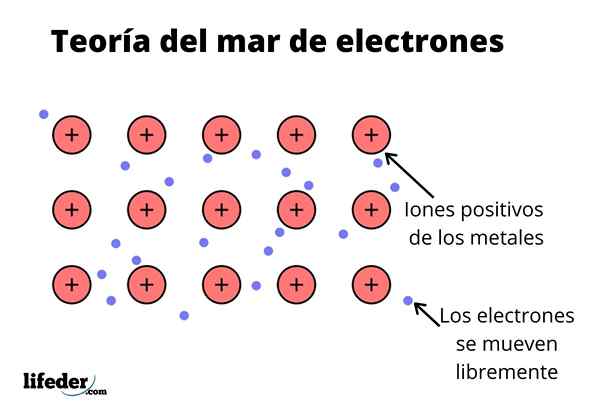
The Teorija elektronskega morja To je hipoteza, ki pojasnjuje izjemen kemični pojav, ki se pojavlja v kovinskih veznih med elementi z nizkimi elektronegativnostmi. To je delitev elektronov med različnimi združenimi atomi skozi kovinske vezi.
Elektronska gostota med temi vezmi je takšna, da se elektroni preselijo in tvorijo "morje", kjer se prosto gibljejo. Izrazi ga lahko tudi s kvantno mehaniko: nekateri elektroni (običajno jih je eden do sedem na atom) so razporejeni v orbitalih z več centri, ki jih raztegne kovinska površina.
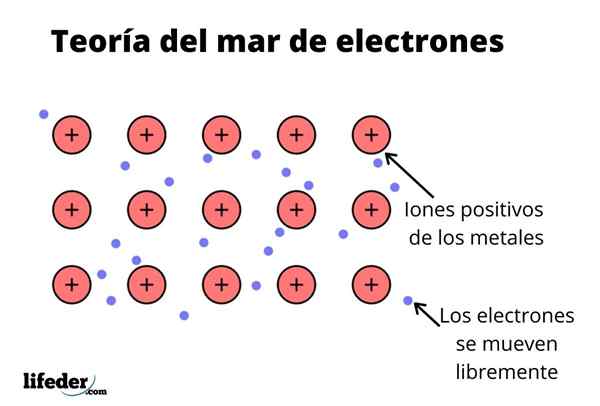
Tudi elektroni zadržijo nekaj lokacije v kovini, čeprav ima verjetnostna porazdelitev elektronskega oblaka večjo gostoto okoli nekaterih specifičnih atomov. To je zato, ker ko se uporabi določen tok, manifestirajo svojo prevodnost v določeni smeri.
[TOC]
Osnove teorije elektronskega morja
Kovinski elementi imajo veliko težnjo po doniranju elektronov svoje najnovejše energijske ravni (Valence Layer) zaradi nizke ionizacijske energije glede na druge elemente.
Če to vedo, bi lahko vsak kovinski element obravnavali kot kation, povezan z elektronom njegove zadnje ravni energije, ki bi bil bolj nagnjen k donaciji.
Kot v kovini je veliko atomov, ki so med seboj povezani, lahko domnevamo, da ta kovina tvori skupino kovinskih kationov, ki se potopijo v nekakšno morje valenčnih elektronov.
Glede na to, da imajo sile elektrostatične privlačnosti med kationom (pozitivno obremenitvijo) in elektronom (negativna obremenitev) atome kovine močno povezane, si predstavljajte selitev valenčnih elektronov, ki se obnašajo kot elektrostatično lepilo, ki se zadržuje povezano s kovinskimi kationi.
Vam lahko služi: polimeriNa ta način je mogoče sklepati, da bo večje število elektronov, prisotnih v plasti Valencije kovine, tovrstno elektrostatično lepilo večje trdnost.
Lastnosti
Teorija elektronskega morja ponuja preprosto razlago značilnosti kovinskih vrst, kot so odpornost, prevodnost, duktilnost in pokrajšalnost, ki se razlikujejo od ene kovine do druge.
Ugotovljeno je bilo, da je upor, dodeljen kovinam.
Na ta način je duktilnost znana kot sposobnost nekaterih materialov, da dovolijo deformacijo njihove strukture, ne da bi dali dovolj, da se prelomijo, ko so podvrženi določenim silam.
Delokalizacija v obliki plasti
Tako duktilnost kot pobožnost kovine sta določena z dejstvom, da so Valencia elektroni v vseh smereh v obliki plasti, zaradi česar se med seboj izpodrinejo pred delovanjem zunanje sile njegova deformacija.
Prav tako svoboda gibanja premeščenih elektronov omogoča pretok električnega toka, zaradi česar imajo kovine zelo dobro prevodnost električne energije.
Poleg tega ta pojav prostega gibanja elektronov omogoča prenos kinetične energije med različnimi kovinskimi regijami, kar spodbuja prenos toplote in kovine manifestira veliko toplotno prevodnost.
Lahko vam služi: jodozna kislina (HIO2): lastnosti in uporabeTeorija morja elektronov v kovinskih kristalih
Kristali so trdne snovi, ki imajo fizične in kemijske lastnosti - kot gostota, taljenje in trdota -, ki jih določajo vrste sil, ki delajo delce, ki jih sestavljajo skupaj.
Na nek način velja, da imajo kovinski kristali najpreprostejše strukture, ker je vsako "točko" steklene mreže zasedel atom same kovine.
V istem smislu je bilo ugotovljeno, da je struktura kovinskih kristalov na splošno kubična in se osredotoča na obraze ali telo.
Vendar imajo te vrste lahko tudi šesterokotno obliko in imajo dokaj kompaktno embalažo, kar jim daje tako ogromno gostoto, ki je značilna zanje.
Zaradi tega strukturnega razloga so povezave, ki so nastale v kovinskih kristalih, drugačne od tistih, ki se pojavljajo v drugih razredih kristalov. V celotni kristalni strukturi so elektroni, ki lahko tvorijo vezi, kot je razloženo zgoraj, že pojasnjeni.

Slabosti teorije
V kovinskih atomih je majhna količina valenčnih elektronov v sorazmerju z njihovo energijsko raven; To pomeni, da je na voljo večja količina energetskih stanj kot količina povezanih elektronov.
To pomeni, da se lahko elektronski premestitev in tudi energetski pasovi, ki so se delno napolnili, elektroni premikajo skozi retikularno strukturo, ko so podvrženi električnemu polju iz tujine, poleg tega, da tvorijo elektronski ocean, ki priznava prepustnost omrežje.
Vam lahko služi: oxácidoTako se zveza kovin razlaga kot konglomerat pozitivnih ionov, povezanih z morje elektronov (negativna obremenitev).
Vendar pa obstajajo značilnosti, ki se s tem modelom ne pojasnjujejo, na primer nastajanje nekaterih zlitin med kovinami s specifičnimi sestavinami ali stabilnost kolektivnih kovinskih povezav.
Te nevšečnosti pojasnjujejo s kvantno mehaniko, ker so bila ta teorija in številni drugi pristopi vzpostavljena na podlagi najpreprostejšega modela enega samega elektrona, medtem ko se poskušajo uporabiti v veliko bolj zapletenih strukturah multielektronskih atomov.
Reference
- Wikipedija. (2018). Wikipedija. Pridobljeno iz.Wikipedija.org
- Holman, J. S., In Stone, str. (2001). Kemija. Okrevano iz knjig.Google.co.pojdi
- Parkin, g. (2010). Kovinsko kovinsko vezanje. Okrevano iz knjig.Google.co.pojdi
- Rohrer, g. S. (2001). Struktura in vez v kristalnih materialih. Okrevano iz knjig.Google.co.pojdi
- Ibach, h., in Lüth, h. (2009). Fizika v trdni državi: uvod v načela znanosti o materialih. Okrevano iz knjig.Google.co.pojdi
- « Proces kulturne hibridizacije, vrste in primeri
- 20 turističnih krajev Aguascalientes (fotografije) »

