Vzroki, primeri, aplikacije in poskusi površinske napetosti

- 3177
- 214
- Roman Schamberger
The površinska napetost Fizična lastnost je, da so prisotne vse tekočine in zanj je značilna odpornost, da njihove površine nasprotujejo kakršnemu koli povečanju na svojem območju. To je isto, kot da bo ta površina iskala najmanj možno območje. Ta pojav prepleta več kemijskih konceptov, kot so kohezija, adhezija in medmolekularne sile.
Površinska napetost je odgovorna za nastanek krivulj površine tekočin v cevastih posodah (diplomirani jeklenki, stebri, epruvete itd.). Ti so lahko konkavni (dolinska ukrivljena) ali izbočena (ukrivljena kupola). Številne fizične pojave je mogoče razložiti glede na spremembe, ki jih je utrpela površinska napetost tekočine.
 Sferične oblike, ki jih sprejmejo kapljice vode na listih, so deloma posledica njihove površinske napetosti. Vir: Fotografija uporabnika Flickr Tanakawho [cc by (https: // creativeCommons.Org/licence/by/2.0)]
Sferične oblike, ki jih sprejmejo kapljice vode na listih, so deloma posledica njihove površinske napetosti. Vir: Fotografija uporabnika Flickr Tanakawho [cc by (https: // creativeCommons.Org/licence/by/2.0)] Eden od teh pojavov je trend, ki ga morajo molekule tekočin aglomerirati v obliki kapljic, ko počivajo na površinah, ki jih odbijajo. Na primer, kapljice vode, ki jih vidimo nad listi.
Vendar pride čas, ko gravitacija izvaja svojo vlogo in se kapljica razlije kot vodni stolpec. Podoben pojav se pojavi pri sferičnih kapljicah živega srebra, ko se termometer razlije.
Po drugi strani je napetost površinske vode najpomembnejša od vseh, saj prispeva in organizira stanje mikroskopskih teles v vodnih medijih, kot so celice in njihove lipidne membrane. Poleg tega je ta napetost odgovorna, da voda počasi izhlapi, in nekatera najgostejša telesa, ki lahko plavajo na njegovi površini.
[TOC]
Vzroki za površinsko napetost
Razlaga pojava površinske napetosti je na molekularni ravni. Molekule tekočine medsebojno delujejo, tako da so kohezivne v svojih zmotnih gibih. Molekula sodeluje s sosedi soseda in tistimi, ki so nad njo ali pod njo.
Vendar se to ne zgodi enako z molekulami površine tekočine, ki so v stiku z zrakom (ali katerim koli drugim plinom) ali s trdno snovjo. Površinske molekule ne morejo kohezivne s tistimi iz zunanjega okolja.
Posledično ne doživljajo nobene sile, ki bi jih pritegnila; Samo navzdol, od sosedov tekočega medija. Da bi preprečili to neravnovesje, so površinske molekule "stisnjene", ker jim šele takrat uspejo premagati silo, ki jih potisne navzdol.
Vam lahko služi: natrijev silikat (Na2Sio3): struktura, lastnosti, uporabe, tveganjaNato se ustvari površina, kjer so molekule v bolj napetosti. Če delček želi prodreti v tekočino, mora najprej prečkati to molekulsko pregrado, sorazmerno s površinsko napetostjo omenjene tekočine. Enako velja za delček, ki želi pobegniti v zunanje okolje iz globine tekočine.
Zato se njegova površina obnaša, kot da bi bila elastičen film, ki kaže odpor do deforme.
Enote
Površinska napetost je običajno predstavljena s simbolom γ in je izražena v n/m enotah, sili po dolžini. Vendar je večino časa vaša enota Dyn/Cm. Skozi naslednji faktor pretvorbe lahko postane drugi:
1 dyn/cm = 0,001 n/m
Napetost površinske vode
Voda je zahod in najbolj presenetljiva od vseh tekočin. Njegova površinska napetost in več lastnosti imajo nenavadno visoko vrednost: 72 Dyn/cm pri sobni temperaturi. Ta vrednost se lahko poveča na 75,64 DYN/CM, pri temperaturi 0 ° C; ali se zmanjšajo na 58,85 ° C pri temperaturi 100 ° C.
Ta opažanja so smiselna, če se šteje, da je molekularna pregrada še bolj napeta pri temperaturah blizu zamrzovalne točke ali "popusti" še malo okoli vrelišča.
Voda ima veliko površinsko napetost po svojih vodikovih mostovih. Če so ti razvpitni znotraj tekočine, so še bolj na površini. Molekule vode so močno prepletene z oblikovanjem dipol-dipolo interakcij tipa H2Oh oh.
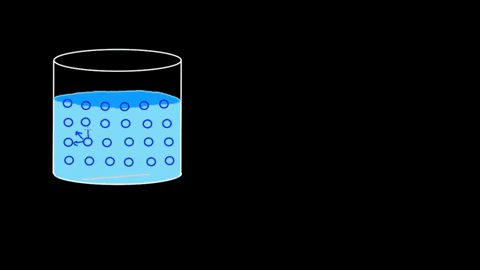 Molekule vode pritegnejo drug drugega; Povezujejo jih z vodikovimi mostovi
Molekule vode pritegnejo drug drugega; Povezujejo jih z vodikovimi mostovi Učinkovitost njegovih interakcij je taka, da lahko vodna molekularna pregrada sploh vzdrži nekatera telesa, preden potopijo. V razdelkih aplikacij in poskusov se bo ta točka nadaljevala.
Drugi primeri
Vse tekočine imajo površinske napetosti, bodisi v manjši ali večji meri kot v vodi, ali če so čiste snovi ali rešitve. Kako močne in napete so molekularne ovire njihovega površnega, bo odvisno od njegovih medmolekulskih interakcij, poleg strukturnih in energetskih faktorjev.
Kondenzirani plini
Na primer, molekule gase v tekočem stanju medsebojno medsebojno sodelujejo s pomočjo disperzivnih sil v Londonu. To se strinja z dejstvom, da imajo njihove površinske napetosti nizke vrednosti:
-Tekoči helij, 0,37 Dyn/cm A -273 ° C
Lahko vam služi: amonijev klorid (NH4Cl)-Tekoči dušik, 8,85 Dyn/cm A -196 ° C
-Tekoči kisik, 13,2 Dyn/cm A -182 ° C
Površinska napetost tekočega kisika je večja kot pri heliju, ker imajo njegove molekule večjo maso.
Apolarne tekočine
Od apolarnih in organskih tekočin naj bi imeli večje površinske napetosti kot v teh kondenziranih plinih. Med nekaterimi imamo naslednje:
-Dieteter, 17 Dyn/cm pri 20 ° C
-n-Hexano, 18,40 Dyn/cm pri 20 ° C
-n-Octane, 21,80 Dyn/cm pri 20 ° C
-Toluene, 27,73 Dyn/cm pri 25 ° C
Podoben trend opazimo pri teh tekočinah: površinska napetost se poveča, ko se molekularna masa povečuje. Vendar n-Octane bi moral imeti v skladu s tem največjo površinsko napetost in ne toluen. Tu se začnejo igrati molekularne strukture in geometrije.
Molekule toluena, načrta in anilres imajo učinkovitejše interakcije kot tiste n-oktan. Zato je površina toluena "napeta" kot površina n-oktan.
Polarne tekočine
Biti močnejši dipol-dipol. Vendar ni vedno tako. Med nekaterimi primeri imamo:
-Ocetna kislina, 27,60 Dyn/cm pri 20 ° C
-Aceton, 23,70 Dyn/cm pri 20 ° C
-Kri, 55,89 Dyn/cm pri 22 ° C
-Etanol, 22,27 Dyn/cm pri 20 ° C
-Glicerol, 63 Dyn/cm pri 20 ° C
-Molten natrijev klorid, 163 Dyn/cm pri 650 ° C
-NaCl 6 m raztopina, 82,55 Dyn/cm pri 20 ° C
Pričakuje se, da bo staljeni natrijev klorid ogromno površinske napetosti: je viskozna in ionska tekočina.
Po drugi strani je Merkur ena izmed tekočin z najvišjo površinsko napetostjo: 487 Dyn/cm. V njej je njegova površina sestavljena iz močno kohezivnih atomov živega srebra, veliko več, kot so lahko molekule vode.
Prijave
 Nekatere žuželke uporabljajo površinsko napetost vode za hojo po njej. Vir: Pixabay.
Nekatere žuželke uporabljajo površinsko napetost vode za hojo po njej. Vir: Pixabay. Površna napetost sama nima aplikacij. Vendar to ne pomeni, da ni vključen v več vsakodnevnih pojavov, da če ne bi bilo, se ne bi zgodilo.
Na primer, komarji in druge žuželke se lahko sprehodijo skozi vodo. To je zato, ker njihove hidrofobne noge odbijajo vodo, hkrati pa jim njihova mala masa omogoča.

Površna napetost izpolnjuje tudi vlogo pri vlaženju tekočine. Večja kot je površna napetost, manj je nagnjenost k puščanju skozi pore ali piščanci materiala. Poleg tega so malo uporabne tekočine za čiščenje površin.
Vam lahko služi: reakcija nevtralizacijeDetergenti
Tukaj delujejo detergenti, zmanjša površinsko napetost vode in pomaga, da pokrije večje površine; Med izboljševanjem vašega razmaščenega dejanja. Z zmanjšanjem površinske napetosti sprejme molekule zraka, s katerimi se tvorijo mehurčki.
Emulzije
Po drugi strani so nizke višje napetosti povezane s stabilizacijo emulzij, zelo pomembne pri oblikovanju različnih izdelkov.
Preprosti poskusi
 Kovinska sponka, ki plava zaradi napetosti na površini. Vir: AlvesGaspar [CC by-S (https: // creativeCommons.Org/licence/by-sa/3.0)]
Kovinska sponka, ki plava zaradi napetosti na površini. Vir: AlvesGaspar [CC by-S (https: // creativeCommons.Org/licence/by-sa/3.0)] Nazadnje bodo navedeni nekateri poskusi, ki jih je mogoče izvesti v katerem koli domačem prostoru.
Poskus posnetka
V kozarcu s hladno vodo je na njegovi površini nameščena kovinska sponka. Kot je razvidno iz zgornje slike, bo posnetek zaradi površinske napetosti vode ostal na plaži. Če pa v kozarec dodamo malo lava loza, se bo površinska napetost drastično zmanjšala in posnetek se bo nenadoma potopil.

Papirnata ladjica
Če imamo papirnato ladjo ali leseno paleto in če operete malega ali detergenta, ga dodamo v glavi brisa, potem bo prišlo do zanimivega pojava: prišlo bo kozarca. Papirna ladja in lesena paleta se bosta oddaljila od brisa, razmazanega z detergentom.

Drug podoben in bolj grafični poskus je ponoviti isto operacijo, vendar v vedru vode, razpršene s črnim poprom. Delci črnega paprika se bodo odselili in površina bo šla od popra, da bo kristalna, z robovi na robovih.
Reference
- Whitten, Davis, Peck & Stanley. (2008). Kemija. (8. izd.). Cengage učenje.
- Wikipedija. (2020). Površinska napetost. Pridobljeno iz: v.Wikipedija.org
- USGS. (s.F.). Površinska napetost in voda. Pridobljeno od: USGS.Gov
- Jones, Andrew Zimmerman. (12. februar 2020). Površinska napetost - definicija in poskusi. Okreval od: Thoughtco.com
- Susanna Lauren. (15. november 2017). Zakaj je površinska napetost pomembna? Biolin znanstveni. Obnovi se od: blog.BioLinscientific.com
- Znanost za starševstvo. (7. november 2019). Kaj je površinska napetost | Kul znanstveni eksperiment. Okrevano od: Rookieparent.com
- Jessica Mock. (2020). Eksperiment s površinsko napetostjo. Študij. Okrevano od: študij.com
- Otrok bi moral to videti. (2020). Sedem eksperimentov površinske napetosti - Fizika Girl. Okreval od: the lahko.com

