Struktura TechNecio (TC), lastnosti, uporabe, pridobivanje
- 1302
- 366
- Roman Schamberger
On Tecnecio (TC) je kemični element skupine VII periodične tabele. Vaša atomska številka je 43. Njegovo ime izhaja iz grške besede "Tekhnetos", kar pomeni umetno, in je bilo dodeljeno, ker je bilo takrat odkrito, da je bilo umetno ustvarjeno. Dandanes je znano, da je naravno v Zemljini skorji, čeprav le v drobnih količinah.
Je radioaktivna kovina. Ima veliko izotopov, ki so atomi Technecium z različnimi količinami nevtronov v jedru. Zavzemajo isto mesto v periodični tabeli, vendar imajo različne atomske mase.
 Simbol atomskega števila in atomska masa elementa Tecnecio. Jaz/cc by-sa (https: // creativeCommons.Org/licence/by-sa/2.5). Vir: Wikimedia Commons.
Simbol atomskega števila in atomska masa elementa Tecnecio. Jaz/cc by-sa (https: // creativeCommons.Org/licence/by-sa/2.5). Vir: Wikimedia Commons. Vsi njegovi izotopi imajo kratko življenje v primerjavi z zemljo, tako.
Najpomembnejša izotopa je Tecnecio-99m, ki se v nuklearni medicini pogosto uporablja za diagnozo različnih bolezni.
Tecnecio nastaja v jedrskih reaktorjih. Zaznana je bila tudi njegova prisotnost v zvezdnih zadevah.
[TOC]
Struktura
Njegova elektronska konfiguracija je:
1s2 2s2 2str6 3s2 3str6 3d10 4s2 4str6 4d5 5s2,
ali tudi:
[KR] 4d5 5s2.
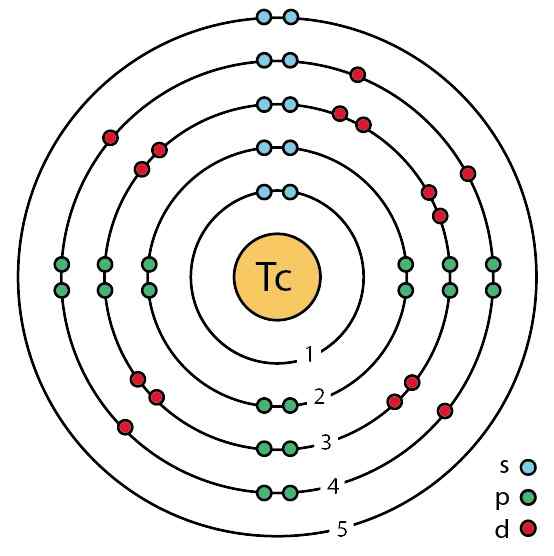
Spodaj je model bohr tecnecio atoma, kjer je mogoče videti različne orbitale s svojimi elektroni okoli jedra.
 Elektroni v orbitalah atoma Tecnecio. Ahazard.Sciencewriter/CC BY-SA (https: // creativeCommons.Org/licence/by-sa/4.0. Vir: Wikimedia Commons.
Elektroni v orbitalah atoma Tecnecio. Ahazard.Sciencewriter/CC BY-SA (https: // creativeCommons.Org/licence/by-sa/4.0. Vir: Wikimedia Commons. Kristalizira v kompaktni šesterokotni razporeditvi ali omrežju.
Nomenklatura
- Tecnecio, simbol: TC
- 99TCM, 99mTC, TECNECIO-99M: Različni načini označevanja izotopa metero, ki ga je mogoče določiti z atomsko maso 99
- Tecnecio-95m: metajljiv izotop z atomsko maso 95
Lastnosti
Fizično stanje
Kovinsko trdno s srebrno svetlostjo.
 Zlati list, prevlečen s tecnecio. Ampule, ki ga vsebuje, je zapečaten in je poln inertnega plina argona. Marco Cardin/CC by-S (https: // createCommons.Org/licence/by-sa/4.0. Vir: Wikimedia Commons.
Zlati list, prevlečen s tecnecio. Ampule, ki ga vsebuje, je zapečaten in je poln inertnega plina argona. Marco Cardin/CC by-S (https: // createCommons.Org/licence/by-sa/4.0. Vir: Wikimedia Commons. Standardna atomska masa
98
Tališče
2157 ° C
Vrelišče
4262 ° C
Gostota
11 g/cm3
Topnost
Raztopi se v dušikovi kislini (hno3), V Regia agua (ki je mešanica hno3 koncentrirani koncentrat) in koncentrirana žveplova kislina (H2SW4). Je netopna v klorovodiki (HCl) ali fluorhorični (HF).
Kemične lastnosti
Stanja oksidacije, ki jih ta element sprejme, so +4, +5 in +7. Tecnecio počasi izgubi svojo kovinsko svetlost, ko je izpostavljen vlažnemu zraku, saj pride do oksocida.
Vam lahko služi: ionska povezava: značilnosti, kako se oblikuje, in primeriGori kisik nad 400 ° C, da daje TC oksid2Tudi7 ki sublima (neposredno prehaja iz trdnega v plin). Ne reagira z vodikovim peroksidom (h2Tudi2).
Izotopi
Tecnecio ima 22 izotopov. Izotopi so atomi istega elementa, ki imajo v jedru različne količine nevtronov, zato imajo različne mase. Vsi so torej radioaktivni, torej nestabilni in imajo atomske mase med 90 in 111.
Izotopi z daljšim povprečnim življenjem so: 97TC, katerega polovico življenja je 4,2 × 106 leta, 98TC s polovico 6,6 × 106 leta in 992.1 × 10 TC5 leta. Napol je povprečni čas, ki ga potrebuje za radioaktivni izotop.
 Laboratorijski zvonec, posebej zasnovan s stekleno in svinčeno steno, za ravnanje s Tecnecio, katerega izotopi so vsi radioaktivni. Jejecam/cc by-sa (https: // createCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons.
Laboratorijski zvonec, posebej zasnovan s stekleno in svinčeno steno, za ravnanje s Tecnecio, katerega izotopi so vsi radioaktivni. Jejecam/cc by-sa (https: // createCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons. Biokemično vedenje
Čeprav ta element v živih bitjih nima biokemične funkcije, se lahko kemično pridruži številnim biološko aktivnim molekulam.
Pridobivanje
Odkritje
To je bil prvi element, ki je bil umetno proizveden. Njegov obstoj je napovedal ruski kemik Dmitri Mendeléjev v devetnajstem stoletju, ki je svoje trenutno mesto dodelil v periodični tabeli.
Šele leta 1937 so ga odkrili v vzorcu molibdena, ki so ga v fizičnem laboratoriju v Berkeleyju bombardirali z nevtroni. Od tega trenutka je začel iskati kopenske materiale.
Malo naravne prisotnosti
Leta 1962 so ga v Afriki našli v naravnem mineralu v Uraniniti kot produkt spontane cepitve urana-238. Njegova koncentracija v tej vrsti kamnine je izjemno majhna.
Zaznana je bila njegova prisotnost v nekaterih vrstah zvezd, kar je privedlo do novih teorij o proizvodnji težkih elementov v zvezdni snovi.
Proizvodnja
Umetno nastane v jedrskih reaktorjih iz uranove cepitve. Izvleče se iz porabljenih jedrskih gorivnih palic v obliki sivega prahu.
Za vsako tono urana nastane tecnecio miligram. Trenutno obstajajo zelo velike količine (tone), ki so se z leti nabrale.
Vam lahko služi: živo srebro: struktura, lastnosti, pridobivanje, uporabe Pridobivanje Tecnecio-99m v laboratoriju leta 1958. Nacionalni laboratorij v Brookhavenu. / Javna domena. Vir: Wikimedia Commons.
Pridobivanje Tecnecio-99m v laboratoriju leta 1958. Nacionalni laboratorij v Brookhavenu. / Javna domena. Vir: Wikimedia Commons. Prijave
- Na področju jedrske medicine
Tecnecio-99m (kjer "m" pomeni metastabilno) je izotop, ki se najbolj uporablja. Ima pol življenja 6,01 ure. Široko se uporablja za medicinske diagnostične študije, saj oddaja gama žarke.
Uporaba njihovih kombinacij z drugimi kemičnimi snovmi se vbrizga v bolnike, ki jih bomo ocenili. Ko je v organizem vstavljen, ga absorbirajo nekateri organi in gama žarki, ki jih oddajajo, omogočajo pridobivanje slik različnih delov telesa.
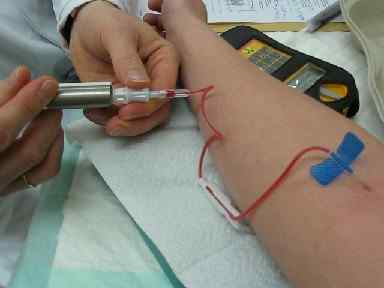 Vbrizgavanje tecnecio-99m spojin za izvajanje tomografij v jedrski medicini. Bionerd/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons.
Vbrizgavanje tecnecio-99m spojin za izvajanje tomografij v jedrski medicini. Bionerd/cc by-sa (https: // creativeCommons.Org/licence/by-sa/3.0. Vir: Wikimedia Commons. Srce
Ko se Tecnecio-99M pridruži pirofosfatu, se lahko drži kalcijevih nahajališč poslabšanih mišic srca, kar omogoča oceno lezij, ki jih povzroča srčni infarkt.
Arterije in žile
Če je v kombinaciji s kositrno spojino, se pridruži rdečim krvnim celicam in služi za izdelavo zemljevida motenj krvnega sistema.
Vranica
Skupaj z žveplom se nabira v vranici in jasno podobo omenjenega organa je mogoče dobiti.
Spodaj je primer vrste pridobljenih slik zahvaljujoč gama žarkom, ki jih je izdal Tecnecio-99m:
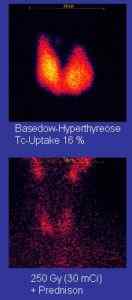 Gamografije slike vratnega območja, kjer je mogoče videti ščitnico. Dobimo jih s TC-99M. Brezplačna uporaba MBQ / CopyRished. Vir: Wikimedia Commons.
Gamografije slike vratnega območja, kjer je mogoče videti ščitnico. Dobimo jih s TC-99M. Brezplačna uporaba MBQ / CopyRished. Vir: Wikimedia Commons. Kosti
TC-99M se uporablja za oceno stopnje aktivnosti osteoblastov v kostni leziji. Osteoblasti so kostne celice, ki ustvarjajo kostno matrico.
Skeniranje ali raziskave s tem izotopom so zelo občutljive in omogočajo odkrivanje metastaz (širjenje rakavih celic) in limfomov v kosteh (maligna proliferacija limfocitov v kostnem mozgu).
Možgani
Etilcisteinatni dimer 99mTC zlahka absorbira možgansko tkivo, kar vam omogoča, da pridobite slike tega organa s pomočjo računalniške monofotonske emisijske tomografije.
- Druge uporabe
V obliki ionov pertekneta (TCO4-) deluje kot zaviralec korozije za jeklo, ki je še vedno v zelo majhnih količinah. Vendar ga je treba uporabiti v zaprtih sistemih zaradi radioaktivnosti Tecnecio.
Lahko vam služi: nikelj hidroksid (III): struktura, lastnosti, uporabe, tveganjaPri temperaturi 11 K (-262,15 ° C) ali nižji se obnaša kot izjemen superprevodnik.
Tecnecio-95m je izotop, ki ima razpolovno dobo 61 dni in se uporablja kot radioaktivni marker ali sledil v ekologiji, na primer za sledenje onesnaževalski spojini in preučiti gibanje površinskih voda.
- Potencialne aplikacije
Je učinkovitejši katalizator kot renio (re) ali paladij (PD) v reakciji dehidrogenacije izopropilnega alkohola. Predlagana je bila tudi njegova uporaba v jedrskih baterijah.
Toda njegova radioaktivnost je težava za te uporabe.
Tveganja
Zdravje
Je radioaktiven, zato zelo škodljiv za zdravje živih bitij. Ocenjuje se, da je človeška izpostavljenost temu elementu večinoma posledica uporabe 99TCM v jedrski medicini.
 Simbol, ki označuje nevarnost sevanja. Avtor: katalonski katalino. Vir: Pixabay.
Simbol, ki označuje nevarnost sevanja. Avtor: katalonski katalino. Vir: Pixabay. V takih primerih se ta izotop čez nekaj časa odlaga predvsem v ščitnico in prebavili.
Atmosfera
Ker ga jedrski reaktorji proizvajajo v velikih količinah, je Tecnecio dodatna obremenitev, ki se veže na neželene radioaktivne odpadke na planetu.
Reference
- Royal Society of Chemistry. (2020). Technetium. RSC je bil obnovljen.org.
- Lentech b.V. (2020). Technetium - TC. Okreval od Lentecha.com.
- Andersen, ali. (2016). Dekoracija radionuklidov. Technetium. Pri kelacijski terapiji pri zdravljenju zastrupitve s kovino. Okrevano od Scientirect.com.
- Lor Randall, R. (2010). Pristop k diagnozi tumorjev kosti in mehkih tkiv - kliničnih, radioloških in klasifikacijskih vidikov. V patologiji kosti in mehkih tkiv. Okrevano od Scientirect.com.
- Infeld, b. in Davis, s.M. (2004). En-Thoton Issussion Compute Tomography. 99mTC-ECD SPECT. V Stroke (četrta izdaja). Okrevano od Scientirect.com.
- Bombaž, f. Albert in Wilkinson, Geoffrey. (1980). Napredna anorganska kemija. Četrta izdaja. John Wiley & Sons.
- Svinec, d.R. (Urednik) (2003). Priročnik za kemijo in fiziko CRC. 85th CRC Press.

